
题目列表(包括答案和解析)
 g
g


 g
g
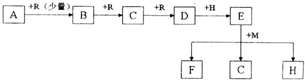
以煤为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业叫煤化工.
(1)将水蒸气通过红热的碳即可产生水煤气.反应为:
C(s)+H2O(g)①该反应在常温下________自发进行(填“能”与“不能”);
②恒温,在容积可变的密闭容器中,进行如上可逆反应.一段时间后,下列物理量不发生变化时,能表明该反应已达到平衡状态的有________
Ⅰ混合气体的密度;
Ⅱ容器内气体的压强;
Ⅲ混合气体的总物质的量;
ⅣCO物质的量浓度
A.只有Ⅳ
B.只有Ⅰ和Ⅳ
C.只有Ⅱ和Ⅲ
D.Ⅰ、Ⅲ和Ⅳ
(2)水煤气再进一步反应可制取氢气.反应为H2O(g)+CO(g)![]() H2(g)+CO2(g),某温度下该反应的平衡常数K=4/9.该温度下在甲、乙、丙三个恒容密闭容器中,只投入H2(g)和CO2(g),其起始浓度如下表所示.下列判断不正确的是________.
H2(g)+CO2(g),某温度下该反应的平衡常数K=4/9.该温度下在甲、乙、丙三个恒容密闭容器中,只投入H2(g)和CO2(g),其起始浓度如下表所示.下列判断不正确的是________.
A.反应开始时,丙中的反应速率最快,甲中的反应速率最慢
B.平衡时,甲中和丙中H2的转化率均是60%
C.平衡时,丙中c(CO2)是甲中的2倍,是0.012 mol/L
D.平衡时,乙中CO2的转化率大于60%
(3)目前工业上有一种方法是用CO2来生产甲醇.一定条件下发生反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g),下图表示该反应进行过程中能量(单位为kJ·mol-1)的变化.在体积为1 L的恒容密闭容器中,充入1 mol CO2和3 mol H2反应
CH3OH(g)+H2O(g),下图表示该反应进行过程中能量(单位为kJ·mol-1)的变化.在体积为1 L的恒容密闭容器中,充入1 mol CO2和3 mol H2反应
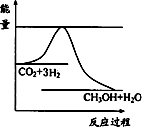
①下列措施中能使c(CH3OH)增大的是________.
A.升高温度
B.充入He(g),使体系压强增大
C.将H2O(g)从体系中分离出来
D.再充入1 mol CO2和3 mol H2
②在温度T1时,当反应达到平衡时,测得n(H2)=2.4 mol;其它条件不变,在温度T2时,当反应达到平衡时,测得n(CO2)=0.82 mol,则T2________T1.(填“>”、“<”或“=”)
(4)在一定条件下科学家从烟道气中分离出CO2与太阳能电池电解水产生的H2合成甲醇.CH3OH、H2的燃烧热分别为:ΔH=-725.5 kJ/mol、ΔH=-285.8 kJ/mol.
①写出工业上以CO2、H2合成CH3OH和液态水的热化学方程式:________;
②该转化的积极意义是________;
③有人提出,可以设计反应CO2=C+O2(ΔH>0、ΔS<0)来消除CO2对环境的影响.请你判断是否可行并说出理由:________
| 起始浓度 | 甲 | 乙 | 丙 |
| c(H2)/mol/L | 0.010 | 0.020 | 0.020 |
| c(CO2)/mol/L | 0.010 | 0.010 | 0.020 |
| 起始浓度 | 甲 | 乙 | 丙 |
| c(H2)/mo1/L | 0.010 | 0.020 | 0.020 |
| c(CO2)/moI/L | 0.010 | 0.010 | 0.020 |
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
D
D
A
B
D
D
C
D
B
B
B
C
C
A
C
C
B
A
19.(8分)( 1 ) B D ( 2 分)
(2)一定有 NO3-、Al3+、SO42-(2分); 一定无 Fe3+、Ba2+、HCO3-(2分)
(3) Al3+ + 3 NH3?H2O = Al(OH)3↓+3NH4+ (2分)
 20.(10分)(一)(1)2NH4Cl
+ Ca(OH)2 CaCl2+2NH3↑+2H2O (2分)
20.(10分)(一)(1)2NH4Cl
+ Ca(OH)2 CaCl2+2NH3↑+2H2O (2分)
|