
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
КюЪЯжЦМюЗЈЫљЕУДПМюбљЦЗжаЭљЭљКЌгаЩйаэNaClЃЌЯжгћВтЖЈЦфжаNa2CO3ЕФжЪСПЗжЪ§ЃЌЗжБ№ЩшМЦСЫШчЯТЪЕбщЗНАИЁЃ
ЗНАИвЛЃКГСЕэЗжЮіЗЈ
ЃЈ1ЃЉАбвЛЖЈСПЕФбљЦЗШмНтКѓМгШыЙ§СПCaCl2ЃЌНЋЫљЕУГСЕэ ЃЈЬюВйзїЃЉЁЂЯДЕгЁЂКцИЩЁЂГЦСПЁЃШЗЖЈCaCl2ШмвКЪЧЗёЙ§СПЕФЗНЗЈЪЧ ЃЛЯДЕгГСЕэЕФВйзїЪЧ ЁЃ
ЗНАИЖўЃКЦјЬхЗжЮіЗЈ

ЃЈ2ЃЉАбвЛЖЈСПЕФЛьКЯЮягызуСПбЮЫсЗДгІКѓЃЌгУШчЭМзАжУВтЖЈВњЩњЕФCO2ЦјЬхЕФЬхЛ§ЃЌЮЊМѕаЁCO2ЕФШмНтЃЌBжаШмвКЮЊ ЃЌЕЋбЁгУИУШмвККѓЪЕбщНсЙћШдШЛЛЙЪЧВЛзМШЗЃЌЦфдвђЪЧ ЁЃ
ЃЈ3ЃЉЪЕбщЪвжаЯжгабЮЫсЁЂЬьЦНЁЂеєЗЂУѓЁЂВЃСЇАєЁЂЬњМмЬЈЯЕСаЁЃЧыФуЩшМЦвЛИіаТЕФЗНАИЃЌВтЖЈДПМюбљЦЗжаNa2CO3ЕФКЌСП ЁЃ
| 106W3 |
| 197W1 |
| 106W3 |
| 197W1 |
| 53(W3-W1) |
| 22W2 |
| 53(W3-W1) |
| 22W2 |
ЃЈ18ЗжЃЉЙЄвЕЩњВњЕФДПМюжаГЃКЌгаЩйСПNaClдгжЪЁЃЮЊВтЖЈФГДПМюбљЦЗЕФДПЖШЃЌЛЏбЇПЮЭтЛюЖЏаЁзщЩшМЦСЫШ§жжЪЕбщЗНАИЃК
ЁОЗНАИвЛЁПШЁбљЦЗШмНтКѓЃЌМгЪдМСЪЙCO32ЃГСЕэЃЌВтЖЈГСЕэЕФжЪСПЁЃ
ЁОЗНАИЖўЁПгУ0.100mol/LбЮЫсЕЮЖЈЁЃ
ЁОЗНАИШ§ЁПгУЯЁЫсНЋCO32ЃзЊЛЏЮЊCO2ЃЌВтЖЈCO2ЕФжЪСПЁЃ
НтД№1-4аЁЬтЃК
1ЃЎЗНАИвЛЕФВйзїВНжшгаЃКЂйГЦСПВЂШмНтбљЦЗЃЛЂкМгШызуСПЕФBaCl2ШмвКЃЛЂлЙ§ТЫЃЛЂмЯДЕгЃЛЂнИЩдяЃЛЂоГЦСПВЂНјааКужиВйзїЁЃГЦСПЪБЫљашЖЈСПЪЕбщвЧЦїЮЊ____________________ЁЃХаЖЯЪЧЗёДяЕНКужиЕФБъзМЪЧ_____________________________________________________ЁЃ
2ЃЎЗНАИЖўЕФОпЬхЙ§ГЬЮЊЃК
ЂйВйзї1ЫљашвЊЕФвЧЦїга_____________________________________________ЁЃ
ЂкЕЮЖЈЪБбЁдёЕФжИЪОМСЮЊМзЛљГШЁЃЕБШмвК____________________________________ЪБЃЌЫЕУїДяЕНСЫЕЮЖЈжеЕуЁЃ
ЂлЮЊМѕЩйХМШЛЮѓВюЃЌЭЈГЃЕФДІРэАьЗЈЪЧ_______________________________ЁЃ
ЂмЕЮЖЈЪБШєзЖаЮЦПФкгаЩйСПвКЬхНІГіЃЌдђВтЖЈНсЙћ_________ЁЃЃЈбЁЬюЁАЦЋИпЁБЁЂЁАЦЋЕЭЁБЁЂЁАВЛгАЯьЁБЃЌЯТЭЌЃЉЃЌШєЪЂзАЮДжЊвКЕФзЖаЮЦПгУеєСѓЫЎЯДЙ§ЃЌЮДгУЮДжЊвКШѓЯДЃЌВтЖЈНсЙћ_________ЁЃ
3ЃЎЗНАИШ§ЕФЪЕбщзАжУШчЯТЭМЃК

ВйзїВНжшгаЃКЂйМьВщзАжУЕФЦјУмадЃЛЂкдкИЩдяЙмФкзАТњМюЪЏЛвЃЌГЦСПжЪСПЮЊW1 gЃЛЂлГЦСПW2 gбљЦЗзАШыЙуПкЦПBжаЃЛЂмЙиБежЙЫЎМаЃЛЂнЛКТ§МгШыЯЁH2SO4жСВЛдйВњЩњЦјЬхЮЊжЙЃЛЂо ДђПЊжЙЫЎМаЃЛЂпЛКЛКЙФШыПеЦјЪ§ЗжжгЃЌдйГЦСПИЩдяЙмЃЌжЪСПЮЊW3 gЁЃ
ИУЗНАИбљЦЗжаДПМюЕФжЪСПЗжЪ§ЮЊ__________________________ЃЈгУДњЪ§ЪНБэЪОЃЉЁЃ
ЩЯЭМжазАжУAЕФзїгУЪЧ_____________________ЁЃзАжУCЕФзїгУЪЧ_____________________ЁЃгаЭЌбЇШЯЮЊПеЦјжаЕФЫЎеєЦјЛсНјШыИЩдяЙмЕМжТВтСПНсЙћ_____________(ЬюЁАЦЋДѓЁБЁЂЁАЦЋаЁЁБЛђЁАЮогАЯьЁБЃЉЁЃИФНјДыЪЉПЩвдЪЧ______________________________________________ЁЃ
4ЃЎШєгУЯТЭМзАжУЖдбљЦЗНјааЗжЮіЃЌИљОнСПЦПжаЪеМЏЕНЕФвКЬхЕФЬхЛ§РДМЦЫубљЦЗжаЬМЫсФЦЕФКЌСПЁЃдђЯТСазАжУжаЃЌзюКЯРэЕФЪЧ______ЁЃЃЈбЁЬюађКХЃЉ
A B
C D
ЃЈ18ЗжЃЉЙЄвЕЩњВњЕФДПМюжаГЃКЌгаЩйСПNaClдгжЪЁЃЮЊВтЖЈФГДПМюбљЦЗЕФДПЖШЃЌЛЏбЇПЮЭтЛюЖЏаЁзщЩшМЦСЫШ§жжЪЕбщЗНАИЃК
ЁОЗНАИвЛЁПШЁбљЦЗШмНтКѓЃЌМгЪдМСЪЙCO32ЃГСЕэЃЌВтЖЈГСЕэЕФжЪСПЁЃ
ЁОЗНАИЖўЁПгУ0.100 mol/LбЮЫсЕЮЖЈЁЃ
ЁОЗНАИШ§ЁПгУЯЁЫсНЋCO32ЃзЊЛЏЮЊCO2ЃЌВтЖЈCO2ЕФжЪСПЁЃ
НтД№1-4аЁЬтЃК
1ЃЎЗНАИвЛЕФВйзїВНжшгаЃКЂйГЦСПВЂШмНтбљЦЗЃЛЂкМгШызуСПЕФBaCl2ШмвКЃЛЂлЙ§ТЫЃЛЂмЯДЕгЃЛЂнИЩдяЃЛЂоГЦСПВЂНјааКужиВйзїЁЃГЦСПЪБЫљашЖЈСПЪЕбщвЧЦїЮЊ____________________ЁЃХаЖЯЪЧЗёДяЕНКужиЕФБъзМЪЧ_____________________________________________________ЁЃ
2ЃЎЗНАИЖўЕФОпЬхЙ§ГЬЮЊЃК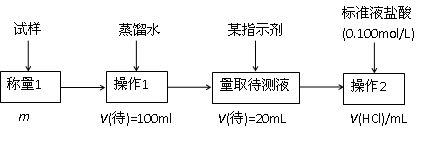
ЂйВйзї1ЫљашвЊЕФвЧЦїга_____________________________________________ЁЃ
ЂкЕЮЖЈЪБбЁдёЕФжИЪОМСЮЊМзЛљГШЁЃЕБШмвК____________________________________ЪБЃЌЫЕУїДяЕНСЫЕЮЖЈжеЕуЁЃ
ЂлЮЊМѕЩйХМШЛЮѓВюЃЌЭЈГЃЕФДІРэАьЗЈЪЧ_______________________________ЁЃ
ЂмЕЮЖЈЪБШєзЖаЮЦПФкгаЩйСПвКЬхНІГіЃЌдђВтЖЈНсЙћ_________ЁЃЃЈбЁЬюЁАЦЋИпЁБЁЂЁАЦЋЕЭЁБЁЂЁАВЛгАЯьЁБЃЌЯТЭЌЃЉЃЌШєЪЂзАЮДжЊвКЕФзЖаЮЦПгУеєСѓЫЎЯДЙ§ЃЌЮДгУЮДжЊвКШѓЯДЃЌВтЖЈНсЙћ_________ЁЃ
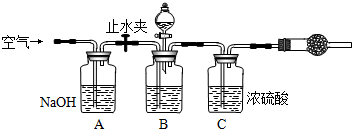
3ЃЎЗНАИШ§ЕФЪЕбщзАжУШчЯТЭМЃК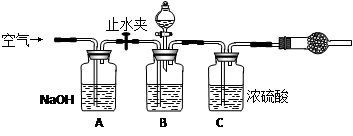
ВйзїВНжшгаЃКЂйМьВщзАжУЕФЦјУмадЃЛЂкдкИЩдяЙмФкзАТњМюЪЏЛвЃЌГЦСПжЪСПЮЊW1 gЃЛЂлГЦСПW2 gбљЦЗзАШыЙуПкЦПBжаЃЛЂмЙиБежЙЫЎМаЃЛЂнЛКТ§МгШыЯЁH2SO4жСВЛдйВњЩњЦјЬхЮЊжЙЃЛЂо ДђПЊжЙЫЎМаЃЛЂпЛКЛКЙФШыПеЦјЪ§ЗжжгЃЌдйГЦСПИЩдяЙмЃЌжЪСПЮЊW3 gЁЃ
ИУЗНАИбљЦЗжаДПМюЕФжЪСПЗжЪ§ЮЊ__________________________ЃЈгУДњЪ§ЪНБэЪОЃЉЁЃ
ЩЯЭМжазАжУAЕФзїгУЪЧ_____________________ЁЃзАжУCЕФзїгУЪЧ_____________________ЁЃгаЭЌбЇШЯЮЊПеЦјжаЕФЫЎеєЦјЛсНјШыИЩдяЙмЕМжТВтСПНсЙћ_____________(ЬюЁАЦЋДѓЁБЁЂЁАЦЋаЁЁБЛђЁАЮогАЯьЁБЃЉЁЃИФНјДыЪЉПЩвдЪЧ______________________________________________ЁЃ
4ЃЎШєгУЯТЭМзАжУЖдбљЦЗНјааЗжЮіЃЌИљОнСПЦПжаЪеМЏЕНЕФвКЬхЕФЬхЛ§РДМЦЫубљЦЗжаЬМЫсФЦЕФКЌСПЁЃдђЯТСазАжУжаЃЌзюКЯРэЕФЪЧ______ЁЃЃЈбЁЬюађКХЃЉ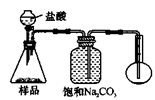
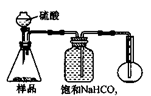
A B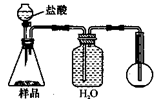
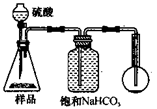
C D
ЃЈ18ЗжЃЉЙЄвЕЩњВњЕФДПМюжаГЃКЌгаЩйСПNaClдгжЪЁЃЮЊВтЖЈФГДПМюбљЦЗЕФДПЖШЃЌЛЏбЇПЮЭтЛюЖЏаЁзщЩшМЦСЫШ§жжЪЕбщЗНАИЃК
ЁОЗНАИвЛЁПШЁбљЦЗШмНтКѓЃЌМгЪдМСЪЙCO32ЃГСЕэЃЌВтЖЈГСЕэЕФжЪСПЁЃ
ЁОЗНАИЖўЁПгУ0.100 mol/LбЮЫсЕЮЖЈЁЃ
ЁОЗНАИШ§ЁПгУЯЁЫсНЋCO32ЃзЊЛЏЮЊCO2ЃЌВтЖЈCO2ЕФжЪСПЁЃ
НтД№1-4аЁЬтЃК
1ЃЎЗНАИвЛЕФВйзїВНжшгаЃКЂйГЦСПВЂШмНтбљЦЗЃЛЂкМгШызуСПЕФBaCl2ШмвКЃЛЂлЙ§ТЫЃЛЂмЯДЕгЃЛЂнИЩдяЃЛЂоГЦСПВЂНјааКужиВйзїЁЃГЦСПЪБЫљашЖЈСПЪЕбщвЧЦїЮЊ____________________ЁЃХаЖЯЪЧЗёДяЕНКужиЕФБъзМЪЧ_____________________________________________________ЁЃ
2ЃЎЗНАИЖўЕФОпЬхЙ§ГЬЮЊЃК

ЂйВйзї1ЫљашвЊЕФвЧЦїга_____________________________________________ЁЃ
ЂкЕЮЖЈЪБбЁдёЕФжИЪОМСЮЊМзЛљГШЁЃЕБШмвК____________________________________ЪБЃЌЫЕУїДяЕНСЫЕЮЖЈжеЕуЁЃ
ЂлЮЊМѕЩйХМШЛЮѓВюЃЌЭЈГЃЕФДІРэАьЗЈЪЧ_______________________________ЁЃ
ЂмЕЮЖЈЪБШєзЖаЮЦПФкгаЩйСПвКЬхНІГіЃЌдђВтЖЈНсЙћ_________ЁЃЃЈбЁЬюЁАЦЋИпЁБЁЂЁАЦЋЕЭЁБЁЂЁАВЛгАЯьЁБЃЌЯТЭЌЃЉЃЌШєЪЂзАЮДжЊвКЕФзЖаЮЦПгУеєСѓЫЎЯДЙ§ЃЌЮДгУЮДжЊвКШѓЯДЃЌВтЖЈНсЙћ_________ЁЃ
3ЃЎЗНАИШ§ЕФЪЕбщзАжУШчЯТЭМЃК

ВйзїВНжшгаЃКЂйМьВщзАжУЕФЦјУмадЃЛЂкдкИЩдяЙмФкзАТњМюЪЏЛвЃЌГЦСПжЪСПЮЊW1 gЃЛЂлГЦСПW2 gбљЦЗзАШыЙуПкЦПBжаЃЛЂмЙиБежЙЫЎМаЃЛЂнЛКТ§МгШыЯЁH2SO4жСВЛдйВњЩњЦјЬхЮЊжЙЃЛЂо ДђПЊжЙЫЎМаЃЛЂпЛКЛКЙФШыПеЦјЪ§ЗжжгЃЌдйГЦСПИЩдяЙмЃЌжЪСПЮЊW3 gЁЃ
ИУЗНАИбљЦЗжаДПМюЕФжЪСПЗжЪ§ЮЊ__________________________ЃЈгУДњЪ§ЪНБэЪОЃЉЁЃ
ЩЯЭМжазАжУAЕФзїгУЪЧ_____________________ЁЃзАжУCЕФзїгУЪЧ_____________________ЁЃгаЭЌбЇШЯЮЊПеЦјжаЕФЫЎеєЦјЛсНјШыИЩдяЙмЕМжТВтСПНсЙћ_____________(ЬюЁАЦЋДѓЁБЁЂЁАЦЋаЁЁБЛђЁАЮогАЯьЁБЃЉЁЃИФНјДыЪЉПЩвдЪЧ______________________________________________ЁЃ
4ЃЎШєгУЯТЭМзАжУЖдбљЦЗНјааЗжЮіЃЌИљОнСПЦПжаЪеМЏЕНЕФвКЬхЕФЬхЛ§РДМЦЫубљЦЗжаЬМЫсФЦЕФКЌСПЁЃдђЯТСазАжУжаЃЌзюКЯРэЕФЪЧ______ЁЃЃЈбЁЬюађКХЃЉ


A B


C D
ЦРЗжЫЕУїЃК
1ЃЎЪдЬтЕФВЮПМНтД№ЪЧгУРДЫЕУїЦРЗжБъзМЕФЃЌПМЩњШчгУЦфЫћЗНЗЈНтД№е§ШЗЕФЃЌЭЌбљИјЗжЃЛгаДэЕФЃЌИљОнДэЮѓЕФЧщПіЃЌВЮееЦРЗжБъзМжаЯргІЕФЙцЖЈЦРЗжЁЃ
2ЃЎЮяРэМЦЫуЬтжЛгазюКѓД№АИЖјЮобнЫуЙ§ГЬЕФЃЌВЛИјЗжЃЛжЛаДГівЛАуЙЋЪНЃЌЕЋЮДФмгыЪдЬтЫљИјЕФОпЬхЬѕСЊЯЕЕФЃЌВЛИјЗжЁЃ
3ЃЎЛЏбЇЗНГЬЪНЁЂРызгЗНГЬЪНЮДХфЦНЕФЃЌЖМВЛИјЗжЁЃ
ЕкIОэ
ЕкIОэЙВ18аЁЬтЃЌУПаЁЬт6ЗжЃЌЙВ108ЗжЁЃ
вЛЁЂбЁдёЬтЃКбЁЖдЕФЕУ6ЗжЃЌбЁДэЛђЮДбЁЕФЕУ0ЗжЁЃ
1ЃЎC 2ЃЎB 3ЃЎA 4ЃЎC 5ЃЎD 6ЃЎD 7ЃЎD 8ЃЎB 9ЃЎA
10ЃЎC 11ЃЎC 12ЃЎB
ЖўЁЂбЁдёЬтЃКШЋВПбЁЖдЕФЕУ6ЗжЃЌбЁЖдЕЋВЛШЋЕФЕУ3ЗжЃЌгабЁДэЛђЮДбЁЕФЕУ0ЗжЁЃ
13ЃЎA 14ЃЎB 15ЃЎC 16ЃЎAC 17ЃЎB 18ЃЎAD
ЕкЂђОэ
ЕкЂђОэБиПМВПЗжЙВ9ЬтЃЌЙВ157ЗжЁЃ
19ЃЎЃЈ18ЗжЃЉ
ЃЈ1ЃЉЂй BDE
ЂкЬНОПЛЌЖЏФІВССІгые§бЙСІЕФЙиЯЕЛђВтЖЈЖЏФІВСвђЪ§ЃЛ
ЬНОПЮяЬхдЫЖЏЫйЖШЫцдЫЖЏЪБМфБфЛЏЙцТЩЛђбаОПдШБфЫйдЫЖЏЙцТЩЃЛ
 ЬНОПЮяРэЕФМгЫйЖШгыСІЁЂжЪСПЕФЙиЯЕЕШЁЃ
ЬНОПЮяРэЕФМгЫйЖШгыСІЁЂжЪСПЕФЙиЯЕЕШЁЃ
ЃЈ2ЃЉЂйЭМЯпШчгвЭМЫљЪО
 ОљПЩЃЉ
ОљПЩЃЉ
ЂкЕчТЗЭМбЁC
ЕчСїБэбЁ
БфзшЦїбЁ
20ЃЎЃЈ15ЗжЃЉ
НтЃКЃЈ1ЃЉШЫДг ЕуХмЕН
ЕуХмЕН ЕуЫљгУЪБМфЮЊЃК
ЕуЫљгУЪБМфЮЊЃК

ЦћГЕДгAжСBЃЌгаЃК

ДњШыЪ§ОнНтЕУЃК

21ЃЎЃЈ19ЗжЃЉ
НтЃКЃЈ1ЃЉдЫЖЏдБРыПЊЦНЬЈКѓДгAжСBдкЪњжБЗНЯђгаЃК
 Ђй
Ђй
дкBЕугаЃК
 Ђк
Ђк
гЩЂйЂкЕУЃК
 Ђл
Ђл
ЃЈ2ЃЉдЫЖЏдБДгAжСCЙ§ГЬгаЃК
 Ђм
Ђм
дЫЖЏдБДгCжСDЙ§ГЬгаЃК
 Ђн
Ђн
гЩЂлЂмЂнНтЕУЃК

ЦфЫће§ШЗНтЗЈЭЌбљИјЗж
22ЃЎЃЈ20ЗжЃЉ
НтЃКЃЈ1ЃЉЕБЦНааН№ЪєАх ЁЂ
ЁЂ МфВЛМгЕчбЙЪБЃЌЩшСЃзгвдЫйЖШ
МфВЛМгЕчбЙЪБЃЌЩшСЃзгвдЫйЖШ НјШыДХГЁКѓзідШЫйдВжмдЫЖЏЕНДя
НјШыДХГЁКѓзідШЫйдВжмдЫЖЏЕНДя ЕуЃЌЙьМЃАыОЖЮЊ
ЕуЃЌЙьМЃАыОЖЮЊ ЃЌга
ЃЌга
гЩХЃЖйЕкЖўЖЈТЩЕУ

гЩЖЏФмЖЈРэга 
ЕУЃКДјЕчСЃзгЕФБШКЩ
ЃЈ2ЃЉЩшНјШыДХГЁЪБСЃзгЫйЖШЮЊ ЃЌЫќЕФЗНЯђгы
ЃЌЫќЕФЗНЯђгы ЕФМаНЧЮЊ
ЕФМаНЧЮЊ ЃЌЦфЩфШыДХГЁЪБЕФШыЩфЕуКЭДђЕНИаЙтЦЌЩЯЕФЮЛжУжЎМфЕФОрРы
ЃЌЦфЩфШыДХГЁЪБЕФШыЩфЕуКЭДђЕНИаЙтЦЌЩЯЕФЮЛжУжЎМфЕФОрРы ЃЌгаЃК
ЃЌгаЃК



гЩМИКЮЙиЯЕЕУЃК
МД гы
гы ЮоЙиЃЌЮЊЖЈжЕЁЃ
ЮоЙиЃЌЮЊЖЈжЕЁЃ
дђДјЕчСЃзгдкЦНааН№ЪєАх ЁЂ
ЁЂ МфЕФзюДѓЦЋвЦСП
МфЕФзюДѓЦЋвЦСП
 ЃЌ ЖдгІЕФЦЋзЊЕчбЙ
ЃЌ ЖдгІЕФЦЋзЊЕчбЙ
гЩЙІФмЙиЯЕПЩжЊЦЋвЦСПзюДѓЕФДјЕчСЃзгРыПЊЦНааН№ЪєАх ЁЂ
ЁЂ ЪБгазюДѓЖЏФм
ЪБгазюДѓЖЏФм ЃЌ
ЃЌ
гЩЖЏФмЖЈРэ

НтЕУ

ЭЌРэЃЌ ЪБПЬНјШыЦНааН№ЪєАх
ЪБПЬНјШыЦНааН№ЪєАх ЁЂ
ЁЂ МфЕФДјЕчСЃзгРыПЊЦНааН№ЪєАхЪБгазюаЁЖЏФм
МфЕФДјЕчСЃзгРыПЊЦНааН№ЪєАхЪБгазюаЁЖЏФм ЃЌдђЃК
ЃЌдђЃК

ЙЪЃК 
23ЃЎЃЈ15ЗжЃЉ
ЃЈ1ЃЉ
ЃЈ2ЃЉ ЃЈЛђ
ЃЈЛђ
ЃЈ3ЃЉ ЃЈШлШкЃЉ
ЃЈШлШкЃЉ

ЃЈ4ЃЉ 3
3
ЃЈ5ЃЉ ЃЈ1ЃЉ+
ЃЈ1ЃЉ+


24ЃЎЃЈ15ЗжЃЉ
ЃЈ1ЃЉ
ЃЈ2ЃЉШЗБЃЬМЫсЧтФЦЭъШЋЗжНтЃЌМѕЩйВтЖЈЮѓВюЃЈЛђЦфЫћКЯРэД№АИЃЉ
ЃЈ3ЃЉЯДЕг
ЃЈ4ЃЉ ЃЈЛђЦфЫћКЯРэД№АИЃЉ
ЃЈЛђЦфЫћКЯРэД№АИЃЉ
ЃЈ5ЃЉЦЋИп
ЃЈ6ЃЉХЈСђЫс
ЃЈ7ЃЉНЋBЁЂCзАжУжаЕФ ШЋВПЧ§ШыDзАжУЕФМюЪЏЛвжаЃЌМѕаЁЪЕбщЮѓВю
ШЋВПЧ§ШыDзАжУЕФМюЪЏЛвжаЃЌМѕаЁЪЕбщЮѓВю
25ЃЎЃЈ15ЗжЃЉ
ЃЈ1ЃЉМѕаЁЃЛ0.0003
ЃЈ2ЃЉ
ЃЈ3ЃЉЂй ЃЛ Ђк
ЃЛ Ђк ЃЛЂлдіДѓЃЛВЛБф
ЃЛЂлдіДѓЃЛВЛБф
26ЃЎЃЈ25ЗжЃЉ
IЃЎЃЈ15ЗжЃЉ
ЃЈ1ЃЉ ЃЈОЦОЋЃЉ+
ЃЈОЦОЋЃЉ+ +ЩйСПФмСП
+ЩйСПФмСП
ЃЈ2ЃЉЭбТфЫс
ЃЈ3ЃЉУИЕФЛюад ЯИАћКєЮќЪЭЗХЕФВПЗжФмСПзЊЛЏЮЊШШФм
ЃЈ4ЃЉдіЖр
ЃЈ5ЃЉЙтКЯзїгУЧПЖШДѓгкКєЮќзїгУЧПЖШ
ЙтееЧПЖШЁЂЙтееЪБМфЁЂЮТЖШЁЂ ХЈЖШЁЂЫЎЗЪЙмРэЁЂВЁГцКІЁЂдгВнЕШЃЈД№Гі2ЯюМДПЩЃЉ
ХЈЖШЁЂЫЎЗЪЙмРэЁЂВЁГцКІЁЂдгВнЕШЃЈД№Гі2ЯюМДПЩЃЉ
ЂђЃЎЃЈ10ЗжЃЉ
ЃЈ1ЃЉШЁбљЦїШЁбљ
ЃЈ2ЃЉШКТф
ОКељЁЂМФЩњЁЂВЖЪГЁЂЛЅРћЙВЩњ
ЃЈ3ЃЉМфНг
ЃЈ4ЃЉИКЗДРЁЕїНк
27ЃЎЃЈ15ЗжЃЉ
ЃЈ1ЃЉXЁЂЂђЁЂЂѓЁЂЂєЛђYЁЂЂђЁЂЂѓЁЂЂє ЃЈД№ШЋЕУ3ЗжЃЌВЛШЋВЛЕУЗжЁЃЁАЛђЁБВЛФмаДГЩЁАКЭЁБЃЉ
ЃЈ2ЃЉ Лђ
Лђ ЗжРы
ЗжРы
ЃЈ3ЃЉ ЁЂ
ЁЂ Жў
Жў
ЕкЂђОэбЁПМВПЗжЙВ5ЬтЃЌЙВ35ЗжЁЃЦфжаЃЌЕк28ЁЂ29ЬтЮЊЮяРэЬтЃЌЕк30ЁЂ31ЬтЮЊЛЏбЇЬтЃЌПМЩњДгСНЕРЮяРэЬтЁЂСНЕРЛЏбЇЬтжаИїШЮбЁвЛЬтзїД№ЃЌШєЕк28ЁЂ29ЬтЖМзїД№ЃЌдђАДЕк28ЬтМЦЗжЃЌШєЕк30ЁЂ31ЬтЖМзїД№ЃЌдђАДЕк30ЬтМЦЗжЃЛЕк32ЬтЮЊЩњЮяЬтЃЌЪЧБиД№ЬтЁЃ
28ЃЎЃЈ12ЗжЃЉ
ЃЈ1ЃЉЂм ЃЈ2ЃЉЂк
29ЃЎЃЈ12ЗжЃЉ
ЃЈ1ЃЉЂк ЃЈ2ЃЉЂй
30ЃЎЃЈ13ЗжЃЉ
ЃЈ1ЃЉ3
ЃЈ2ЃЉC
ЃЈ3ЃЉЂй РызгМќЃЛЧтМќ
Ђк
ЃЈ4ЃЉ ЕФ
ЕФ
 Дѓгк
Дѓгк ЕФ
ЕФ ЃЌЫљвд
ЃЌЫљвд дйЪЇШЅвЛИіЕчзгБШ
дйЪЇШЅвЛИіЕчзгБШ ИќФбЃЌдвђЪЧ
ИќФбЃЌдвђЪЧ ЪєгкНЯЮШЖЈЕФАыГфТњНсЙЙЁЃ
ЪєгкНЯЮШЖЈЕФАыГфТњНсЙЙЁЃ
31ЃЎЃЈ13ЗжЃЉ
ЃЈ1ЃЉ
ЃЈ2ЃЉCD
ЃЈ3ЃЉ2ЃК2
ЃЈ4ЃЉ
ЃЈ5ЃЉ
32ЃЎЃЈ10ЗжЃЉ
ЃЈ1ЃЉЙЙМўЛљвђБэДядиЬх
ХЉИЫОњзЊЛЏЗЈЁЂЛљвђЧЙЗЈЁЂЛЈЗлЙмЭЈЕРЗЈ
ПЙдЃПЙЬхдгНЛ
ЃЈ2ЃЉжВЮязщжЏХрбј
жВЮяЯИАћЕФШЋФмад
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com