
题目列表(包括答案和解析)
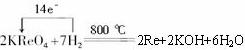
(1)根据你的理解,请说明铼元素的发现为什么会如此艰难?__________________________。
(2)铼有两种天然同位素:稳定同位素185Re和放射性同位素187Re,两种同位素原子中的中子数之和是________________。
(3)写出现代工业上用氢气还原金属铼的化学反应方程式,并标出电子转移的方向和数目____________________________________________________________________。
铼(Re)是自然界中最后一种被诺达克等三位科学家于1926年发现的元素.他们从数以吨计的含有多种元素的矿石中,通过复杂的工艺一点一滴地富集浓缩,才制得了仅2毫克的金属铼.现工业采用的方法是:在氢气流中于800℃的高温下,使高铼酸钾中的铼元素全部被还原出来.
(1)根据你的理解,请说明铼元素的发现为什么会如此艰难?_____________.
(2)铼有两种天然同位素:稳定同位素185Re和放射性同位素187Re,两种同位素原子中的中子数之和是_____________.
(3)写出现代工业上用氢气还原金属铼的化学反应方程式,并标出电子转移的方向和数目________________.
铼
(Re)是自然界中最后一种被诺达克等三位科学家于1926年发现的元素.他们从数以吨计的含有多种元素的矿石中,通过复杂的工艺一点一滴地富集浓缩,才制得了仅2毫克的金属铼.现工业采用的方法是:在氢气流中于800℃的高温下,使高铼酸钾中的铼元素全部被还原出来.
(1)根据你的理解,请说明铼元素的发现为什么会如此艰难?时间上为什么如此漫长?
(2)铼有两种天然同位素:稳定同位素185Re和放射性同位素187Re,两种同位素原子中的中子数之和是________.
(3)写出现代工业上用氢气还原金属铼的化学反应方程式,并标出电子转移的方向和数目________.
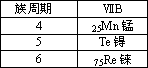
族 周期 | ⅦB |
四 | 25Mn锰 |
五 | 43Te 锝 |
六 | 75Re铼 |
(1)根据你的理解,请说明铼元素的发现为什么如此艰难?时间上会如此漫长?
(2)铼有两种天然同位素。稳定同位素185Re和放射性同位素187Re两种同位素原子中的中子数之和是__________。
(3)写出现代工业上用氢气还原制备金属铼的化学方程式,并标出电子转移的方向和数目__________。
元素代号 | A | B | C | D | E |
原子半径/nm | 0.16 | 0.143 | 0.102 | 0.089 | 0.074 |
主要化合价 | +2 | +3 | +6,-2 | +2 | -2 |
(1)用元素代号标出它们在周期表中对应位置

(2)C、E形成化合物为______________(填化学式),周期表有些元素存在“对角线相似”现象,请写出D的单质与强碱溶液反应的离子方程式:______________________;并用电子式表示其氯化物的形成过程____________________________________________________________。
(3)有一类无机化合反应的通式可以表示为:单质+化合物(1)=化合物(2)。请写出满足以下要
求的4个此类无机化合反应的化学方程式:
①所涉及的元素的原子序数都小于30,②4种单质分属4个不同族。
_______________________________________,_______________________________________,
_______________________________________,_______________________________________。
(4)M为金属元素铼(Re),铼是自然界中最后一种被诺达克等三位科学家于1926年发现的元素。他们从数以吨计的含有多种元素的矿石中,通过复杂的工艺一点一滴地富集浓缩,才制得了仅2mg的金属铼。现代工业上采用的方法是:于
①元素铼的原子序数为_____________,铼元素发现如此艰难和时间上如此漫长的原因:
____________________________________________________________________。
②写出现代工业上用氢气冶炼金属铼的化学方程式,并标出电子转移的方向和数目:_____________________________________________________________________。
一、选择题(本题包括18小题,每小题2分,共36分)
1
2
3
4
5
6
7
8
9
B
D
B
B
A
D
B
C
A
10
11
12
13
14
15
16
17
18
D
A
C
B
A
D
D
B
C
二、填空题(本题包括6小题,共64分)
(2)
(3) ①如2Na+2H2O = 2Na++2OH-+H2↑;
②如H++NH3×H2O = NH4++H2O;
③如Al3++3H2O Al(OH)3+3H+;
Al(OH)3+3H+;
20.(10分)(1)铼元素在自然界的存在分散,矿石中含量低,难于富集;铼元素与其他元素共存,难以分离(4分)(2)222(2分)
21.(8分)(1)吸热(2)1/9,1/7(3)2NO+O2+4CO = 4CO2+N2
22.(16分)(每空2分)(1)Al(OH)3+OH-=AlO2-+2H2O (2)
(3)①酸 ② Al3++3H2O Al(OH)3+3H+
Al(OH)3+3H+
(4)SO2+Cl2+2H2O=H2SO4+2HCl (5)HCl>H2S
(6)S2->Cl->Na+>Al3+ (7)Cl2O7(l)+H2O(l)=2HClO4(aq) △H= -4QkJ/mol
23.(12分)步骤一:(1)①正 (1分);②Cu2++2e = Cu (2分);(2)变小(1分)
步骤二:(一)①3Ag + 4H+ + NO3― = 3Ag+ + NO↑+ 2H2O(2分);
②浓盐酸含有大量氯离子,Au3+ 离子与氯离子形成稳定的AuCl4―离子,使反应2平衡向右移动,则金溶于王水中。(2分)(二)①0.5 (2分);②0.1(2分)
24.(8分)(每空2分)(1) 10Ca(OH)2+10Cl2=2Ca(C1O)2+Ca(C1O3)2+7CaCl2+10H2O
(2) 5 (3)Ⅰ < ; Ⅱ 
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com