某化学兴趣小组,在学习碱的化学性质时,进行了如图所示的实验.

(1)A实验能证明盐酸和氢氧化钠发生反应,其理由是______.
(2)B实验用于确认二氧化碳与氢氧化钠能发生化学反应(实验前K
1、K
2均处于关闭状态).请写出实验中K
2处于关闭状态下打开K
1时发生反应的化学反应方程式______;打开K
1后,再打开K
2时观察到的现象______.
(3)实验结束后,同学们将A、B两个实验的废液倒入同一个干净的烧杯中,观察到液体呈红色,由此产生疑问.
【提出问题】烧杯的废液中含有哪些物质?
【交流讨论】一定含有的物质:酚酞、水和______,还含有能使酚酞变红的物质.
【查阅资料】碳酸钠溶液呈碱性,氯化钙溶液呈红色.
【猜想】废液中能使酚酞变红的物质:
A、只有氢氧化钠 B、只有碳酸钠 C、______.
【设计实验】兴趣小组的同学用氯化钙溶液来验证猜想.
【实验验证】取一定量的废液于试管,逐滴加入氯化钙溶液.
【结论解释】通过实验,同学们得出了确切的结论.
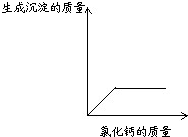
①根据部分实验现象绘制出右图的关系曲线,则猜想中一定不成立的是______(填序号).
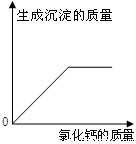
②加入过量氯化钙溶液后发现______则不含氢氧化钠.
【拓展应用】还可以用______代替氯化钙溶液得出正确结论.

 18、某化学兴趣小组,在学习碱的化学性质时,进行了如图所示的实验.
18、某化学兴趣小组,在学习碱的化学性质时,进行了如图所示的实验.




