TiO
2Φ» «÷Τ±ΗΤδΥϊΚ§ν―Μ·ΚœΈοΒΡ‘≠ΝœΘ§”÷ «“Μ÷÷–‘Ρή”≈“λΒΡΑΉ…Ϊ―’ΝœΘ°
Θ®1Θ© Β―ι “άϊ”ΟΖ¥”ΠTiO
2Θ®sΘ©+CCl
4Θ®gΘ©
TiCl
4Θ®gΘ©+CO
2Θ®gΘ©Θ§‘ΎΈόΥ°Έό―θΧθΦΰœ¬Θ§÷Τ»ΓTiCl
4 Β―ιΉΑ÷Ο Ψ“βΆΦ»γœ¬
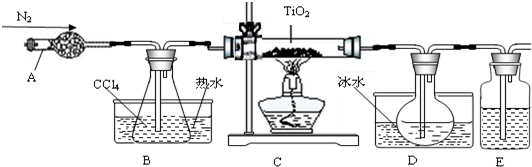
”–ΙΊ–‘÷ »γœ¬±μ
| Έο÷ |
»έΒψ/Γφ |
Ζ–Βψ/Γφ |
ΤδΥϊ |
| CCl4 |
-23 |
76 |
”κTiCl4ΜΞ»ή |
| TiCl4 |
-25 |
136 |
”ω≥± ΣΩ’Τχ≤ζ…ζΑΉΈμ |
“«ΤςAΒΡΟϊ≥Τ «
Θ§ΉΑ÷ΟE÷–ΒΡ ‘ΦΝ «
Θ°Ζ¥”ΠΩΣ Φ«Α“ά¥ΈΫχ––»γœ¬≤ΌΉςΘΚΉιΉΑ“«ΤςΓΔ
ΓΔΦ”ΉΑ“©ΤΖΓΔΆ®N
2Θ°“ΜΕΈ ±ΦδΚσΒψ»ΦΨΤΨΪΒΤΘ°Ζ¥”ΠΫα χΚσΒΡ≤ΌΉςΑϋά®ΘΚΔΌΆΘ÷ΙΆ®ΒΣΤχΔΎœ®ΟπΨΤΨΪΒΤΔέά以÷Ν “Έ¬Θ°’ΐ»ΖΒΡΥ≥–ρΈΣ
Θ®Χν–ρΚ≈Θ©Θ°”ϊΖ÷άκD÷–ΒΡ“ΚΧ§ΜλΚœΈοΘ§Υυ≤…”Ο≤ΌΉςΒΡΟϊ≥Τ «
Θ°
Θ®2Θ©ΙΛ“Β…œ”…ν―ΧζΩσΘ®FeTiO
3Θ©Θ®Κ§Fe
2O
3ΓΔSiO
2Β»‘”÷ Θ©÷Τ±ΗTiO
2ΒΡ”–ΙΊΖ¥”ΠΑϋά®ΘΚ
Υα»ή FeTiO
3Θ®sΘ©+2H
2SO
4Θ®aqΘ©®TFeSO
4Θ®aqΘ©+TiOSO
4Θ®aqΘ©+2H
2OΘ®lΘ©
Υ°Ϋβ TiOSO
4Θ®aqΘ©+2H
2OΘ®lΘ©
H
2TiO
3Θ®sΘ©+H
2SO
4Θ®aqΘ©
Φρ“ΣΙΛ“’Νς≥Χ»γœ¬ΘΚ
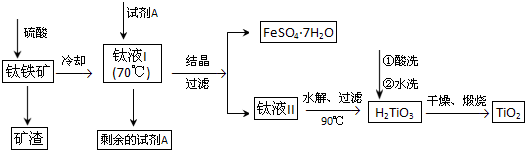
ΔΌ ‘ΦΝAΈΣ
Θ°ν―“ΚΔώ–ηά以÷Ν70ΓφΉσ”“Θ§»τΈ¬Ε»ΙΐΗΏΜαΒΦ÷¬≤ζΤΖ ’¬ ΫΒΒΆΘ§‘≠“ρ «
ΔΎ»Γ…ΌΝΩΥαœ¥ΚσΒΡH
2TiO
3Θ§Φ”»κ―ΈΥα≤Δ’ώΒ¥Θ§ΒΈΦ”KSCN»ή“ΚΚσΈόΟςœ‘œ÷œσΘ§‘ΌΦ”H
2O
2Κσ≥ωœ÷ΈΔΚλ…ΪΘ§ΥΒΟςH
2TiO
3÷–¥φ‘ΎΒΡ‘”÷ άκΉ” «
Θ°’β÷÷H
2TiO
3Φ¥ Ι”ΟΥ°≥δΖ÷œ¥Β”Θ§λ―…’ΚσΜώΒΟΒΡTiO
2“≤ΜαΖΔΜΤΘ§ΖΔΜΤΒΡ‘”÷ «
Θ®ΧνΜ·―ß ΫΘ©Θ°



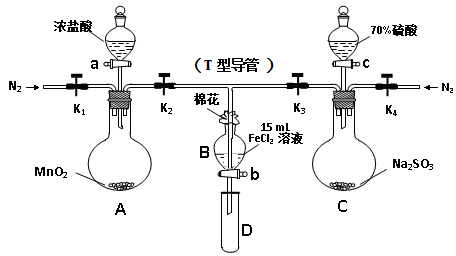
 FeSO3(s)Θ®ΡΪ¬Χ…ΪΘ©Χα≥ωΦΌ…ηΘΚFeCl3”κ SO2ΒΡΖ¥”ΠΨ≠άζΝΥ÷–Φδ≤ζΈοFeSO3Θ§»ή“ΚΒΡΚλΉΊ…Ϊ «FeSO3Θ®ΡΪ¬Χ…ΪΘ©”κFeCl3Θ®ΜΤ…ΪΘ©ΒΡΜλΚœ…ΪΓΘ
FeSO3(s)Θ®ΡΪ¬Χ…ΪΘ©Χα≥ωΦΌ…ηΘΚFeCl3”κ SO2ΒΡΖ¥”ΠΨ≠άζΝΥ÷–Φδ≤ζΈοFeSO3Θ§»ή“ΚΒΡΚλΉΊ…Ϊ «FeSO3Θ®ΡΪ¬Χ…ΪΘ©”κFeCl3Θ®ΜΤ…ΪΘ©ΒΡΜλΚœ…ΪΓΘ