
题目列表(包括答案和解析)
 B+D在四种不同条件下进行,B、D起始浓度为零.反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表:
B+D在四种不同条件下进行,B、D起始浓度为零.反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表:| 实验序号 | 时间/浓度/温度 | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 1 | 800℃ | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2 | 800℃ | C2 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | 800℃ | C3 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
| 4 | 820℃ | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
| 实验步骤 | 实验现象 | 解释和结论 |
| (1)在小烧杯中加入0.1mol/LFeCl3溶液2mL和0.1mol/LNH4SCN溶液2mL.加水10ml,混匀后分装于3支试管中. | 反应后形成红色溶液. | |
| (2) 往第一支试管加入少量三氯化铁溶液 往第一支试管加入少量三氯化铁溶液 |
试管中溶液 颜色加深 试管中溶液 颜色加深 |
增大反应物浓度促使 化学平衡向正反应的 方向移动 增大反应物浓度促使 化学平衡向正反应的 方向移动 |
| (3) 往第二支试管中加入少量硫氰化钾溶液 往第二支试管中加入少量硫氰化钾溶液 |
试管中溶液 颜色加深 试管中溶液 颜色加深 |
增大反应物浓度促使 化学平衡向正反应的 方向移动 增大反应物浓度促使 化学平衡向正反应的 方向移动 |
| (4)比较上述三支试管的颜色. | 加入铁离子或硫氰根离子都能使溶液 颜色加深 加入铁离子或硫氰根离子都能使溶液 颜色加深 |
增大任何一种反应物 的浓度促使化学平衡向正反应的方向移动 增大任何一种反应物 的浓度促使化学平衡向正反应的方向移动 |
| 实验步骤 | 实验现象 | 解释和结论 |
| (1)在小烧杯中加入0.1mol/LFeCl3溶液2mL和0.1mol/LNH4SCN溶液2mL.加水10ml,混匀后分装于3支试管中. | 反应后形成红色溶液. | |
| (2)______ | ______ | ______ |
| (3)______ | ______ | ______ |
| (4)比较上述三支试管的颜色. | ______ | ______ |
 CoCl42- ; △H>0
CoCl42- ; △H>0 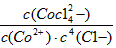
 通过实验测定反应速率的方法有多种,为证明化学反应速率与反应的浓度有关.有同学设计如下实验:
通过实验测定反应速率的方法有多种,为证明化学反应速率与反应的浓度有关.有同学设计如下实验:| 序号 | Na2S2O3溶液 | 稀H2SO4 | 出现混浊时间 | ||
| 浓度 | 用量 | 浓度 | 用量 | ||
| (1) | 0.1mol?L-1 | 10mL | 0.1mol?L-1 | 10mL | t1 |
| (2) | 0.1mol?L-1 | 10mL+5mL 水 | 0.1mol?L-1 | 10mL | t2 |
| (3) | 0.1mol?L-1 | 10mL | 0.1mol?L-1 | 5mL+5mL水 | t3 |
| (4) | 0.1mol?L-1 | 5mL | 0.1mol?L-1 | 5mL | t4 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com