
题目列表(包括答案和解析)
(每空1分,共6分)科学家在研究化学物质时,常常对物质进行分类,以便对同类物质的组成和性能进行![]() 深入的研究。下列各组物质中有一种物质与其它物质不属于同一类,请
深入的研究。下列各组物质中有一种物质与其它物质不属于同一类,请![]() 将其挑出来。
将其挑出来。
| 物质组 | 不属于同类物质 |
| (1)Mg、O2、I2、NO | |
| (2)NaOH、Na2CO3、CH4、CaO | |
| (3)HClO、H2SO4、NH3·H2O、H2SiO3 | |
| ( | |
| (5)Ca(HCO3)2、Na2CO3、AgNO3、BaSO4 | |
| (6)水、液氯、氨水、水银 |
 (每空1分,共9分)纯碱、烧碱等是重要的化工原料。
(每空1分,共9分)纯碱、烧碱等是重要的化工原料。
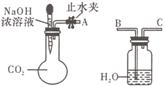
(1)利用如图所示装置可证明二氧化碳与烧碱溶液发生了
反应。将A与B连接,打开止水夹,将胶头滴管中的液体
挤入烧瓶,此时的实验现象是______________________。若其
它操作不变,将A与C连接,可观察到的现象是__________________________________________。
![]() (2)向100mL 2mol/L的NaOH溶液中通入一定量的CO2,结晶,得到9.3g白色固体,该白色固体
(2)向100mL 2mol/L的NaOH溶液中通入一定量的CO2,结晶,得到9.3g白色固体,该白色固体![]() 的组成是_______(写化学式)。设计实验确认该白色固体中存在的阴离子,试完成下列方案:
的组成是_______(写化学式)。设计实验确认该白色固体中存在的阴离子,试完成下列方案:
| 实验操作 | 实验现象 | 结 论 |
| ①取少量白色固体于试管中,加水溶解,再加足量BaCl2溶液 | ||
| ②过滤,取2mL滤液于试管中,滴加酚酞 | 溶液变红 |
(3)现代工业常以氯化钠为原料制备纯碱,部分工艺流程如下:
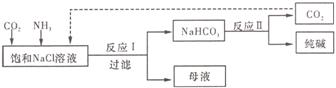
![]() 已知NaHCO3在低温
已知NaHCO3在低温![]() 下溶解度较小。反应Ⅰ为:NaCl+CO2+NH3+H2O
下溶解度较小。反应Ⅰ为:NaCl+CO2+NH3+H2O
NaHCO3↓+NH4Cl,处理母液的两种方法如下:
①向母液中加入石灰乳,可将其中______循环利用,同时得到融雪剂_____。
②向![]() 母液中通入NH3,加入细小食盐颗粒并降温,可得到NH4Cl晶体。
母液中通入NH3,加入细小食盐颗粒并降温,可得到NH4Cl晶体。
试写出通入NH3后,溶解度较小的酸碳酸盐转变为溶解度较大的碳酸盐的离子方程式_________________________________。
(每空1分,共7分)下表为元素周期表的一部分,请回答有关问题:
|
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 |
|
|
|
| ① |
| ② |
|
| 3 |
| ③ | ④ | ⑤ |
| ⑥ | ⑦ | ⑧ |
| 4 | ⑨ |
|
|
|
|
| ⑩ |
|
(1)⑤和⑧的元素符号是_________和__________;
(2)表中最活泼的金属是_________,非金属性最强的元素是_________;(填写元素符号)
(3)表中能形成两性氢氧化物的元素是______,分别写出该元素的氢氧化物与⑥、⑨
的最高价氧化物对应水化物反应的化学方程式__________________________________;
__________________________________.
(每空1分,共8分)
由丙烯经下列反应可得到F和高分子化合物G,它们都是常用的塑料
请回答下列问题:
(1)F的同分异构体有很多,其中属于芳香烃(除去F自身外)有 种,化合物E的官能团的名称: 、 。
(2)写出下列反应过程的反应类型:A→B: 、E→G 。
(3)写出B→C反应的化学方程式为 。
(4)若A在NaOH的醇溶液反应,生成物仍为卤代烃,且其结构存在顺反异构,那么,A所发生的反应的化学方程式为 。
(5)E的一种同分异构体M具有如下性质:①能发生银镜反应;②1mol M与足量的金属钠反应可产生1mol H2,则M的结构简式为_________ ____。(注:两个羟基连在同一碳上的结构不稳定)
(每空1分,共7分)溴乙烷是一种重要的有机化工原料,其沸点为38.4℃。制备溴乙烷的一种方法是乙醇与氢溴酸反应,该反应的化学方程式是 。
实际通常是用溴化钠与一定浓度的硫酸和乙醇反应。某课外小组欲在实验室制备溴乙烷的装置如图,实验操怍步骤如下:
①检查装置的气密性;
②在圆底烧瓶中加入95%乙醇、80%硫酸,然后加 入研细的溴化钠粉末和几粒碎瓷片;
③小心加热,使其充分反应。
请问答下列问题。
(1)装置A的作用是 。
(2)反应时若温度过高,则有 生成,同时观察到还有一种红棕色气体产生,该气体物质的电子式是 。
生成,同时观察到还有一种红棕色气体产生,该气体物质的电子式是 。
(3)反应结束后,得到的粗产品呈棕黄色。为了除去粗产品中的杂质,可选择下列试剂中的 (填写上正确选项的字母)。
a.饱和食盐水 b.稀氢氧化钠溶液 c.乙醇 d.四氯化碳
该实验操作中所需的主要玻璃仪器是 (填仪器名称)。
(4)要进一步制得纯净的溴乙烷,可继续用蒸馏水洗涤,分液后,再加入无水![]() ,然后进行的实验操作是 (填写正确选项的字母)。
,然后进行的实验操作是 (填写正确选项的字母)。
a.分液 b.蒸馏 c.萃取
(5)为了检验溴乙烷中含有溴元素,通常采用的方法是取少量溴乙烷,然后 (按实验的操作顺序选填下列序号)。
①加热 ②加入![]() 溶液 ③加入稀
溶液 ③加入稀![]() 酸化 ④加入NaOH溶液
酸化 ④加入NaOH溶液
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com