
题目列表(包括答案和解析)
下列物质中含有共价键的离子化合物是
A.Ba (OH)2 B.CaCl2 C.H2 SO4 D.NH4Cl
下列物质中,既含极性键又含配位键的离子晶体是
A.Ba(OH)2 B.H2SO4 C.(NH4)2SO4 D.CaF2
镍镉(Ni—Cd)充电电池在现代生活中有广泛应用,它的充放电反应按下式进行:
Cd(OH)2+2Ni(OH)2 Cd+2NiO(OH)+2H2O 则,该电池放电时的负极材料是( )。
A.Cd(OH)2 B.Ni(OH)2 C.Cd D.NiO(OH)
氯碱厂电解饱和食盐水溶液制取NaOH的工艺流程示意图如下:
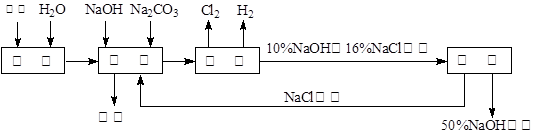
依据上图,完成下列填空:
(1)在电解过程中化学反应方程式为 ,与电源负极相连的电极附近收集到的气体是 。
(2)如果粗盐中SO42—含量较高,必须添加钡试剂除去SO42—,该钡试剂可以是 。
A.Ba(OH)2 B.Ba(NO3)2 C.BaCl2 D.BaSO4
(3)如何除去粗盐中含有的CaCl2、MgCl2及Na2SO4(实际上是指Ca2+、Mg2+及 SO42-),具体操作有: A、过滤 B、加足量的BaCl2溶液 C、加适量的稀盐酸
D、加足量的NaOH溶液 E、加足量的Na2CO3溶液
具体操作的顺序为
(4)脱盐工序中,通过加热浓缩、冷却、过滤的方法除去NaCl,该方法利用的是NaOH与NaCl这两物质在 上的性质差异。
(5)用隔膜法电解食盐水时,电解槽分隔为阳极区和阴极区,防止Cl2和NaOH反应;若采用无隔膜电解冷的食盐水,Cl2和NaOH充分接触,产物仅是NaClO和H2,相应的化学方程式为 。
下列物质的水溶液能导电,但不属于电解质的化合物是( )
A.Ba(OH)2 B.NH3 C.Cl2 D.HCl
说明:
1. 本答案供阅卷评分使用,试题的参考解答是用来说明评分标准的,考生如按其他方法或步骤解答,正确的同样给分;有错的,根据错误的性质,参照评分标准中相应的规定评分。
2. 化学专用名词中出现错别字、元素符号有错误,都要参照评分标准扣分。
3. 化学方程式、离子方程式未配平的,都不给分。
4. 计算只有最后答案而无演算过程的,不给分。
第Ⅰ卷(选择题,共50分)
一、选择题(本题包括25小题,每小题2分,共50分。每小题只有一个选项符合题意)
1. D 2. B 3. C 4. D 5. B 6. D 7. C 8. A 9. A 10. C 11. C 12. B 13. B 14. A
15. D 16. D 17. B 18. A 19. A 20. C 21. C 22. A 23. B 24. C 25. D
第Ⅱ卷(非选择题,共50分)
二、填空题(本题包括6小题,每空1分,共25分)
26.(4分) > > 10-7 mol?L-1 10-14
27.(6分)2 失去2 3 FeS Fe+Cu2+===Fe2++Cu 2Fe+3Cl2点燃=====2FeCl3
28.(4分)→ ← ← ―
 29.(2分)正 氧化
29.(2分)正 氧化
 30.(5分)(1)Al 3 ⅢA (2)钠
30.(5分)(1)Al 3 ⅢA (2)钠
31.(4分)
三、简答题(本题包括3小题,共15分)
32.(共7分,每空1分)(1)2Al+Fe2O3高温=====2Fe+Al2O3 铝(或Al)
(2)大量气泡 2H2O2MnO2======2H2O+O2↑
(3)红 变深 增大任何一种反应物的浓度,都促使化学平衡向正反应方向移动
33.(共4分,每空1分)酸 Fe3++3H2O Fe(OH)3+3H+
盐酸(或HCl)
Fe(OH)3+3H+
盐酸(或HCl)
抑制Ag+ 的水解,防止溶液变浑浊
34.(共4分)(1)气体颜色加深(1分) 气体颜色变浅(1分) (2)升高温度,化学平衡向吸热反应方向移动;降低温度,平衡向放热反应方向移动(2分)
四、计算题(本题包括2小题,共10分)
 35. 解:HNO3+KOH===KNO3+H2O ……………………………………………(1分)
35. 解:HNO3+KOH===KNO3+H2O ……………………………………………(1分)
c(HNO3)?V[HNO3(aq)]=c(KOH)?V[KOH(aq)] ……………………………(1分)
c(HNO3)===0.5018 mol/L (2分)
答:这种HNO3溶液的物质的量浓度为0.5018 mol/L。
36. 解:合金粉末与过量的NaOH溶液混合,只有Al与NaOH反应。
2Al+2NaOH+2H2O===2NaAlO2+3H2↑ 
2×27 g
3×22.4 L
m(Al)
3.36 L …………………………………(2分)
m(Al)= =2.7 g ……………………………………………(2分)
=2.7 g ……………………………………………(2分)
合金中镁的质量分数w(Mg)=×100 %=32.5 % ………………(2分)
答:合金中镁的质量分数为32.5 % 。

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com