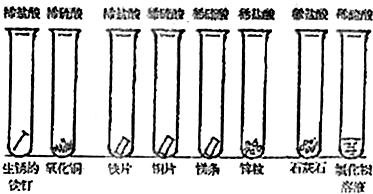
同学们课外探究酸的性质活动中将以下8个实验分为三组进行(如下图所示).

(1)这8个实验是如何分组的?请写出各组的试管编号:第一组
①②
①②
第二组
③④⑤⑥
③④⑤⑥
第三组
⑦⑧
⑦⑧
,你认为如此分组的依据是:
因为本实验的目的是研究强酸(盐酸和硫酸)分别与金属氧化物、金属、盐的反应,所以如此分类.
因为本实验的目的是研究强酸(盐酸和硫酸)分别与金属氧化物、金属、盐的反应,所以如此分类.
.
(2)写出试管②⑤的实验现象及有关的离子方程式:
②
固体溶解,得到蓝色的溶液;
固体溶解,得到蓝色的溶液;
;
CuO+2H+=Cu2++H2O.
CuO+2H+=Cu2++H2O.
.
⑤
镁条溶解,产生大量气体
镁条溶解,产生大量气体
;
Mg+2H+=Mg2++H2↑.
Mg+2H+=Mg2++H2↑.
.
(3)请作为课外活动小组成员,根据实验及现象的分析、比较,归纳出的结论(至少答3条):
①
酸能跟某些金属氧化物反应
酸能跟某些金属氧化物反应
;
②
酸能跟某些盐反应
酸能跟某些盐反应
;
③
酸能跟多种活泼金属反应
酸能跟多种活泼金属反应
.