
题目列表(包括答案和解析)
+ 4 |
3- 4 |
- 3 |
2- 4 |
2- 3 |
- 3 |
- 3 |
2- 3 |
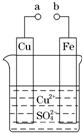 (2011?广东高考)某小组为研究电化学原理,设计如图装置.下列叙述不正确的是( )
(2011?广东高考)某小组为研究电化学原理,设计如图装置.下列叙述不正确的是( )(2007广东) “碘钟”实验中,3I-+S2O82-=I3-+2SO42-的反应速率可以用I3-与加入的淀粉溶液显蓝色的时间t来度量,t越小,反应速率越大。某探究性学习小组在20℃进行实验,得到的数据如下表:
|
实验编号 |
① |
② |
③ |
④ |
⑤ |
|
c(I-)/mol·L- |
0.040 |
0.080 |
0.080 |
0.160 |
0.120 |
|
c(SO42-)/mol·L- |
0.040 |
0.040 |
0.080 |
0.020 |
0.040 |
|
t /s |
88.0 |
44.0 |
22.0 |
44.0 |
t2 |
回答下列问题:
(1)该实验的目的是 。
(2)显色时间t2= 。
(3)温度对该反应的反应速率的影响符合一般规律,若在40℃下进行编号③对应浓度的实验,显色时间t2的范围为 (填字母)
A <22.0s B 22.0~44.0s C >44.0s D 数据不足,无法判断
(4)通过分析比较上表数据,得到的结论是 。
(08广东高考猜想)某溶液中含有HCO3-、SO32-、SiO32-、Cl-等四种离子,若向其中加入某种试剂后,发现溶液中仅有HCO3-、SO32-两种离子数量大量减少。则加入的试剂可能是()
A. 盐酸 B. 过氧化钠 C. 双氧水 D. 氯化钡溶液
(2007广东梅州)(1)肼(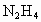 )又称联氨,是一种可燃性的液体,可用作火箭燃料.已知在101kPa时,32.0g
)又称联氨,是一种可燃性的液体,可用作火箭燃料.已知在101kPa时,32.0g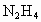 在氧气中完全燃烧生成氮气,放出热量624kJ(25℃时),
在氧气中完全燃烧生成氮气,放出热量624kJ(25℃时),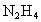 完全燃烧反应的热化学方程式是________.
完全燃烧反应的热化学方程式是________.
(2)肼-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液.肼-空气燃料电池放电时:
正极的电极反应式是________;
负极的电极反应式是________.
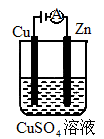
(3)图是一个电化学过程示意图.
①锌片上发生的电极反应是________.
②假设使用肼-空气燃料电池作为本过程中的电源,铜片的质量变化128g,则肼-空气燃料电池理论上消耗标准状况下的空气________L(假设空气中氧气体积含量为20%).
(4)传统制备肼的方法,是以NaClO氧化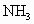 制得肼的稀溶液,该反应的离子方程式为________.
制得肼的稀溶液,该反应的离子方程式为________.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com