ЃЈ2012?ЬьНђФЃФтЃЉФГбаОПаЁзщгћЬНОПSO
2ЕФЛЏбЇаджЪЃЌЩшМЦСЫШчЯТЪЕбщЗНАИЃЎ
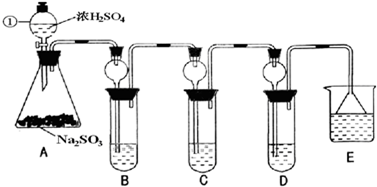
ЃЈ1ЃЉжИГівЧЦїЂйЕФУћГЦ
ЗжвКТЉЖЗ
ЗжвКТЉЖЗ
ЃЎ
ЃЈ2ЃЉМьВщAзАжУЕФЦјУмадЕФЗНЗЈЪЧ
ЙиБеЗжвКТЉЖЗЛюШћЃЌНЋЕМЙмФЉЖЫВхШыBЪдЙмЫЎжаЃЌгУЪжЮцзЁзЖаЮЦПЃЌШєдкЕМЙмПкгаЦјХнУАГіЃЌЫЩПЊЪжКѓЕМЙмжаЩЯЩ§вЛЖЮЫЎжљЃЌдђБэУїзАжУAЦјУмадСМКУ
ЙиБеЗжвКТЉЖЗЛюШћЃЌНЋЕМЙмФЉЖЫВхШыBЪдЙмЫЎжаЃЌгУЪжЮцзЁзЖаЮЦПЃЌШєдкЕМЙмПкгаЦјХнУАГіЃЌЫЩПЊЪжКѓЕМЙмжаЩЯЩ§вЛЖЮЫЎжљЃЌдђБэУїзАжУAЦјУмадСМКУ
ЃЎ
ЃЈ3ЃЉзАжУBМьбщSO
2ЕФбѕЛЏадЃЌдђBжаЫљЪЂЪдМСПЩвдЮЊ
СђЛЏЧтЫЎШмвКЃЈЛђСђЛЏФЦЁЂСђЧтЛЏФЦШмвКОљПЩЃЉ
СђЛЏЧтЫЎШмвКЃЈЛђСђЛЏФЦЁЂСђЧтЛЏФЦШмвКОљПЩЃЉ
ЃЎ
ЃЈ4ЃЉзАжУCжаЪЂзАфхЫЎгУвдМьбщSO
2ЕФ
ЛЙд
ЛЙд
адЃЌдђCжаЗДгІЕФРызгЗНГЬЪНЮЊ
SO2+Br2+2H2O=SO42-+4H++2Br-
SO2+Br2+2H2O=SO42-+4H++2Br-
ЃЎ
ЃЈ5ЃЉзАжУDжаЪЂзАаТжЦЦЏАзЗлХЈШмвКЭЈШыSO
2вЛЖЮ
ММфКѓЃЌDжаГіЯжСЫДѓСПАзЩЋГСЕэЃЎЭЌбЇУЧЖдАзЩЋГСЕэГЩЗжЬсГіШ§жжМйЩшЃК
ЂйМйЩшвЛЃКИУАзЩЋГСЕэЮЊCaSO
3МйЩшЖўЃКИУАзЩЋГСЕэЮЊ
CaSO4
CaSO4
ЃЎ
МйЩшШ§ЃКИУАзЩЋГСЕэЮЊЩЯЪіСНжжЮяжЪЕФЛьКЯЮяЃЎ
ЂкЛљгкМйЩшвЛЃЌЭЌбЇУЧЖдАзЩЋГСЕэГЩЗжНјааСЫЬНОПЃЎЩшМЦШчЯТЗНАИЃК
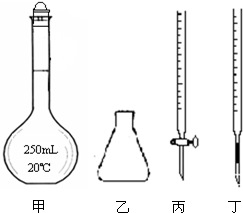
ЯобЁЕФвЧЦїКЭЪдМСЃЛЙ§ТЫзАжУЁЂЪдЙмЁЂЕЮЙмЁЂДјЕМЙмЕФЕЅПзШћЁЂеєСѓЫЎЁЂ0.5molЃЎL
-1 HClЁЂ0.5molЃЎL
-1 H
2SO
4ЁЂ0.5molЃЎL
-1BaCl
2ЁЂ1molЃЎL
-1 NaOHЁЂЦЗКьШмвКЃЎ
Ек1ВНЃЌНЋDжаГСЕэЙ§ТЫЁЂЯДЕгИЩОЛЃЌБИгУЃЎ
ЧыЛиД№ЯДЕгГСЕэЕФЗНЗЈЃК
биВЃСЇАєЯђТЉЖЗжаМгеєСѓЫЎжСНўУЛГСЕэЃЌД§ЫЎСїОЁКѓжиИД2ЁЋ3ДЮвдЩЯВйзї
биВЃСЇАєЯђТЉЖЗжаМгеєСѓЫЎжСНўУЛГСЕэЃЌД§ЫЎСїОЁКѓжиИД2ЁЋ3ДЮвдЩЯВйзї
ЃЎ
Ек2ВНЃЌгУСэвЛжЛИЩОЛЪдЙмШЁЩйСПГСЕэбљЦЗЃЌМгШы
Й§СПЃЈЛђЪЪСПЃЉ0.5molЃЎL-1HClЁЂ
Й§СПЃЈЛђЪЪСПЃЉ0.5molЃЎL-1HClЁЂ
ЃЈЪдМСЃЉЃЌШћЩЯДјЕМЙмЕФЕЅПзШћЃЌНЋЕМЙмЕФСэвЛЖЫВхШыЪЂга
ЦЗКьШмвК
ЦЗКьШмвК
ЃЈЪдМСЃЉЕФЪдЙмжаЃЎ
ШєГіЯж
ШєЙЬЬхЭъШЋШмНтЃЌгаЦјХнВњЩњЃЌЧвФмЪЙЦЗКьШмвКЭЪЩЋ
ШєЙЬЬхЭъШЋШмНтЃЌгаЦјХнВњЩњЃЌЧвФмЪЙЦЗКьШмвКЭЪЩЋ
ЯжЯѓЃЌдђМйЩшвЛГЩСЂЃЎ
ЂлШєМйЩшЖўГЩСЂЃЌЪдаДГіЩњГЩИУАзЩЋГСЕэЕФЛЏбЇЗНГЬЪНЃК
CaЃЈClOЃЉ2+H2O+SO2=CaSO4+2HCl
CaЃЈClOЃЉ2+H2O+SO2=CaSO4+2HCl
ЃЎ
ЃЈ6ЃЉзАжУEжаЪЂЗХЕФЪдМСЪЧ
NaOHШмвК
NaOHШмвК
ЃЌзїгУЪЧ
ЮќЪеSO2ЃЌЗРжЙдьГЩПеЦјЮлШО
ЮќЪеSO2ЃЌЗРжЙдьГЩПеЦјЮлШО
ЃЎ

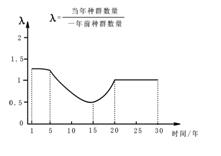

 ИпУЬЫсМиЪЧвЛжжживЊЕФЛЏбЇЪдМСЃЌЦфШмвКВЛКмЮШЖЈЃЌдкЫсадЬѕМўЯТЛсЗжНтЩњГЩЖўбѕЛЏУЬКЭбѕЦјЃЌдкжаадЛђШѕМюадШмвКжаЗжНтЫйЖШКмТ§ЃЌМћЙтЗжНтЫйЖШМгПьЃЎ
ИпУЬЫсМиЪЧвЛжжживЊЕФЛЏбЇЪдМСЃЌЦфШмвКВЛКмЮШЖЈЃЌдкЫсадЬѕМўЯТЛсЗжНтЩњГЩЖўбѕЛЏУЬКЭбѕЦјЃЌдкжаадЛђШѕМюадШмвКжаЗжНтЫйЖШКмТ§ЃЌМћЙтЗжНтЫйЖШМгПьЃЎ