
МвДҝБРұн(°ьАЁҙр°ёәНҪвОц)
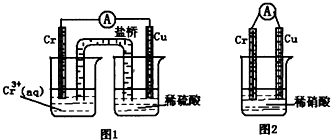


| КөСйДЪИЭ | КөСйПЦПу | |
| A | КХјҜТ»јҜЖшЖҝЖшМеЈ¬№ЫІмСХЙ«Ј¬И»әуПтЖҝДЪө№ИлФјХјЖҝИЭ»э1/5өДХфБуЛ®Ј¬ід·ЦХсөҙЈ® | ХфБуЛ®іКЗі»ЖВМЙ«Ј¬ЖҝДЪЖшМеИФіК»ЖВМЙ«Ј® |
| B | ИЎіцЖҝДЪІҝ·ЦИЬТәЈ¬өОИлЧПЙ«КҜИпКФТәЦРЦұЦБ№эБҝЈ® | ЧПЙ«КҜИпКФТәПИұдәмЙ«Ј¬әуәмЙ«НКЙ«Ј® |
| C | ИЎіцЖҝДЪКЈПВөДІҝ·ЦИЬТәЈ¬өОИлПхЛбТшИЬТәЦРЈ® | ІъЙъҙуБҝ°ЧЙ«іБөн |
| D | ЧоәуПтЖҝДЪө№ИлЙЩБҝЕЁЗвСх»ҜДЖИЬТәЈ¬ХсөҙЈ® | ЖҝДЪ»ЖВМЙ«ЖшМеБўјҙПыК§Ј® |
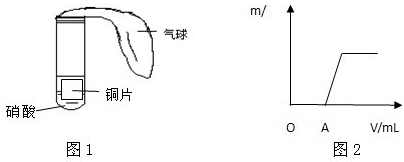

РВЦЖөДВИЛ®іКөӯ»ЖВМЙ«Ј¬ЛөГчВИЛ®ЦРУР____________·ЦЧУҙжФЪЈ»ПтВИЛ®ЦРөОИлјёөОAgNO3ИЬТәЈ¬БўјҙЙъіЙ°ЧЙ«іБөнЈ¬ЛөГчВИЛ®ЦРУР_____________ҙжФЪЈ»А¶Й«КҜИпКФЦҪУцөҪВИЛ®әуЈ¬КЧПИұдәмЈ¬ө«әЬҝмУЦНКЙ«Ј¬ХвКЗТтОӘ__________Ј»ВИЛ®ҫӯ№вХХәуЈ¬өӯ»ЖВМЙ«ЦрҪҘПыК§Ј¬Іў·ЕіцОЮЙ«өДЖшМеЈ¬ёГ·ҙУҰөД»ҜС§·ҪіМКҪКЗ__________ЎЈ?
Ҫ«Т»КўВъCl2ЖшМеөДКФ№Ьө№БўФЪЛ®ІЫЦРЈ¬өұИХ№вХХЙдТ»¶ОКұјдәуЈ¬КФ№ЬЦРЖшМеСХЙ«ұдіЙөӯ»ЖВМЙ«Ј¬ҙЛКұКФ№ЬЦРөДЖшМеКЗ( )
AЈ®Ц»УРO2 BЈ®Ц»УРCl2 CЈ®O2ЎўC12 DЈ®ОЮ·ЁЕР¶П
№ъјКѧУУЕСЎ - Б·П°ІбБРұн - КФМвБРұн
әюұұКЎ»ҘБӘНшОҘ·ЁәНІ»БјРЕПўҫЩұЁЖҪМЁ | НшЙПУРәҰРЕПўҫЩұЁЧЁЗш | өзРЕХ©ЖӯҫЩұЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРәҰРЕПўҫЩұЁЧЁЗш | ЙжЖуЗЦИЁҫЩұЁЧЁЗш
ОҘ·ЁәНІ»БјРЕПўҫЩұЁөз»°Јә027-86699610 ҫЩұЁУКПдЈә58377363@163.com