
题目列表(包括答案和解析)
在25℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表:
![]()

![]() 下列说法错误的是:
下列说法错误的是:![]()
![]()
 w.w.w.k.s.5.u.c.o.m
w.w.w.k.s.5.u.c.o.m
![]() A.反应达到平衡时,X的转化率为50%
A.反应达到平衡时,X的转化率为50%
![]() B.反应可表示为X+3Y
B.反应可表示为X+3Y![]() 2Z,其平衡常数为1600
2Z,其平衡常数为1600
![]() C.增大压强使平衡向生成Z的方向移动,平衡常数增大
C.增大压强使平衡向生成Z的方向移动,平衡常数增大
![]() D.改变温度可以改变此反应的平衡常数
D.改变温度可以改变此反应的平衡常数
(14分)氢氧燃料电池是符合绿色化学理念的新型发电装置。下图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定,请回答:
![]()
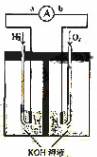
(1)氢氧燃料电池的能量转化主要形式是 ,在导线中电子流动方向为 (用a、b 表示)。
![]() (2)负极反应式为 。
(2)负极反应式为 。
![]() (3)电极表面镀铂粉的原因为 。
(3)电极表面镀铂粉的原因为 。
![]() (4)该电池工作时,H2和O2连续由外部供给,电池可连续不断提供电能。因此,大量安全储氢是关键技术之一。金属锂是一种重要的储氢材料,吸氢和放氢原理如下:w.w.w.k.s.5.u.c.o.m
(4)该电池工作时,H2和O2连续由外部供给,电池可连续不断提供电能。因此,大量安全储氢是关键技术之一。金属锂是一种重要的储氢材料,吸氢和放氢原理如下:w.w.w.k.s.5.u.c.o.m
![]() Ⅰ.2Li+H2
Ⅰ.2Li+H2![]()
![]() 2LIH
2LIH
![]() Ⅱ.LiH+H2O==LiOH+H2↑
Ⅱ.LiH+H2O==LiOH+H2↑
![]() ①反应Ⅰ中的还原剂是 ,反应Ⅱ中的氧化剂是 。
①反应Ⅰ中的还原剂是 ,反应Ⅱ中的氧化剂是 。
②已知LiH固体密度为0.82g/cm3。用锂吸收224L(标准状况)H2,生成的LiH体积与被吸收的H2体积比为 。
③由②生成的LiH与H2O作用,放出的H2用作电池燃料,若能量转化率为80%,则导线中通过电子的物质的量为 mol。
下列实验操作正确的是 ( )w.w.w.k.s.5.u.c.o.m
A.将氢氧化钠固体放在滤纸上称量
B.用10ml量筒量取8.58mL蒸馏水
C.制取氯气时,用二氧化锰与浓盐酸在常温下反应,并用排水集气法收集
D.配置氯化铁溶液时,将一定量氯化铁溶液溶解在较浓的盐酸中,再用水稀释到所需浓度
下列叙述中正确的是( )w.w.w.k.s.5.u.c.o.m
A.NH3、CO、CO2都是极性分子
B.CH4、CCl4都是含有极性键的非极性分子
C.HF、HCl、HBr、Hl的稳定性依次增强
D.CS2、H2O、C2H2都是直线型分子
铝在人体内积累可使人慢性中毒,引起老年痴呆症,世界卫生组织已正式将铝确定为“食品污染源之一”而加以控制,铝在下列使用场合一般无需控制的是 ( )w.w.w.k.s.5.u.c.o.m
A.铝箔电容 B.牙膏皮 C.制造炊具和餐具 D.糖果香烟包装
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com