
ÌâÄ¿Áбí(°üÀ¨´ð°¸ºÍ½âÎö)
1996Äêŵ±´¶û»¯Ñ§½±ÊÚÓè¶Ô·¢ÏÖ ![]() ÓÐÖØ´ó¹±Ï×µÄÈýλ¿Æѧ¼Ò.
ÓÐÖØ´ó¹±Ï×µÄÈýλ¿Æѧ¼Ò.![]() ·Ö×ÓÊÇÐÎÈçÇò×´µÄ¶àÃæÌå(Èçͼ2¡ª20)£¬¸Ã½á¹¹µÄ½¨Á¢»ùÓÚÒÔÏ¿¼ÂÇ£º
·Ö×ÓÊÇÐÎÈçÇò×´µÄ¶àÃæÌå(Èçͼ2¡ª20)£¬¸Ã½á¹¹µÄ½¨Á¢»ùÓÚÒÔÏ¿¼ÂÇ£º

¢Ù![]() ·Ö×ÓÖÐÿ¸ö̼Ô×ÓÖ»¸úÏàÁÚµÄ3¸ö̼Ô×ÓÐγɻ¯Ñ§¼ü£»¢Ú
·Ö×ÓÖÐÿ¸ö̼Ô×ÓÖ»¸úÏàÁÚµÄ3¸ö̼Ô×ÓÐγɻ¯Ñ§¼ü£»¢Ú![]() ·Ö×ÓÖ»º¬ÓÐÎå±ßÐκÍÁù±ßÐΣ»¢Û¶àÃæÌåµÄ¶¥µãÊý¡¢ÃæÊýºÍÀâ±ßÊýµÄ¹Øϵ×ñÑÅ·À¶¨Àí£º¶¥µãÊý+ÃæÊý-Àâ±ßÊý£½2.¾ÝÉÏËùÊö£¬¿ÉÍÆÖª
·Ö×ÓÖ»º¬ÓÐÎå±ßÐκÍÁù±ßÐΣ»¢Û¶àÃæÌåµÄ¶¥µãÊý¡¢ÃæÊýºÍÀâ±ßÊýµÄ¹Øϵ×ñÑÅ·À¶¨Àí£º¶¥µãÊý+ÃæÊý-Àâ±ßÊý£½2.¾ÝÉÏËùÊö£¬¿ÉÍÆÖª![]() ·Ö×ÓÓÐ12¸öÎå±ßÐκÍ20¸öÁù±ßÐΣ¬
·Ö×ÓÓÐ12¸öÎå±ßÐκÍ20¸öÁù±ßÐΣ¬![]() ·Ö×ÓËùº¬µÄË«¼üÊýΪ30.Çë»Ø´ðÏÂÁÐÎÊÌ⣺
·Ö×ÓËùº¬µÄË«¼üÊýΪ30.Çë»Ø´ðÏÂÁÐÎÊÌ⣺
(1)¹ÌÌå![]() Óë½ð¸ÕʯÏà±È½Ï£¬ÈÛµã½Ï¸ßÕßÓ¦ÊÇ___________£¬ÀíÓÉÊÇ_________.
Óë½ð¸ÕʯÏà±È½Ï£¬ÈÛµã½Ï¸ßÕßÓ¦ÊÇ___________£¬ÀíÓÉÊÇ_________.
(2)ÊÔ¹À¼Æ![]() ¸ú
¸ú![]() ÔÚÒ»¶¨Ìõ¼þÏÂÄÜ·ñ·¢Éú·´Ó¦Éú³É
ÔÚÒ»¶¨Ìõ¼þÏÂÄÜ·ñ·¢Éú·´Ó¦Éú³É![]()
![]() (Ìî¡°¿ÉÄÜ¡±»ò¡°²»¿ÉÄÜ¡±)________.²¢¼òÊöÆäÀíÓÉ£º_______.
(Ìî¡°¿ÉÄÜ¡±»ò¡°²»¿ÉÄÜ¡±)________.²¢¼òÊöÆäÀíÓÉ£º_______.
(3)ͨ¹ý¼ÆË㣬ȷ¶¨![]() ·Ö×ÓËùº¬µ¥¼üÊýΪ________.
·Ö×ÓËùº¬µ¥¼üÊýΪ________.
(4)![]() ·Ö×ÓÒ²ÒÑÖƵã¬ËüµÄ·Ö×ӽṹģÐÍ¿ÉÒÔÓë
·Ö×ÓÒ²ÒÑÖƵã¬ËüµÄ·Ö×ӽṹģÐÍ¿ÉÒÔÓë![]() ͬÑù¿¼ÂǶøÍÆÖª£¬Í¨¹ý¼ÆËãÈ·¶¨
ͬÑù¿¼ÂǶøÍÆÖª£¬Í¨¹ý¼ÆËãÈ·¶¨![]() ·Ö×ÓÖÐÎå±ßÐκÍÁù±ßÐεÄÊýÄ¿.
·Ö×ÓÖÐÎå±ßÐκÍÁù±ßÐεÄÊýÄ¿.![]() ·Ö×ÓÖÐËùº¬Îå±ßÐÎÊýΪ__________£¬Áù±ßÐÎÊýΪ________.
·Ö×ÓÖÐËùº¬Îå±ßÐÎÊýΪ__________£¬Áù±ßÐÎÊýΪ________.
(5)µÂ¹úºÍÃÀ¹ú¿Æѧ¼ÒÊ×´ÎÖÆÔì³öÁËÓÉ20¸ö̼Ô×Ó×é³ÉµÄ¿ÕÐÄÁý×´·Ö×Ó£¬Èçͼ2-21Ëùʾ.ÕâÒ»³É¹û¿¯µÇÔÚ2000Äê9ÔÂ7ÈÕ³ö°æµÄÓ¢¹ú¡¶×ÔÈ»¡·ÔÓÖ¾ÉÏ.¸ù¾ÝÀíÂÛ¼ÆË㣬°üº¬20¸ö̼Ô×Ó¡¢½ö½öÓÉÕýÎå±ßÐι¹³ÉµÄ![]() ·Ö×ÓÊǸ»ÀÕʽ½á¹¹·Ö×ÓÖÐ×îСµÄÒ»ÖÖ.
·Ö×ÓÊǸ»ÀÕʽ½á¹¹·Ö×ÓÖÐ×îСµÄÒ»ÖÖ.![]() ÖÐÓÐ__________¸öÎå±ßÐΣ»¹²ÓÐ______ÌõÀâ±ß.
ÖÐÓÐ__________¸öÎå±ßÐΣ»¹²ÓÐ______ÌõÀâ±ß.

(6)Ä¿Ç°£¬¿Æѧ¼ÒÄâºÏ³ÉÒ»ÖÖ¡°¶þÖع¹Ô족µÄÇòÐÍ·Ö×Ó£¬¼´°Ñ¡°×ãÇòÐÍ¡±µÄ![]() Óë¡°×ãÇòÐÍ¡±µÄ
Óë¡°×ãÇòÐÍ¡±µÄ![]() µÄ·Ö×Ó½øÐÐÖØй¹Ô죬²¢Ê¹¹èÔ×ÓÓë̼Ô×ÓÒÔ¹²¼Û¼ü½áºÏ.Çë»Ø´ðÏÂÁÐÎÊÌ⣺
µÄ·Ö×Ó½øÐÐÖØй¹Ô죬²¢Ê¹¹èÔ×ÓÓë̼Ô×ÓÒÔ¹²¼Û¼ü½áºÏ.Çë»Ø´ðÏÂÁÐÎÊÌ⣺
¢ÙÄãÈÏΪ![]() Óë
Óë![]() µÄ·Ö×ÓÓ¦²ÉÈ¡ÔõÑùµÄÏâǶ_________£¬ÀíÓÉÊÇ________.
µÄ·Ö×ÓÓ¦²ÉÈ¡ÔõÑùµÄÏâǶ_________£¬ÀíÓÉÊÇ________.
¢Ú¡°¶þÖع¹Ô족ºóµÄ¾§ÌåÊôÓÚ_________¾§Ì壬ÆäÈÛµãÓë![]() ¡¢
¡¢![]() Ïà±È_______.
Ïà±È_______.
(7)×î½üÓÐÈËÓÃÒ»ÖÖ³ÆΪ¡°³¬ËᡱµÄ»¯ºÏÎï![]() ºÍ
ºÍ![]() ·´Ó¦£¬Ê¹
·´Ó¦£¬Ê¹![]() »ñµÃÒ»¸öÖÊ×Ó£¬µÃµ½Ò»ÖÖÐÂÐÍÀë×Ó»¯ºÏÎï
»ñµÃÒ»¸öÖÊ×Ó£¬µÃµ½Ò»ÖÖÐÂÐÍÀë×Ó»¯ºÏÎï![]() .»Ø´ðÈçÏÂÎÊÌ⣺
.»Ø´ðÈçÏÂÎÊÌ⣺
¢ÙÒÔÉÏ·´Ó¦ÀàÐÍÉÏ¿ÉÒÔ¸úÖÐѧ»¯Ñ§¿Î±¾ÖеÄÒ»¸ö»¯Ñ§·´Ó¦Ïà±ÈÄ⣬ºóÕßÊÇ_______________________.
¢ÚÉÏÊöÒõÀë×Ó![]() µÄ½á¹¹¿ÉÒÔ¸úͼ2-22µÄÅð¶þÊ®ÃæÌåÏà±ÈÄ⣬ҲÊÇÒ»¸ö±ÕºÏµÄÄÉÃ×Áý£¬¶øÇÒ£¬
µÄ½á¹¹¿ÉÒÔ¸úͼ2-22µÄÅð¶þÊ®ÃæÌåÏà±ÈÄ⣬ҲÊÇÒ»¸ö±ÕºÏµÄÄÉÃ×Áý£¬¶øÇÒ£¬![]() ×ÓÓÐÈçϽṹÌØÕ÷£ºËüÓÐÒ»¸ùÖá´©¹ýÁýÐÄ£¬ÒÀ¾ÝÕâ¸ùÖáÐýת360¡ã£¯5µÄ¶ÈÊý£¬²»Äܲì¾õÊÇ·ñÐýת¹ý.ÇëÔÚͼ2-23ÖÐÌí¼ÓÔ×Ó(ÓÃÔªËØ·ûºÅ±íʾ)ºÍ¶ÌÏß(±íʾ»¯Ñ§¼ü)»³öÉÏÊöÒõÀë×Ó.
×ÓÓÐÈçϽṹÌØÕ÷£ºËüÓÐÒ»¸ùÖá´©¹ýÁýÐÄ£¬ÒÀ¾ÝÕâ¸ùÖáÐýת360¡ã£¯5µÄ¶ÈÊý£¬²»Äܲì¾õÊÇ·ñÐýת¹ý.ÇëÔÚͼ2-23ÖÐÌí¼ÓÔ×Ó(ÓÃÔªËØ·ûºÅ±íʾ)ºÍ¶ÌÏß(±íʾ»¯Ñ§¼ü)»³öÉÏÊöÒõÀë×Ó.


£¨15·Ö£©X¡¢Y¡¢Z¡¢W¡¢R¡¢TΪǰËÄÖÜÆÚÔªËØÇÒÔ×ÓÐòÊýÒÀ´ÎÔö´ó¡£TÔ×ÓÐòÊýµÈÓÚX¡¢Y¡¢RÔ×ÓÐòÊýÖ®ºÍ¡£ZΪµØ¿ÇÖк¬Á¿×î¶àµÄÔªËØ¡£X¡¢ZÔ×ÓºËÍâ¾ùÓÐ2¸öδ³É¶Ôµç×Ó¡£ZÓëRλÓÚͬһÖ÷×å¡£X¡¢Y¡¢Z¡¢W¡¢R¡¢TÖÐÖ»ÓÐÁ½ÖÖ½ðÊôÔªËØ£¬ÇÒ´æÔÚÏÂÁз´Ó¦£º 2W+XZ2 X+2WZ
X+2WZ
»Ø´ðÏÂÁÐÎÊÌ⣺
£¨1£©X¡¢Y¡¢ZµÄµÚÒ»µçÀëÄÜ×î´óµÄÊÇ £¨ÓÃÔªËØ·ûºÅ±íʾ£©¡£
£¨2£©ÔÚÔªËØRºÍÔªËØZÐγɵij£¼û»¯ºÏÎïÖУ¬ÊôÓڷǼ«ÐÔ·Ö×ÓµÄÊÇ £¨Ìѧʽ£©£¬¸Ã·Ö×ÓÖÐÖÐÐÄÔ×ÓÒÔ ÔÓ»¯¡£
£¨3£©ÓÉX¡¢TÔªËØ×é³ÉµÄµ¥ÖÊÖÐÒ»¶¨²»´æÔÚ £¨ÌîÐòºÅ£©¡£
| A£®Àë×Ó¾§Ìå | B£®·Ö×Ó¾§Ìå | C£®Ô×Ó¾§Ìå | D£®½ðÊô¾§Ìå |

£¨15·Ö£©X¡¢Y¡¢Z¡¢W¡¢R¡¢TΪǰËÄÖÜÆÚÔªËØÇÒÔ×ÓÐòÊýÒÀ´ÎÔö´ó¡£TÔ×ÓÐòÊýµÈÓÚX¡¢Y¡¢RÔ×ÓÐòÊýÖ®ºÍ¡£ZΪµØ¿ÇÖк¬Á¿×î¶àµÄÔªËØ¡£X¡¢ZÔ×ÓºËÍâ¾ùÓÐ2¸öδ³É¶Ôµç×Ó¡£ZÓëRλÓÚͬһÖ÷×å¡£X¡¢Y¡¢Z¡¢W¡¢R¡¢TÖÐÖ»ÓÐÁ½ÖÖ½ðÊôÔªËØ£¬ÇÒ´æÔÚÏÂÁз´Ó¦£º 2W+XZ2  X+2WZ
X+2WZ
»Ø´ðÏÂÁÐÎÊÌ⣺
£¨1£©X¡¢Y¡¢ZµÄµÚÒ»µçÀëÄÜ×î´óµÄÊÇ £¨ÓÃÔªËØ·ûºÅ±íʾ£©¡£
£¨2£©ÔÚÔªËØRºÍÔªËØZÐγɵij£¼û»¯ºÏÎïÖУ¬ÊôÓڷǼ«ÐÔ·Ö×ÓµÄÊÇ £¨Ìѧʽ£©£¬¸Ã·Ö×ÓÖÐÖÐÐÄÔ×ÓÒÔ ÔÓ»¯¡£
£¨3£©ÓÉX¡¢TÔªËØ×é³ÉµÄµ¥ÖÊÖÐÒ»¶¨²»´æÔÚ £¨ÌîÐòºÅ£©¡£
A¡¢Àë×Ó¾§Ìå B¡¢·Ö×Ó¾§Ìå C¡¢Ô×Ó¾§Ìå D¡¢½ðÊô¾§Ìå
£¨4£©»ù̬TÔ×ӵĺËÍâµç×ÓÅŲ¼Ê½Îª ¡£
£¨5£©T+ÄÜÓëNH3ͨ¹ýÅäλ¼ü½áºÏΪ[T(NH3)n]+¡£¸ÃÀë×ÓÖÐT+µÄ4s¹ìµÀ¼°4p¹ìµÀͨ¹ýspÔÓ»¯½ÓÊÜNH3ÌṩµÄ¹Âµç×Ó¶Ô¡£¢Ù [T(NH3)n]+ÖÐn= ¡£¢Ú [T(NH3)n]+ÖÐT+Óën¸öµªÔ×Ó¹¹³ÉµÄ¿Õ¼ä½á¹¹³Ê ÐÍ¡£
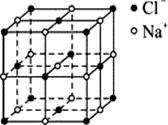
£¨6£©»¯ºÏÎïWZºÍNaClµÄ¾§°û½á¹¹ÐÎËÆ
£¨ÂÈ»¯Äƾ§°û½á¹¹ÈçÓÒͼËùʾ£©¡£
¢ÙÔÚWZÖУ¬ÑôÀë×ÓºÍÒõÀë×ÓµÄÅäλÊý¾ùΪ ¡£
¢ÚÒÑÖªWZµÄÃܶÈΪa g/cm3£¬ÔòWZÖоàÀë×î½üµÄÑôÀë×Ó¼äµÄ¾àÀëΪ pm£¨Óú¬aµÄËãʽ±íʾ£¬°¢·üÙ¤µÂÂÞ³£ÊýΪNA£©¡£
 X+2WZ
X+2WZ| A£®Àë×Ó¾§Ìå | B£®·Ö×Ó¾§Ìå | C£®Ô×Ó¾§Ìå | D£®½ðÊô¾§Ìå |
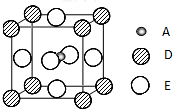 £¨2010?Ì©ÖÝÈýÄ££©ÒÑÖª£ºA¡¢B¡¢C¡¢D¡¢EΪÖÜÆÚ±í1¡«36ºÅÖеÄÔªËØ£¬ËüÃǵÄÔ×ÓÐòÊýÖð½¥Ôö´ó£®AµÄ»ù̬Ô×ÓÓÐ3¸ö²»Í¬µÄÄܼ¶£¬¸÷Äܼ¶Öеç×ÓÊýÏàµÈ£»CµÄ»ù̬Ô×Ó2pÄܼ¶ÉϵÄδ³É¶Ôµç×ÓÊýÓëAÔ×ÓÏàͬ£»C2-Àë×ÓD2+Àë×Ó¾ßÓÐÏàͬµÄ¡¢Îȶ¨µÄµç×Ó²ã½á¹¹£»EµÄ»ù̬Ô×ÓµÄÍâΧµç×ÓÅŲ¼Ê½Îª3d84s2£®
£¨2010?Ì©ÖÝÈýÄ££©ÒÑÖª£ºA¡¢B¡¢C¡¢D¡¢EΪÖÜÆÚ±í1¡«36ºÅÖеÄÔªËØ£¬ËüÃǵÄÔ×ÓÐòÊýÖð½¥Ôö´ó£®AµÄ»ù̬Ô×ÓÓÐ3¸ö²»Í¬µÄÄܼ¶£¬¸÷Äܼ¶Öеç×ÓÊýÏàµÈ£»CµÄ»ù̬Ô×Ó2pÄܼ¶ÉϵÄδ³É¶Ôµç×ÓÊýÓëAÔ×ÓÏàͬ£»C2-Àë×ÓD2+Àë×Ó¾ßÓÐÏàͬµÄ¡¢Îȶ¨µÄµç×Ó²ã½á¹¹£»EµÄ»ù̬Ô×ÓµÄÍâΧµç×ÓÅŲ¼Ê½Îª3d84s2£®¹ú¼ÊѧУÓÅÑ¡ - Á·Ï°²áÁбí - ÊÔÌâÁбí
ºþ±±Ê¡»¥ÁªÍøÎ¥·¨ºÍ²»Á¼ÐÅÏ¢¾Ù±¨Æ½Ì¨ | ÍøÉÏÓк¦ÐÅÏ¢¾Ù±¨×¨Çø | µçÐÅթƾٱ¨×¨Çø | ÉæÀúÊ·ÐéÎÞÖ÷ÒåÓк¦ÐÅÏ¢¾Ù±¨×¨Çø | ÉæÆóÇÖȨ¾Ù±¨×¨Çø
Î¥·¨ºÍ²»Á¼ÐÅÏ¢¾Ù±¨µç»°£º027-86699610 ¾Ù±¨ÓÊÏ䣺58377363@163.com