
题目列表(包括答案和解析)
下列词语中加点的字,读音全都正确的一组是
A.谛(dì)听 横(hénɡ)祸 丢三落(là)四 B.沮(jǔ)丧 窥(kuī)视 宁(nìnɡ)缺毋滥
C.褒(bǎo)贬 透辟(pì) 卓(zhuó)尔不群 D.当(dànɡ)真 牵掣(chè) 屡见不鲜(xiǎn)
化学反应可视为旧键断裂和新键形成的过程。化学键的键能是两种原子间形成1mol化学键时释放的能量或断开1mol化学键所吸收的能量。现提供以下化学键的键能(kJ/mol)
P-P:198 P-O:360 O=O:498 P=O:585
试根据这些数据,计算以下反应的反应热Q。
P4(白磷)+5O2=P4O10;Q
 (提示:白磷是正四面体型的分子,当与氧形成P4O10时,每两个磷原子之间插入一个氧原子,此外,每个磷原子又以双键结合一个氧原子)
(提示:白磷是正四面体型的分子,当与氧形成P4O10时,每两个磷原子之间插入一个氧原子,此外,每个磷原子又以双键结合一个氧原子)
化学反应可视为旧键断裂和新键形成的过程。化学键的键能是两种原子间形成1mol化学键时释放的能量或断开1mol化学键时所吸收的能量。现提供以下化学键的键能(kJ/mol)P―P:198 P―O:360 O=O:498 P=O:585
试根据这些数据,计算以下反应的Q
P4(白磷)(g) + 5O2(g) = P4O10(g); ΔH=―Q kJ/mol
(提示:白磷是正四面体型的分子,当与氧形成P4O10时,每两个磷原子之间插入一个氧原子,此外每个磷原子又以双键结合一个氧原子)
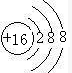

| C | N | O | F | ||
| Si | P | S | Cl | ||
| Ge | As | Se | Br | ||
| Sn | Sb | Te | I | ||
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com