
题目列表(包括答案和解析)
(1)所有原子都含有________________。
(2)所有离子都含有________________。
(3)原子在化学反应中发生变化的是________________。
(4)决定原子相对原子质量的粒子是________________。
(5)同位素中的不同原子具有相同数目的________________。
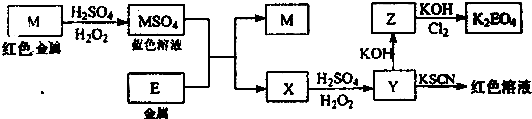
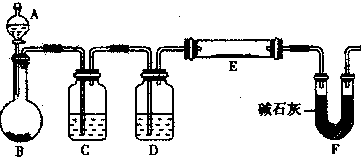
(15分)某化学兴趣小组拟采用下图装置甲电解饱和氯化钠溶液,并用电解产生的H2还原CuO粉末来测定Cu的相对原子质量Ar(Cu),同时检验氯气的氧化性,图中夹持和加热仪器已略去。
(1)写出装置甲中反应的离子方程式: 。
(2)为完成上述实验,正确的连接顺序为a连 ,b连 (填写连接的字母)。
(3)装置乙中第一个广口瓶内的溶液不能是( )
A. 淀粉碘化钾溶液 B. NaOH溶液
C. FeCl2与KSCN混合溶液 D. Na2SO3溶液
(4)在对硬质玻璃管里的氧化铜粉末加热前,需进行的操作为 。
(5)装置丙中广口瓶内盛放的试剂为 ,作用是 。
(6)为了测定Cu的相对原子质量,某同学通过实验测得丙装置反应前后如下数据:样品质量为m1 g、反应后硬质玻璃管中剩余固体质量为m2 g、反应前后U型管及其中固体质量差为m3 g、反应前后洗气瓶及其中液体质量差为m4 g。
①请选择理论上误差最小的一组数据计算Ar(Cu),Ar(Cu)= 。
②如果选用其他组数据进行计算,会导致Ar(Cu) (填“偏大”、“偏小”或“不受影响”),理由是 。
根据氨气还原氧化铜的反应,可设计测定铜元素相对原子质量Ar(Cu)(近似值)的实验。先称量反应物氧化铜的质量m(CuO),反应完全后测定生成物水的质量m(H2O),同时生成有一种对环境无害的气体,由此计算Ar(Cu)。为此,提供的实验仪器及试剂如下(根据需要可重复选用,加入的NH4C1与Ca(OH)2的量足以产生使CuO完全还原的氨气):
请回答下列问题:
(1)检验装置A的气密性的方法是
。
(2)装置A中发生反应的化学方程式为 ,氨气还原炽热氧化铜的化学方程式为 。
(3)从所提供的仪器及试剂中选择并组装本实验的一套合理、简单的装置,按气流方向的连接顺序为(用图中标注的导管口符号表示)a→ 。
(4)在本实验中,若测得m(CuO)=ag,m(H2O)=bg,则Ar(Cu)= 。
(5)在本实验中,使测定结果Ar(Cu)偏大的是_______________(填序号)。
①CuO未完全起反应 ②CuO不干燥 ③CuO中混有不反应的杂质
④碱石灰不干燥 ⑤NH4C1与Ca(OH)2混合物不干燥
(6)在本实验中,还可通过测定______________和_____________,或_______________和_______________达到实验目的。
(20分)某课外小组利用H2还原CuO粉末测定铜元素的相对原子质量,下图是测定装置的示意图,A中的试剂是盐酸,C中试剂是稀氢氧化钠溶液。
请回答下列问题。
(1)仪器中装入的试剂:B 、D 。
(2)装置C的作用是 。
(3)连接好装置后应首先 。
(4)“①加热反应管E”和“②从A瓶逐滴滴加液体”这两步操作应该先进行的是 (填序号)。在这两步之间还应进行的操作是 。
(5)反应过程中G管逸出的气体是 ,其处理方法是 。
(6)从实验中测得了下列数据:
①空E管的质量a ; ②E管和CuO的总质量b;
③反应后E管和Cu粉的总质量c(冷却到室温称量);
④反应前F管及内盛物的总质量d ;⑤反应后F管及内盛物的总质量e。
由以上数据可以列出计算Cu的相对原子质量的两个不同计算式(除Cu外,其他涉及的元素的相对原子质量均为已知):
计算式1:Ar(Cu)= ;计算式2:Ar(Cu)= 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com