
ĢāÄæĮŠ±ķ(°üĄØ“š°øŗĶ½āĪö)
µē½ā·ØŌŚ½šŹō¾«Į¶”¢±£»¤»·¾³”¢“¦Ąķ·ĻĖ®ÖŠĘš×ÅŹ®·ÖÖŲŅŖµÄ×÷ÓĆ”£
(1)ČēĶ¼ĪŖµē½ā¾«Į¶ŅųµÄŹ¾ŅāĶ¼£¬________(Ģīa»ņb)¼«ĪŖŗ¬ÓŠŌÓÖŹµÄ“ÖŅų£¬Čōb¼«ÓŠÉŁĮæŗģ×ŲÉ«ĘųĢåÉś³É£¬ŌņÉś³ÉøĆĘųĢåµÄµē¼«·“Ó¦Ź½ĪŖ______________________”£
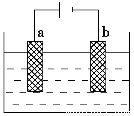
AgNO3”ŖHNO3ČÜŅŗ
(2)µē½ā·Ø“¦ĄķĖįŠŌŗ¬øõ·ĻĖ®(Ö÷ŅŖŗ¬ÓŠCr2O72£)Ź±£¬ŅŌĢś°å×÷Ņõ”¢Ńō¼«£¬“¦Ąķ¹ż³ĢÖŠ“ęŌŚ·“Ó¦Cr2O72££«6Fe2£«£«14H£«=2Cr3£«£«6Fe3£«£«7H2O£¬×īŗóCr3£«ŅŌCr(OH)3ŠĪŹ½³żČ„”£»Ų“šĻĀĮŠĪŹĢā£ŗ
¢ŁŠ“³öµē¼«·“Ó¦Ź½£ŗŅõ¼«________________£¬Ńō¼«________________”£
¢Śµ±Éś³É1 mol Cr(OH)3Ź±£¬µēĀ·ÖŠ×ŖŅʵē×ÓµÄĪļÖŹµÄĮæÖĮÉŁĪŖ________mol”£
¢Ūµē½ā¹ż³ĢÖŠÓŠFe(OH)3³ĮµķÉś³É£¬ŌŅņŹĒ___________________________”£
(3)µē½ā½µ½ā·ØæÉÓĆÓŚÖĪĄķĖ®ÖŠĻõĖįŃĪµÄĪŪČ¾”£µē½ā½µ½āNO3£µÄŌĄķČēĶ¼ĖłŹ¾”£
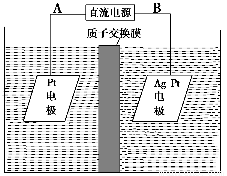
µēŌ“Õż¼«ĪŖ________(ĢīA»ņB)£¬Ņõ¼«·“Ó¦Ź½ĪŖ______________________”£
¢ŚČōµē½ā¹ż³ĢÖŠ×ŖŅĘĮĖ2 molµē×Ó£¬ŌņĤĮ½²ąµē½āŅŗµÄÖŹĮæ±ä»Æ²ī(¦¤m×󣦤mÓŅ)ĪŖ________g”£
µē½ā·ØŌŚ½šŹō¾«Į¶”¢±£»¤»·¾³”¢“¦Ąķ·ĻĖ®ÖŠĘš×ÅŹ®·ÖÖŲŅŖµÄ×÷ÓĆ”£
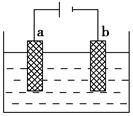
(1)ČēĶ¼ĪŖµē½ā¾«Į¶ŅųµÄŹ¾ŅāĶ¼£¬________(Ģīa»ņb)¼«ĪŖŗ¬ÓŠŌÓÖŹµÄ“ÖŅų£¬Čōb¼«ÓŠÉŁĮæŗģ×ŲÉ«ĘųĢåÉś³É£¬ŌņÉś³ÉøĆĘųĢåµÄµē¼«·“Ó¦Ź½ĪŖ______________________”£
AgNO3”ŖHNO3ČÜŅŗ
(2)µē½ā·Ø“¦ĄķĖįŠŌŗ¬øõ·ĻĖ®(Ö÷ŅŖŗ¬ÓŠCr2O72£)Ź±£¬ŅŌĢś°å×÷Ņõ”¢Ńō¼«£¬“¦Ąķ¹ż³ĢÖŠ“ęŌŚ·“Ó¦Cr2O72££«6Fe2£«£«14H£«=2Cr3£«£«6Fe3£«£«7H2O£¬×īŗóCr3£«ŅŌCr(OH)3ŠĪŹ½³żČ„”£»Ų“šĻĀĮŠĪŹĢā£ŗ
¢ŁŠ“³öµē¼«·“Ó¦Ź½£ŗŅõ¼«________________£¬Ńō¼«________________”£
¢Śµ±Éś³É1 mol Cr(OH)3Ź±£¬µēĀ·ÖŠ×ŖŅʵē×ÓµÄĪļÖŹµÄĮæÖĮÉŁĪŖ________mol”£
¢Ūµē½ā¹ż³ĢÖŠÓŠFe(OH)3³ĮµķÉś³É£¬ŌŅņŹĒ___________________________”£
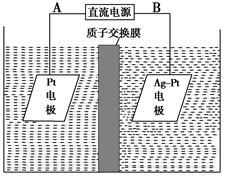
(3)µē½ā½µ½ā·ØæÉÓĆÓŚÖĪĄķĖ®ÖŠĻõĖįŃĪµÄĪŪČ¾”£µē½ā½µ½āNO3£µÄŌĄķČēĶ¼ĖłŹ¾”£
µēŌ“Õż¼«ĪŖ________(ĢīA»ņB)£¬Ņõ¼«·“Ó¦Ź½ĪŖ______________________”£
¢ŚČōµē½ā¹ż³ĢÖŠ×ŖŅĘĮĖ2 molµē×Ó£¬ŌņĤĮ½²ąµē½āŅŗµÄÖŹĮæ±ä»Æ²ī(¦¤m×󣦤mÓŅ)ĪŖ________g”£
ÓŠA”¢B”¢C”¢DĖÄÖÖµē½āÖŹµÄĖ®ČÜŅŗ£¬ŃęÉ«·“Ó¦¾łĪŖ»ĘÉ«”£AĻŌĖįŠŌ£¬BĻŌ¼īŠŌ£¬C”¢DĪŖĮ½ÖÖŃĪ”£ŌŚAµÄĖ®ČÜŅŗĄļ¼ÓČėHNO3Ėį»ÆµÄBaCl2ČÜŅŗ£¬²śÉś°×É«³Įµķ£»AÓėB”¢C”¢D·“Ó¦Ź±£¬BĪŽĆ÷ĻŌĻÖĻó£¬CŗĶD¾łÄܲśÉśĪŽÉ«”¢ĪŽĪ¶”¢ÄÜŹ¹³ĪĒåŹÆ»ŅĖ®±ä»ė×ĒµÄĘųĢ壻BŗĶDŅ²æÉ·“Ӧɜ³ÉC”£ŹŌ»Ų“š£ŗ
(1)Š“»ÆѧŹ½£ŗA._________£¬B._________£¬C._________£¬D._________”£
(2)BÓėD×÷ÓƵĥė×Ó·½³ĢŹ½£ŗ_______________________________”£
(3)AÓėD·“Ó¦µÄĄė×Ó·½³ĢŹ½£ŗ_______________________________”£
ÓŠA”¢B”¢C”¢DĖÄÖÖµē½āÖŹµÄĖ®ČÜŅŗ£¬ŃęÉ«·“Ó¦¾łĻŌ»ĘÉ«£®AĪŖĖįŠŌ£¬BĪŖ¼īŠŌ£¬C”¢DĪŖĮ½ÖÖŃĪ£®ŌŚAµÄĖ®ČÜŅŗĄļ¼ÓČėHNO3Ėį»ÆµÄBaCl2ČÜŅŗ£¬²śÉś°×É«³Įµķ£»AÓėB”¢C”¢D·“Ó¦Ź±£¬BĪŽĆ÷ĻŌĻÖĻó£¬CŗĶD¾łÄܲśÉśĪŽÉ«”¢ĪŽŠį”¢²¢ÄÜŹ¹³ĪĒåŹÆ»ŅĖ®±ä»ė×ĒµÄĘųĢ壻BŗĶDŅ²æÉĻą»„·“Ӧɜ³ÉC£®ŹŌ»Ų“š£ŗ
(1)Š“³ö»ÆѧŹ½£ŗA________£¬B________£¬C________D________£»
(2)BÓėD×÷ÓƵĥė×Ó·½³ĢŹ½ĪŖ________________£»
(3)AÓėD×÷ÓƵĥė×Ó·½³ĢŹ½ĪŖ________________£»
(4)AĻŌĖįŠŌµÄŌŅņ________________£®
Ņ»”¢¶žŃ”ŌńĢā“š°ø
1
2
3
4
5
6
B
D
D
A
C
C
7
8
9
10
11
12
A
C
D
C
D
C
13
14
15
16
17
18
B
C
D
A
D
D
19
20
21
22
23
D
B
C
B
A
Čż”¢
24”¢£Ø7·Ö£©
(1) H £ŗ O £ŗ H (1·Ö)
£Ø2·Ö£©3NO2+H2O=2HNO3+NO
Cl2+H2O=HCl+HClO
2Na2O2+2H2O=4NaOH+O2ӟ
25”¢£Ø6·Ö£©
£Ø1£© C ŃõŌ×Ó½į¹¹Ź¾ŅāĶ¼ £ØĆææÕ1·Ö£©
 £Ø2£©
Al2(SO4)3 £Ø1·Ö£© Al3+ +
3H2O
Al(OH)3 +3 H+ £Ø2·Ö£© ĮņĖį»ņŃĒĮņĖį»ņĢ¼Ėį£Ø1·Ö£©£ØŠ“³öŅ»ÖÖ¼“æÉ£¬ŗĻĄķ“š°øŅ²æÉ£©
£Ø2£©
Al2(SO4)3 £Ø1·Ö£© Al3+ +
3H2O
Al(OH)3 +3 H+ £Ø2·Ö£© ĮņĖį»ņŃĒĮņĖį»ņĢ¼Ėį£Ø1·Ö£©£ØŠ“³öŅ»ÖÖ¼“æÉ£¬ŗĻĄķ“š°øŅ²æÉ£©
26”¢£Ø8·Ö£©
£Ø1£©¼ŁÉč2£ŗČÜŅŗÖŠ“ęŌŚHCO3-
¼ŁÉč3£ŗČÜŅŗÖŠ“ęŌŚCO32-ŗĶHCO3-
¼ŁÉč4£ŗČÜŅŗÖŠ“ęŌŚCO32-ŗĶSO42-
¼ŁÉč5£ŗČÜŅŗÖŠ“ęŌŚSO42 ”¢HCO3- £ØĖ³Šņ²»ĻŽ”££©£Øø÷1·Ö£©
£Ø2£©¢ŁÓĆ½ŗĶ·µĪ¹ÜȔɣĮæČÜŅŗ¼ÓČėŹŌ¹ÜÖŠ£¬ŌŁÓƵĪ¹ÜČ”¹żĮæµÄ1mol/LĀČ»Æ±µČÜŅŗ²¢µĪ¼Óµ½ŹŌ¹ÜAÖŠ£¬³ä·Ö·“Ó¦ŗ󣬾²ÖĆ£¬Č»ŗó¹żĀĖ£¬½«³ĮµķŗĶĀĖŅŗ·Ö±š×°ČėĮķĶāµÄĮ½øöŹŌ¹ÜÖŠ£Ø2·Ö£©£»²śÉś°×É«³Įµķ”£
¢ŚĶł×°ÓŠ³ĮµķµÄŹŌ¹ÜÖŠ¼ÓČė¹żĮæµÄ2mol/LŃĪĖį£»³Įµķ²æ·ÖČܽāĒŅÓŠĘųĢåÉś³É”£ĖµĆ÷ŌČÜŅŗÖŠŅ»¶Øŗ¬ÓŠSO42-ŗĶCO32-”£
¢ŪĶł×°ÓŠĀĖŅŗµÄŹŌ¹ÜÖŠ¼ÓČė2mol/LŃĪĖį£»³öĻÖĪŽÉ«ĘųĢ壬ĖµĆ÷ŌČÜŅŗÖŠŗ¬ÓŠHCO3-”£
£Ø£ØĆææÕø÷1·Ö”£ĘäĖūŗĻĄķ·½°ø²ĪÕÕøų·Ö£©
27”¢£Ø13·Ö£©£Ø1£©²»ÄÜ £Ø1·Ö£© ĪĀ¶Čøߣ¬Ė®ĪŖĘųĢ¬,²»ĄūÓŚ°±ĘųµÄÉś³É £Ø2·Ö£©
(2) 25% £Ø2·Ö£©K= £Ø1·Ö£© ¼õŠ” ¼õŠ” £Ø2·Ö£©
(3) C3H3N6 £Ø2·Ö£©6CO(NH2)2=6NH3+3CO2+C3H6N6 £Ø2·Ö£©
N C N H H £Ø1·Ö£©
28”¢£Ø10·Ö£©
(1) µŚĖÄÖÜĘŚ£¬µŚ¢ų×å £Ø2·Ö£©
(2) 3Fe3O4+8Al=9Fe+4Al2O3 £Ø2·Ö£© ÓÉĄ“Ņ±Į¶ÄŃČŪ½šŹō£ØĘäĖūÕżČ·“š°ø²ĪÕÕøų·Ö£©£Ø1·Ö£©
Al2O3+2OH-=2AlO2-+H2O £Ø2·Ö£©
(3) Cl2+2Fe2+=2Fe3++2Cl- £Ø1·Ö£© 3SCN-+Fe3+=Fe£ØSCN£©3 £Ø2·Ö£©
29”¢£Ø15·Ö£©
¢Å¢ŁŃōĄė×Ó½»»»Ä¤ £Ø2·Ö£© ¢Ś 2Cu2++4e-=2Cu 4OH-ØD4e-=2H2O+O2 £Øø÷1·Ö£©
£Ø2£©Cl2+2Br-=Br2+2Cl- £Ø2·Ö£© BrO3- 5Br- £Øø÷1·Ö£©
·ÖŅŗĀ©¶· ÉÕ±£Øø÷1·Ö£© ¢Ś £Ø1·Ö£©
£Ø3£©H2S+HDO=HDS+H2O ¢ŪH2S£ØĆææÕ2·Ö£¬¹²10·Ö£©
30”¢£Ø15·Ö£©
£Ø1£©B (1·Ö) µŚ4ÖÜĘŚµŚIB×å £Øø÷1·Ö£© 1s22s22P63s23P63d104s1»ņ[Ar] 3d104s1 (2·Ö) (2) CO2 ”¢CCl4 £ØĘäĖūŗĻĄķ“š°ø²ĪÕÕøų·Ö£©(ø÷1·Ö) ·Ö×Ó¾§Ģå Ō×Ó¾§Ģå (ø÷1·Ö) £Ø3£© 7 1 £Øø÷1·Ö£© £Ø4£© IIIA IVA £» b (ø÷1·Ö)
AµćĖłŹ¾µÄĒā»ÆĪļŹĒĖ®£¬Ęä·ŠµćŌŚŃõ×åŌŖĖŲµÄĒā»ÆĪļÖŠ×īøߏĒÓÉÓŚŌŚĖ®·Ö×Ó¼ä“ęŌŚ×ÅĒā¼ü£¬ĘäĒæ¶ČŌ¶“óÓŚ·Ö×Ó¼ä×÷ÓĆĮ¦”££Ø1·Ö£©
31”¢£Ø15·Ö£©ĀŌ
(1) £Øø÷1·Ö£©
(2) £Øø÷1·Ö£©
£Ø3£© £Øø÷2·Ö£©
(4) 3 3:2:2 £Øø÷1·Ö£©
£Ø5£© £Øø÷1·Ö£©

 w.w.w.k.s.5.u.c.o.m
w.w.w.k.s.5.u.c.o.m
www.ks5u.com
¹ś¼ŹŃ§Š£ÓÅŃ” - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com