
ƒø¡–±Ì(∞¸¿®¥∞∏∫ÕΩ‚Œˆ)
| ‘™Àÿ –‘÷ |
A | B | C | D | E | F | G | H | I | J |
| ‘≠◊”∞Îæ∂£®10-10m£© | 1.02 | 2.27 | 0.74 | 1.43 | 0.77 | 1.10 | 0.99 | 1.86 | 0.75 | 1.17 |
| ◊Ó∏þº€Ã¨ | +6 | +1 | - | +3 | +4 | +5 | +7 | +1 | +5 | +4 |
| ◊ÓµÕº€Ã¨ | -2 | - | -2 | - | -4 | -3 | -1 | - | -3 | -4 |

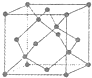 [ªØ—ß--—°–ÞŒÔ÷ Ω·ππ”Ζ‘÷ ]ƒø«∞£¨Œ“ °∂ýµÿ’˝‘⁄ª˝º´Õ∆π„ π”√ô—كУÆ≥£º˚µƒÃ´—كеÁ≥ÿ”–µ•æßπËô—كеÁ≥ÿ°¢∂ý æßπËô—كеÁ≥ÿ°¢GaAsô—كеÁ≥ÿº∞Õ≠Ó˜ÔÿŒ¯±°ƒ§Ã´—كеÁ≥ÿµ»£Æ
[ªØ—ß--—°–ÞŒÔ÷ Ω·ππ”Ζ‘÷ ]ƒø«∞£¨Œ“ °∂ýµÿ’˝‘⁄ª˝º´Õ∆π„ π”√ô—كУÆ≥£º˚µƒÃ´—كеÁ≥ÿ”–µ•æßπËô—كеÁ≥ÿ°¢∂ý æßπËô—كеÁ≥ÿ°¢GaAsô—كеÁ≥ÿº∞Õ≠Ó˜ÔÿŒ¯±°ƒ§Ã´—كеÁ≥ÿµ»£Æ£€ªØ—ß°™—°–ÞŒÔ÷ Ω·ππ”Ζ‘÷ £ð£®15∑÷£©
√¿π˙°∂ø∆—ß°∑‘”÷æ∆¿≥ˆµƒ2009ƒÍ Æ¥Ûø∆—ßÕª∆∆÷Æ“ª « ؃´œ©µƒ—–æø∫Õ”¶”√∑Ω√ʵƒÕª∆∆°£ ؃´œ©æþ”–‘≠◊”º∂µƒ∫Ò∂»°¢”≈“ϵƒµÁ—ß–‘ƒÐ°¢≥ˆ…´µƒªØ—ߌ»∂®–‘∫Õ»»¡¶—ߌ»∂®–‘°£÷∆±∏ ؃´œ©∑Ω∑®”– ؃´∞˛¿Î∑®°¢ªØ—ß∆¯œý≥¡ª˝∑®µ»°£ ؃´œ©µƒ«Úπ˜ƒ£–Õº∞∑÷◊”Ω·ππ æ“‚Õº»Á”“£∫
£®1£©œ¬¡–”–πÿ ؃´œ©Àµ∑®’˝»∑µƒ «£þ£þ£þ£þ°£
A£Æ ؃´œ©µƒΩ·ππ”ÎΩ∏’ ØœýÀ∆
B£Æ ؃´œ©∑÷◊”÷–À˘”–‘≠◊”ø…“‘¥¶”⁄Õ¨“ª∆Ω√Ê
C£Æ12g ؃´œ©∫¨¶“º¸ ˝Œ™NA
D£Æ¥” ؃´∞˛¿Îµ√ ؃´œ©–ËøÀ∑˛ ؃´≤„”Î≤„÷ƺ‰µƒ∑÷◊”º‰◊˜”√¡¶
£®2£©ªØ—ß∆¯œý≥¡ª˝∑® «ªÒµ√¥Û¡ø ؃´œ©µƒ”––ß∑Ω∑®÷Æ“ª£¨¥þªØº¡Œ™Ω°¢Õ≠°¢Óе»Ω ÙªÚ∫œΩ£¨∫¨Ãº‘¥ø…“‘ «º◊ÕÈ°¢““»≤°¢±Ω°¢““¥ºªÚÙ𺵻÷–µƒ“ª÷÷ªÚ»Œ“‚◊È∫œ°£
¢ŸÓБ≠◊”‘⁄ª˘Ã¨ ±£¨∫ÀÕ‚µÁ◊”≈≈≤º ΩŒ™£∫£þ£þ£þ£þ£þ£þ£þ£þ£þ£þ£þ£þ°£
¢⁄““¥º∑–µ„±»¬»““ÕÈ∏þ£¨÷˜“™‘≠“Ú « £þ£þ£þ£þ£þ£þ£þ£þ£þ£þ£þ£þ°£
¢€…œÕº «Ω”ÎÕ≠–Œ≥…µƒΩ Ùª•ªØŒÔ∫œΩ£¨À¸µƒªØ—ß Ωø…±Ì 挙£∫£þ£þ£þ£þ£þ£þ£þ£þ°£
¢Ð∫¨Ãº‘¥÷– Ù”⁄∑«º´–‘∑÷◊”µƒ «£þ£þ£þ£®a£Æº◊ÕÈ b£Æ““»≤ c£Æ±Ω d£Æ““¥º£©
¢ðÙðº”ÎÙðºÕ≠»æ¡œ∑÷◊”Ω·ππ»Áœ¬Õº£¨Ã™ðº∑÷◊”÷–µ™‘≠◊”≤…”√µƒ‘”ªØ∑Ω Ω”–£∫£þ£þ£þ£þ£þ£þ£þ£þ°£
£€ªØ—ß°™—°–ÞŒÔ÷ Ω·ππ”Ζ‘÷ £ð£®15∑÷£©
√¿π˙°∂ø∆—ß°∑‘”÷æ∆¿≥ˆµƒ2009ƒÍ Æ¥Ûø∆—ßÕª∆∆÷Æ“ª « ؃´œ©µƒ—–æø∫Õ”¶”√∑Ω√ʵƒÕª∆∆°£ ؃´œ©æþ”–‘≠◊”º∂µƒ∫Ò∂»°¢”≈“ϵƒµÁ—ß–‘ƒÐ°¢≥ˆ…´µƒªØ—ߌ»∂®–‘∫Õ»»¡¶—ߌ»∂®–‘°£÷∆±∏ ؃´œ©∑Ω∑®”– ؃´∞˛¿Î∑®°¢ªØ—ß∆¯œý≥¡ª˝∑®µ»°£ ؃´œ©µƒ«Úπ˜ƒ£–Õº∞∑÷◊”Ω·ππ æ“‚Õº»Á”“£∫
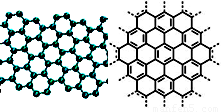
£®1£©œ¬¡–”–πÿ ؃´œ©Àµ∑®’˝»∑µƒ «£þ£þ£þ£þ°£
A£Æ ؃´œ©µƒΩ·ππ”ÎΩ∏’ ØœýÀ∆
B£Æ ؃´œ©∑÷◊”÷–À˘”–‘≠◊”ø…“‘¥¶”⁄Õ¨“ª∆Ω√Ê
C£Æ12g ؃´œ©∫¨¶“º¸ ˝Œ™NA
D£Æ¥” ؃´∞˛¿Îµ√ ؃´œ©–ËøÀ∑˛ ؃´≤„”Î≤„÷ƺ‰µƒ∑÷◊”º‰◊˜”√¡¶
£®2£©ªØ—ß∆¯œý≥¡ª˝∑® «ªÒµ√¥Û¡ø ؃´œ©µƒ”––ß∑Ω∑®÷Æ“ª£¨¥þªØº¡Œ™Ω°¢Õ≠°¢Óе»Ω ÙªÚ∫œΩ£¨∫¨Ãº‘¥ø…“‘ «º◊ÕÈ°¢““»≤°¢±Ω°¢““¥ºªÚÙ𺵻÷–µƒ“ª÷÷ªÚ»Œ“‚◊È∫œ°£

¢ŸÓБ≠◊”‘⁄ª˘Ã¨ ±£¨∫ÀÕ‚µÁ◊”≈≈≤º ΩŒ™£∫£þ£þ£þ£þ£þ£þ£þ£þ£þ£þ£þ£þ°£
¢⁄““¥º∑–µ„±»¬»““ÕÈ∏þ£¨÷˜“™‘≠“Ú « £þ£þ£þ£þ£þ£þ£þ£þ£þ£þ£þ£þ°£
¢€…œÕº «Ω”ÎÕ≠–Œ≥…µƒΩ Ùª•ªØŒÔ∫œΩ£¨À¸µƒªØ—ß Ωø…±Ì 挙£∫£þ£þ£þ£þ£þ£þ£þ£þ°£
¢Ð∫¨Ãº‘¥÷– Ù”⁄∑«º´–‘∑÷◊”µƒ «£þ£þ£þ£®a£Æº◊ÕÈ b£Æ““»≤ c£Æ±Ω d£Æ““¥º£©
¢ðÙðº”ÎÙðºÕ≠»æ¡œ∑÷◊”Ω·ππ»Áœ¬Õº£¨Ã™ðº∑÷◊”÷–µ™‘≠◊”≤…”√µƒ‘”ªØ∑Ω Ω”–£∫£þ£þ£þ£þ£þ£þ£þ£þ°£

£€ªØ—ß°™—°–ÞŒÔ÷ Ω·ππ”Ζ‘÷ £ð
√¿π˙°∂ø∆—ß°∑‘”÷æ∆¿≥ˆµƒ2009ƒÍ Æ¥Ûø∆—ßÕª∆∆÷Æ“ª « ؃´œ©µƒ—–æø∫Õ”¶”√∑Ω√ʵƒÕª∆∆°£ ؃´œ©æþ”–‘≠◊”º∂µƒ∫Ò∂»°¢”≈“ϵƒµÁ—ß–‘ƒÐ°¢≥ˆ…´µƒªØ—ߌ»∂®–‘∫Õ»»¡¶—ߌ»∂®–‘°£÷∆±∏ ؃´œ©∑Ω∑®”– ؃´∞˛¿Î∑®°¢ªØ—ß∆¯œý≥¡ª˝∑®µ»°£ ؃´œ©µƒ«Úπ˜ƒ£–Õº∞∑÷◊”Ω·ππ æ“‚Õº»Á”“£∫
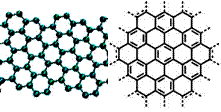
£®1£©œ¬¡–”–πÿ ؃´œ©Àµ∑®’˝»∑µƒ «£þ£þ£þ£þ°£
A£Æ ؃´œ©µƒΩ·ππ”ÎΩ∏’ ØœýÀ∆
B£Æ ؃´œ©∑÷◊”÷–À˘”–‘≠◊”ø…“‘¥¶”⁄Õ¨“ª∆Ω√Ê
C£Æ12g ؃´œ©∫¨¶“º¸ ˝Œ™NA
D£Æ¥” ؃´∞˛¿Îµ√ ؃´œ©–ËøÀ∑˛ ؃´≤„”Î≤„÷ƺ‰µƒ∑÷◊”º‰◊˜”√¡¶
£®2£©ªØ—ß∆¯œý≥¡ª˝∑® «ªÒµ√¥Û¡ø ؃´œ©µƒ”––ß∑Ω∑®÷Æ“ª£¨¥þªØº¡Œ™Ω°¢Õ≠°¢Óе»Ω ÙªÚ∫œΩ£¨∫¨Ãº‘¥ø…“‘ «º◊ÕÈ°¢““»≤°¢±Ω°¢““¥ºªÚÙ𺵻÷–µƒ“ª÷÷ªÚ»Œ“‚◊È∫œ°£
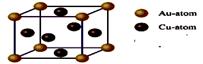
¢ŸÓБ≠◊”‘⁄ª˘Ã¨ ±£¨∫ÀÕ‚µÁ◊”≈≈≤º ΩŒ™£∫£þ£þ£þ£þ£þ£þ£þ£þ£þ£þ£þ£þ°£
¢⁄““¥º∑–µ„±»¬»““ÕÈ∏þ£¨÷˜“™‘≠“Ú « £þ£þ£þ£þ£þ£þ£þ£þ£þ£þ£þ£þ°£
¢€…œÕº «Ω”ÎÕ≠–Œ≥…µƒΩ Ùª•ªØŒÔ∫œΩ£¨À¸µƒªØ—ß Ωø…±Ì 挙£∫£þ£þ£þ£þ£þ£þ£þ£þ°£
¢Ð∫¨Ãº‘¥÷– Ù”⁄∑«º´–‘∑÷◊”µƒ «£þ£þ£þ£®a£Æº◊ÕÈ b£Æ““»≤ c£Æ±Ω d£Æ““¥º£©
¢ðÙðº”ÎÙðºÕ≠»æ¡œ∑÷◊”Ω·ππ»Áœ¬Õº£¨Ã™ðº∑÷◊”÷–µ™‘≠◊”≤…”√µƒ‘”ªØ∑Ω Ω”–£∫£þ£þ£þ£þ£þ£þ£þ£þ°£
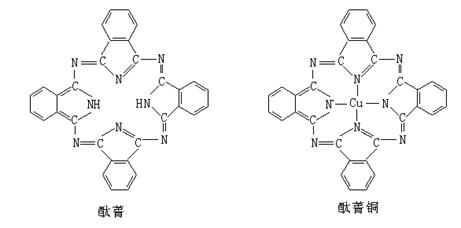
“ª°¢∂˛—°‘ÒÂ¥∞∏
1
2
3
4
5
6
B
D
D
A
C
C
7
8
9
10
11
12
A
C
D
C
D
C
13
14
15
16
17
18
B
C
D
A
D
D
19
20
21
22
23
D
B
C
B
A
»˝°¢
24°¢£®7∑÷£©
(1) H £∫ O £∫ H (1∑÷)
£®2∑÷£©3NO2+H2O=2HNO3+NO
Cl2+H2O=HCl+HClO
2Na2O2+2H2O=4NaOH+O2°¸
25°¢£®6∑÷£©
£®1£© C —ı‘≠◊”Ω·ππ æ“‚Õº £®√øø’1∑÷£©
 £®2£©
Al2(SO4)3 £®1∑÷£© Al3+ +
3H2O
Al(OH)3 +3 H+ £®2∑÷£© ¡ÚÀ·ªÚ—«¡ÚÀ·ªÚúÀ·£®1∑÷£©£®–¥≥ˆ“ª÷÷º¥ø…£¨∫œ¿Ì¥∞∏“≤ø…£©
£®2£©
Al2(SO4)3 £®1∑÷£© Al3+ +
3H2O
Al(OH)3 +3 H+ £®2∑÷£© ¡ÚÀ·ªÚ—«¡ÚÀ·ªÚúÀ·£®1∑÷£©£®–¥≥ˆ“ª÷÷º¥ø…£¨∫œ¿Ì¥∞∏“≤ø…£©
26°¢£®8∑÷£©
£®1£©ºŸ…Ë2£∫»Ð“∫÷–¥Ê‘⁄HCO3-
ºŸ…Ë3£∫»Ð“∫÷–¥Ê‘⁄CO32-∫ÕHCO3-
ºŸ…Ë4£∫»Ð“∫÷–¥Ê‘⁄CO32-∫ÕSO42-
ºŸ…Ë5£∫»Ð“∫÷–¥Ê‘⁄SO42 °¢HCO3- £®À≥–Ú≤ªœÞ°££©£®∏˜1∑÷£©
£®2£©¢Ÿ”√Ω∫Õ∑µŒπл°…Ÿ¡ø»Ð“∫º”»Î ‘πÐ÷–£¨‘Ÿ”√µŒπл°π˝¡øµƒ1mol/L¬»ªØ±µ»Ð“∫≤¢µŒº”µΩ ‘πÐA÷–£¨≥‰∑÷∑¥”¶∫Û£¨æ≤÷√£¨»ª∫Ûπ˝¬À£¨Ω´≥¡µÌ∫Õ¬À“∫∑÷±◊∞»Î¡ÌÕ‚µƒ¡Ω∏ˆ ‘πÐ÷–£®2∑÷£©£ª≤˙…˙∞◊…´≥¡µÌ°£
¢⁄Õ˘◊∞”–≥¡µÌµƒ ‘πÐ÷–º”»Îπ˝¡øµƒ2mol/L—ŒÀ·£ª≥¡µÌ≤ø∑÷»ÐΩ‚«“”–∆¯ÃÂ…˙≥…°£Àµ√˜‘≠»Ð“∫÷–“ª∂®∫¨”–SO42-∫ÕCO32-°£
¢€Õ˘◊∞”–¬À“∫µƒ ‘πÐ÷–º”»Î2mol/L—ŒÀ·£ª≥ˆœ÷ŒÞ…´∆¯Ã£¨Àµ√˜‘≠»Ð“∫÷–∫¨”–HCO3-°£
£®£®√øø’∏˜1∑÷°£∆‰À˚∫œ¿Ì∑Ω∞∏≤Œ’’∏¯∑÷£©
27°¢£®13∑÷£©£®1£©≤ªƒÐ £®1∑÷£© Œ¬∂»∏þ£¨ÀÆŒ™∆¯Ã¨,≤ª¿˚”⁄∞±∆¯µƒ…˙≥… £®2∑÷£©
(2) 25% £®2∑÷£©K= £®1∑÷£© ºı–° ºı–° £®2∑÷£©
(3) C3H3N6 £®2∑÷£©6CO(NH2)2=6NH3+3CO2+C3H6N6 £®2∑÷£©
N C N H H £®1∑÷£©
28°¢£®10∑÷£©
(1) µ⁄Àƒ÷Ð∆⁄£¨µ⁄¢¯◊ £®2∑÷£©
(2) 3Fe3O4+8Al=9Fe+4Al2O3 £®2∑÷£© ”…¿¥“±¡∂ƒ—»€Ω Ù£®∆‰À˚’˝»∑¥∞∏≤Œ’’∏¯∑÷£©£®1∑÷£©
Al2O3+2OH-=2AlO2-+H2O £®2∑÷£©
(3) Cl2+2Fe2+=2Fe3++2Cl- £®1∑÷£© 3SCN-+Fe3+=Fe£®SCN£©3 £®2∑÷£©
29°¢£®15∑÷£©
¢≈¢Ÿ—Ù¿Î◊”Ωªªªƒ§ £®2∑÷£© ¢⁄ 2Cu2++4e-=2Cu 4OH-®D4e-=2H2O+O2 £®∏˜1∑÷£©
£®2£©Cl2+2Br-=Br2+2Cl- £®2∑÷£© BrO3- 5Br- £®∏˜1∑÷£©
∑÷“∫¬©∂∑ …’±≠£®∏˜1∑÷£© ¢⁄ £®1∑÷£©
£®3£©H2S+HDO=HDS+H2O ¢€H2S£®√øø’2∑÷£¨π≤10∑÷£©
30°¢£®15∑÷£©
£®1£©B (1∑÷) µ⁄4÷Ð∆⁄µ⁄IB◊ £®∏˜1∑÷£© 1s22s22P63s23P63d104s1ªÚ[Ar] 3d104s1 (2∑÷) (2) CO2 °¢CCl4 £®∆‰À˚∫œ¿Ì¥∞∏≤Œ’’∏¯∑÷£©(∏˜1∑÷) ∑÷◊”æßà‘≠◊”æßà(∏˜1∑÷) £®3£© 7 1 £®∏˜1∑÷£© £®4£© IIIA IVA £ª b (∏˜1∑÷)
Aµ„À˘ 浃«‚ªØŒÔ «ÀÆ£¨∆‰∑–µ„‘⁄—ı◊‘™Àÿµƒ«‚ªØŒÔ÷–◊Ó∏þ «”…”⁄‘⁄ÀÆ∑÷◊”º‰¥Ê‘⁄◊≈«‚º¸£¨∆‰«ø∂»‘∂¥Û”⁄∑÷◊”º‰◊˜”√¡¶°££®1∑÷£©
31°¢£®15∑÷£©¬‘
(1) £®∏˜1∑÷£©
(2) £®∏˜1∑÷£©
£®3£© £®∏˜2∑÷£©
(4) 3 3:2:2 £®∏˜1∑÷£©
£®5£© £®∏˜1∑÷£©

 w.w.w.k.s.5.u.c.o.m
w.w.w.k.s.5.u.c.o.m
www.ks5u.com
π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com