
ĢāÄæĮŠ±ķ(°üĄØ“š°øŗĶ½āĪö)
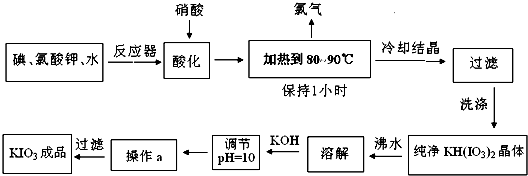
| ĪĀ¶Č | 0 | 10 | 20 | 40 | 60 | 80 |
| KIO3g/100gĖ® | 4.60 | 6.27 | 8.08 | 12.6 | 18.3 | 24.8 |
| KOH g/100gĖ® | 49.2 | 50.8 | 52.8 | 59.8 | 62.4 | 78.6 |
£Ø15·Ö£©Ä³»ÆѧŠĖȤŠ”×éÓĆĻĀĮŠ×°ÖĆ½ųŠŠ”°ÄĘÓė¶žŃõ»ÆĢ¼·“Ó¦”±µÄŹµŃéĢ½¾æ£ØĪ²Ęų“¦Ąķ×°ÖĆŅŃĀŌČ„£©”£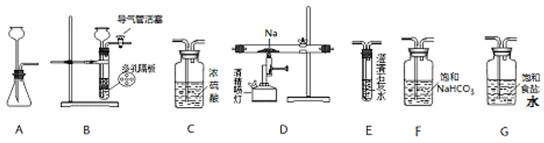
Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©Ń”Ōń±ŲŅŖµÄŅĒĘ÷£¬°“___________________________Ė³ŠņĮ¬½ÓŗĆ×°ÖĆ£ØĢī×°ÖĆŠņŗÅ£©”£
£Ø2£©¼ģŃé×°ÖĆBĘųĆÜŠŌµÄ·½·Ø£ŗ__________________________________”£
£Ø3£©ŹµŃ鏱£¬ŌŚµćČ¼¾Ę¾«ÅēµĘĒ°±ŲŠė½ųŠŠµÄ²Ł×÷ŹĒ______________________£¬“ż×°ÖĆEÖŠ³öĻÖ_____________ĻÖĻóŹ±£¬ŌŁµćČ¼¾Ę¾«ÅēµĘ£¬ŅŌÉĻ²Ł×÷µÄÄæµÄŹĒ___________________”£
£Ø4£©¼ÓČČŅ»¶ĪŹ±¼äŗó¹Ū²ģµ½ÄĘæé±ķĆę±äŗŚ£¬¼ĢŠų¼ÓČČŗó£¬ÄĘČ¼ÉÕ£¬ÓŠ°×ŃĢÉś³É”£Į½ÖÖ²śĪļÖŠÓŠŅ»ÖÖŹĒÖŲŅŖµÄ»Æ¹¤ŌĮĻ£¬ŌŚ²£Į§¹¤ŅµÖŠÓĆĮæŗÜ“ó”£ŌņÄĘÓė¶žŃõ»ÆĢ¼·“Ó¦µÄ»Æѧ·½³ĢŹ½ŹĒ______________”£
£Ø5£©ÉĻŹöŹµŃéÉś³ÉµÄŗŚÉ«ĪļÖŹÓėÅØĮņĖįŌŚŅ»¶ØĢõ¼žĻĀ·“Ó¦»įÉś³ÉŅ»ÖÖ“óĘųĪŪČ¾Īļ£¬æÉĄūÓĆĖįŠŌKMnO4ČÜŅŗĄ“²ā¶ØøĆĘųĢåŌŚæÕĘųÖŠµÄŗ¬Į棬·“Ó¦µÄĄė×Ó·½³ĢŹ½__________________£»ÅŠ¶Ø·“Ó¦ŹĒ·ńŠčŅŖÖøŹ¾¼Į£ØČē¹ūŠčŅŖ£¬Ń”ŌńŗĪÖÖÖøŹ¾¼Į£¬ĒėĆčŹöĻÖĻó”£Čē¹ū²»ŠčŅŖ£¬ĒėĖµĆ÷ĄķÓÉ”££©_______ ____________________________________”£
£Ø15·Ö£©Ä³»ÆѧŠĖȤŠ”×éÓĆĻĀĮŠ×°ÖĆ½ųŠŠ”°ÄĘÓė¶žŃõ»ÆĢ¼·“Ó¦”±µÄŹµŃéĢ½¾æ£ØĪ²Ęų“¦Ąķ×°ÖĆŅŃĀŌČ„£©”£
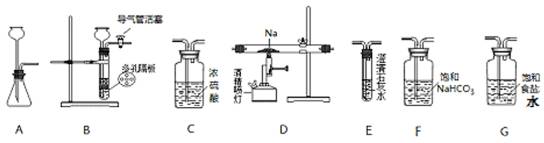
Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©Ń”Ōń±ŲŅŖµÄŅĒĘ÷£¬°“___________________________Ė³ŠņĮ¬½ÓŗĆ×°ÖĆ£ØĢī×°ÖĆŠņŗÅ£©”£
£Ø2£©¼ģŃé×°ÖĆBĘųĆÜŠŌµÄ·½·Ø£ŗ__________________________________”£
£Ø3£©ŹµŃ鏱£¬ŌŚµćČ¼¾Ę¾«ÅēµĘĒ°±ŲŠė½ųŠŠµÄ²Ł×÷ŹĒ______________________£¬“ż×°ÖĆEÖŠ³öĻÖ_____________ĻÖĻóŹ±£¬ŌŁµćČ¼¾Ę¾«ÅēµĘ£¬ŅŌÉĻ²Ł×÷µÄÄæµÄŹĒ___________________”£
£Ø4£©¼ÓČČŅ»¶ĪŹ±¼äŗó¹Ū²ģµ½ÄĘæé±ķĆę±äŗŚ£¬¼ĢŠų¼ÓČČŗó£¬ÄĘČ¼ÉÕ£¬ÓŠ°×ŃĢÉś³É”£Į½ÖÖ²śĪļÖŠÓŠŅ»ÖÖŹĒÖŲŅŖµÄ»Æ¹¤ŌĮĻ£¬ŌŚ²£Į§¹¤ŅµÖŠÓĆĮæŗÜ“ó”£ŌņÄĘÓė¶žŃõ»ÆĢ¼·“Ó¦µÄ»Æѧ·½³ĢŹ½ŹĒ______________”£
£Ø5£©ÉĻŹöŹµŃéÉś³ÉµÄŗŚÉ«ĪļÖŹÓėÅØĮņĖįŌŚŅ»¶ØĢõ¼žĻĀ·“Ó¦»įÉś³ÉŅ»ÖÖ“óĘųĪŪČ¾Īļ£¬æÉĄūÓĆĖįŠŌKMnO4ČÜŅŗĄ“²ā¶ØøĆĘųĢåŌŚæÕĘųÖŠµÄŗ¬Į棬·“Ó¦µÄĄė×Ó·½³ĢŹ½__________________£»ÅŠ¶Ø·“Ó¦ŹĒ·ńŠčŅŖÖøŹ¾¼Į£ØČē¹ūŠčŅŖ£¬Ń”ŌńŗĪÖÖÖøŹ¾¼Į£¬ĒėĆčŹöĻÖĻó”£Čē¹ū²»ŠčŅŖ£¬ĒėĖµĆ÷ĄķÓÉ”££©_______ ____________________________________”£

ĪŖĮĖ¼õÉŁĪĀŹŅĘųĢåÅÅ·Å£¬ÄæĒ°¹¤ŅµÉĻ²ÉÓĆCO2ÓėH2ŌŚ“߻ƼĮ×÷ÓĆĻĀ·“Ó¦ÖʱøÖŲŅŖ»Æ¹¤ŌĮĻCH3OHµÄ¹¤ŅÕ£ŗCO2(g)+3H2(g) CH3OH(g) +H2O(g)”£ĪŖĮĖĢ½¾æĘä·“Ó¦ŌĄķ½ųŠŠČēĻĀŹµŃ飬ŌŚ2LŗćČŻµÄĆܱÕČŻĘ÷ÄŚ250”ęĢõ¼žĻĀ£¬²āµĆn(CO2)Ėꏱ¼äµÄ±ä»ÆĒéæöČēĻĀ±ķ£ŗ
CH3OH(g) +H2O(g)”£ĪŖĮĖĢ½¾æĘä·“Ó¦ŌĄķ½ųŠŠČēĻĀŹµŃ飬ŌŚ2LŗćČŻµÄĆܱÕČŻĘ÷ÄŚ250”ęĢõ¼žĻĀ£¬²āµĆn(CO2)Ėꏱ¼äµÄ±ä»ÆĒéæöČēĻĀ±ķ£ŗ
| Ź±¼ä£Øs£© | 0 | 1 | 2 | 3 | 4 | 5 |
| n(CO2)(mol) | 0.40 | 0.35 | 0.31 | 0.30 | 0.30 | 0.30 |
¹ś¼ŹŃ§Š£ÓÅŃ” - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com