
题目列表(包括答案和解析)
反应物Ⅰ | 反应物Ⅱ | 反应现象 | 说明 |
AgNO3溶液 | NaCl溶液 | 生成白色沉淀 | 该沉淀为AgCl,不溶于稀硝酸 |
BaCl2溶液 | Na2SO4溶液 | 生成白色沉淀 | 该沉淀为BaSO4,不溶于稀盐酸 |
Na2CO3溶液 | __________ | 生成白色沉淀 | 该沉淀为__________,溶于稀盐酸 |
由蒸发海水制得的粗盐中常含有Na2SO4、CaCl2和MgCl2等杂质,在食盐生产过程中需要将这些杂质除去。请回答:
(1)Na2SO4、CaCl2和MgCl2在溶液里能形成Na+、Ca2+、Mg2+、![]() 和Cl-五种离子。要除去其中的Mg2+,可使用氢氧化钠溶液;除去其中的
和Cl-五种离子。要除去其中的Mg2+,可使用氢氧化钠溶液;除去其中的![]() ,可使用____________________溶液;除去其中的Ca2+,可使用____________________溶液。
,可使用____________________溶液;除去其中的Ca2+,可使用____________________溶液。
(2)在食盐生产的除杂过程中,会带进![]() 和OH-。要同时除去这两种杂质离子,最简便的方法是加入适量的,并用______________________测定溶液的酸碱性。
和OH-。要同时除去这两种杂质离子,最简便的方法是加入适量的,并用______________________测定溶液的酸碱性。
(6分)合成气经压缩升温后进入10m3甲醇合成塔,在催化剂作用下,进行甲醇合成,主要反应是:2H2(g) + CO(g)  CH3OH(g) △H =-181.6kJ·mol-1。T4℃下此反应的平衡常数为160。此温度下,在密闭容器中加入CO、H2,反应到某时刻测得各组分的浓度如下:
CH3OH(g) △H =-181.6kJ·mol-1。T4℃下此反应的平衡常数为160。此温度下,在密闭容器中加入CO、H2,反应到某时刻测得各组分的浓度如下:
| 物质 | H2 | CO | CH3OH |
| 浓度/(mol·L-1) | 0.2 | 0.1 | 0.4 |
(6分)合成气经压缩升温后进入10m3甲醇合成塔,在催化剂作用下,进行甲醇合成,主要反应是:2H2(g)
+ CO(g)  CH3OH(g)
△H =-181.6kJ·mol-1。T4℃下此反应的平衡常数为160。此温度下,在密闭容器中加入CO、H2,反应到某时刻测得各组分的浓度如下:
CH3OH(g)
△H =-181.6kJ·mol-1。T4℃下此反应的平衡常数为160。此温度下,在密闭容器中加入CO、H2,反应到某时刻测得各组分的浓度如下:
|
物质 |
H2 |
CO |
CH3OH |
|
浓度/(mol·L-1) |
0.2 |
0.1 |
0.4 |
⑴ 比较此时正、逆反应速率的大小:v正 v逆 (填“>”、“<”或“=”)。
⑵ 若加入同样多的CO、H2,在T5℃反应,10 min后达到平衡,此时c(H2)=0.4 mol·L-1,则该时间内反应速率v(CH3OH) = mol·(L·min)-1。
⑶ 生产过程中,合成气要进行循环,其目的是 。
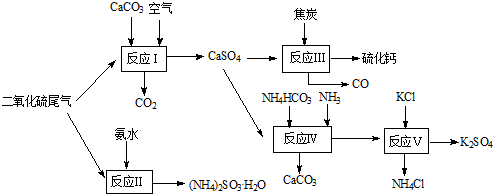
(1)该厂生产过程中涉及的物质有:①石灰石 ②纯碱 ③小苏打 ④烧碱 ⑤CO2⑥消石灰。下列叙述中正确的是( )
A.起始原料是①② B.起始原料是②⑥
C.最终产品是④⑤ D.最终产品是③④
(2)该厂生产过程中的优点可能有( )
①排放的气体对大气无污染 ②生产过程中的部分产品可作为起始原料作用 ③无高温作业
A.只有① B.只有② C.①和④ D.②和③
(3)生产过程中没有涉及到的化学反应类型是( )
A.分解反应 B.化合反应 C.复分解反应 D.置换反应
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com