
题目列表(包括答案和解析)
化学能与电能之间的相互转化与人的生活实际密切相关,在生产、生活中有重要的应用,同时也是学生形成化学学科素养的重要组成部分。
(1)熔融状态下,钠的单质和氯化亚铁能组成可充电电池(如图1),反应原理为:2Na+FeCl2 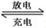 Fe+2NaCl,该电池放电时,正极反应式为 ________________ _____:
Fe+2NaCl,该电池放电时,正极反应式为 ________________ _____:
充电时,__________(写物质名称)电极接电源的负极;
该电池的电解质为________ _。
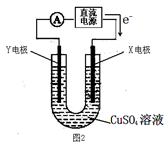
(2)某同学用铜片、石墨作电极电解一定浓度的硫酸铜溶液(如图2),一段时间停止通电取出电极。若在电解后的溶液中加入0.98g氢氧化铜粉末恰好完全溶解,经测定所得溶液与电解前完全相同。请回答下列问题:
①Y电极材料是 ,发生 (填“氧化或还原”)反应。
②电解过程中X电极上发生的电极反方应式是:
③如在电解后的溶液中加入足量的小苏打,充分反应后产生气体在标准状况下所占的体积是
(3)常温时,BaSO4的Ksp=1.08×10-10,现将等体积的BaCl2溶液与2.0×10-3mol/l的Na2SO4
溶液混合。若要生成BaSO4沉淀,BaCl2溶液的最小浓度为______________。
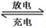 Fe+2NaCl,该电池放电时,正极反应式为 ________________ _____:
Fe+2NaCl,该电池放电时,正极反应式为 ________________ _____: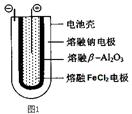
有些化学反应的化学能能直接转化成电能
I.利用 Fe + CuSO4 = FeSO4 + Cu反应,设计一个原电池:
(1)在下框中画出装置图(标明电解质溶液、正、负极和电极材料)

(2)下列说法中,正确的是 。(填字母)
A.电解质溶液中阳离子向负极移动 B.电子通过外导线由负极流向正极
C.当导线中有1mol电子通过时,理论上正极放出1g气体
D.若所选电极的质量相等,理论上两极质量差为60g,导线中有1 mol电子通过
II.三套装置如下图所示, A、B、C烧杯中分别盛有相同物质的量浓度的稀硫酸。
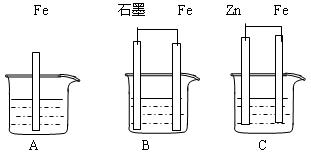
(1)比较A、B、C中铁被腐蚀的速率,由快到慢的顺序为 ;
(2)若C中电解质溶液是氯化钠溶液,则Fe电极的电极反应式为 ;
III.目前常用的镍(Ni)镉(Cd)电池,其电池总反应可以表示为:
![]()
已知Ni(OH)2和Cd(OH)2均难溶于水但能溶于酸。
(1)以下说法中正确的是
①以上反应是可逆反应 ②以上反应不是可逆反应
③充电时化学能转变为电能 ④放电时化学能转变为电能
(2)废弃的镍镉电池已成为重要的环境污染物,资料表明一节废镍镉电池可以使一平方米面积的耕地失去作用价值。在酸性土壤中这种污染特别严重,这是因为
(3)另一种常用的电池是锂电池,锂是一种碱金属元素,其相对原子质量为7,由于它的比容量(单位质量电极材料所能转换的电量)特别大而广泛应用于心脏起搏器,一般使用时间可长达十年,它的负极用金属锂制成,电池总反应可表示为Li+ MnO2 = LiMnO2。
锂电池中的电解质溶液需用非水溶剂配制,为什么这种电池不能使用电解质的水溶液(请用化学方程式表示其原因) 。
(14分)某中学化学课外活动小组欲探究铁在氯气中燃烧产物的成份、性质和用途,设计了如下实验步骤:
(1)用下列实验装置制取干燥纯净的氯气
①制备并收集得到干燥纯净的氯气,上述各装置按气流从左到右方向连接顺序为
(填仪器接口的字母编号)
②该实验还存在不足之处,应如何改进?
(2)某同学将一定量铁粉与Cl2恰好完全反应得到一固体物质a,然后通过实验确定其成分。探究过程如下:
①提出假设:(请把下列假设补充完整)
假设①:该固体物质是FeCl3;假设②: ;假设③: 。
②设计实验方案:
取少量固体物质a于烧杯中,加适量水溶解,然后取两份a溶液分别进行实验,实验现象与结论如下表,请在表格内的横线处填空。
| 实验方法 | 实验现象 | 结论 |
| 在溶液中加 KSCN溶液 | | 固体物质中有FeCl3 |
| 向a溶液中滴加 酸性KMnO4溶液 | KMnO4溶液紫色 不褪色 | 固体物质中不含______ |

(14分)某中学化学课外活动小组欲探究铁在氯气中燃烧产物的成份、性质和用途,设计了如下实验步骤:
(1)用下列实验装置制取干燥纯净的氯气
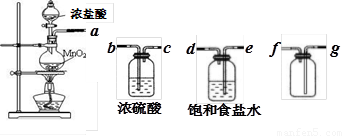
①制备并收集得到干燥纯净的氯气,上述各装置按气流从左到右方向连接顺序为
(填仪器接口的字母编号)
②该实验还存在不足之处,应如何改进?
(2)某同学将一定量铁粉与Cl2恰好完全反应得到一固体物质a,然后通过实验确定其成分。探究过程如下:
①提出假设:(请把下列假设补充完整)
假设①:该固体物质是FeCl3;假设②: ;假设③: 。
②设计实验方案:
取少量固体物质a于烧杯中,加适量水溶解,然后取两份a溶液分别进行实验,实验现象与结论如下表,请在表格内的横线处填空。
|
实验方法 |
实验现象 |
结论 |
|
在溶液中加 KSCN溶液 |
|
固体物质中有FeCl3 |
|
向a溶液中滴加 酸性KMnO4溶液 |
KMnO4溶液紫色 不褪色 |
固体物质中不含______ |
由此得出结论:假设 成立(填序号①②③)。
(3)为进一步探究物质a的性质,他们又利用a溶液做了如下一些实验,其中现象、结论均正确的是_____________(填写序号)
A.向氢氧化镁悬浊液中滴加a溶液出现红褐色沉淀,证明Fe(OH)3溶解度小于Mg(OH)2溶解度
B.向a溶液中加入少量铁粉,铁粉溶解,溶液颜色由浅绿色变成黄色
C.向沸水中滴加a的饱和溶液,立即出现红褐色沉淀
D.将a溶液加热蒸干并灼烧,得到Fe2O3固体
(4)a溶液常作印刷电路铜板的腐蚀剂,得到含有Cu2+等的废液,有人提出可以利用如右图的装置从得到的废液中提炼金属铜。该过程中甲池负极的电极反应式是 ,若乙池中装入废液500mL,当阴极增重3.2g时,停止通电,此时阳极产生气体的体积
(标准状况)为 (假设气体全部逸出)。

题号
1
2
3
4
5
6
7
8
9
10
11
12
13
14
答案
B
D
A
A
C
D
B
D
B
B
AC
AD
BC
C
15.(10分,每空2分)
(1)过滤(洗涤) ; 蒸发浓缩、冷却结晶,过滤
(2)连接好装置,从漏斗向量气筒内注入一定量的水,移动漏斗使左、右两侧形成液面高度差。静置后,液面高度不再变化,即表明气密性良好。(其他合理方法均给分)
16.(8分)(1)Al
(2)1.204×1024(或2NA)(2分)
(3)4NH3+5O2 4NO+6H2O(2分)
4NO+6H2O(2分)
(4)AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-(2分);
 17.(10分,每空2分) (1)HC2O4-+ OH―= C2O42-+ H2O (2)>
17.(10分,每空2分) (1)HC2O4-+ OH―= C2O42-+ H2O (2)>
(3)H2C2O4 CO↑+CO2↑+H2O
(4)温度过低反应速率缓慢;温度过高时,H2C2O4在酸性溶液中会部分分解。(每个点1分 共2分)
(5)C
18.(10分)(1)保护臭氧层(1分)
(3)A(2分)
②CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH=-49.47kJ•mol-1(2分)
CH3OH(g)+H2O(g) ΔH=-49.47kJ•mol-1(2分)

 (5)B或D(B、D都选给分)(1分)
(5)B或D(B、D都选给分)(1分)
19.(12分,每空2分)
 (1)反应①:加成反应;反应④:取代反应(2) A:CH3CCN; G:
(1)反应①:加成反应;反应④:取代反应(2) A:CH3CCN; G:
(3)B→C;CH3CCOOH CH2=CCOOH+H2O
 |
 |
||||
 |
|||||

|