
题目列表(包括答案和解析)
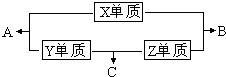 X、Y、Z、M三种短周期元素,其中X、Y、Z的原子序数之和为16,X、Y、Z三种元素的常见单质在常温常压下都是无色气体,在适当的条件下可以发生如下图所示的变化:
X、Y、Z、M三种短周期元素,其中X、Y、Z的原子序数之和为16,X、Y、Z三种元素的常见单质在常温常压下都是无色气体,在适当的条件下可以发生如下图所示的变化:
| ||
| △ |
| ||
| △ |
| 加热 |
| 加热 |
(14分)“低碳循环”引起各国的高度重视,而如何降低大气中CO2的含量及有效地开发利用CO2,引起了全世界的普遍重视。所以“低碳经济”正成为科学家研究的主要课题
(1)用电弧法合成的储氢纳米碳管常伴有大量的碳纳米颗粒(杂质),这种颗粒可用如下氧化法提纯,请完成该反应的化学方程式:(系数按顺序填在答题卷上)
___ C+ ___ KMnO4+ ____ H2SO4 = ____CO2↑+ ____MnSO4 + ____K2SO4+ ____H2O
(2)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应
CO(g)+H2O(g)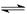 CO2(g)+H2(g),得到如下三组数据:
CO2(g)+H2(g),得到如下三组数据:
|
实验组 |
温度℃ |
起始量/mol |
平衡量/mol |
达到平衡所需时间/min |
||
|
CO |
H2O |
H2 |
CO |
|||
|
1 |
650 |
4 |
2 |
1.6 |
2.4 |
6 |
|
2 |
900 |
2 |
1 |
0.4 |
1.6 |
3 |
|
3 |
900 |
a |
b |
c |
d |
t |
①实验1中以v (CO2) 表示的反应速率为 (取小数点后二位,下同)。
②该反应为 (填“吸”或“放”)热反应,实验2条件下平衡常数K= 。
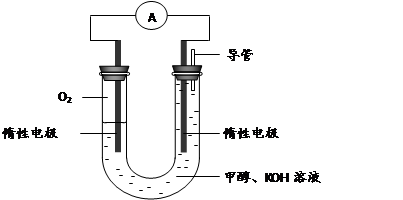
(3) 某实验小组依据甲醇燃烧的反应原理,设计如下图所示的电池装置。
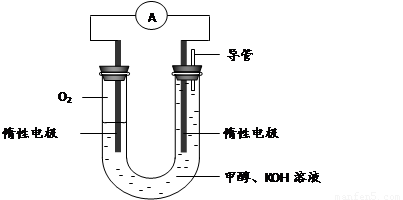
①该电池正极的电极反应为 。
② 工作一段时间后,测得溶液的pH减小,该电池总反应的化学方程式为 。
⑷CO2在自然界循环时可与CaCO3反应,CaCO3是一种难溶物质,其Ksp=2.8×10—9。CaCl2溶液与Na2CO3溶液混合可形成CaCO3沉淀,现将等体积的CaCl2溶液与Na2CO3溶液混合,若Na2CO3溶液的浓度为2×10—4mo1/L ,则生成沉淀所需CaCl2溶液的最小浓度为 。
(14分)“低碳循环”引起各国的高度重视,而如何降低大气中CO2的含量及有效地开发利用CO2,引起了全世界的普遍重视。所以“低碳经济”正成为科学家研究的主要课题
(1)用电弧法合成的储氢纳米碳管常伴有大量的碳纳米颗粒(杂质),这种颗粒可用如下氧化法提纯,请完成该反应的化学方程式:(系数按顺序填在答题卷上)
___ C+ ___ KMnO4+ ____ H2SO4 = ____CO2↑+ ____MnSO4 + ____K2SO4+ ____H2O
(2)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应
CO(g)+H2O(g)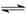 CO2(g)+H2(g),得到如下三组数据:
CO2(g)+H2(g),得到如下三组数据:
| 实验组 | 温度℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
| CO | H2O | H2 | CO | |||
| 1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
| 2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
| 3 | 900 | a | b | c | d | t |
 X、Y、Z、M三种短周期元素,其中X、Y、Z的原子序数之和为16,X、Y、Z三种元素的常见单质在常温常压下都是无色气体,在适当的条件下可以发生如下图所示的变化:
X、Y、Z、M三种短周期元素,其中X、Y、Z的原子序数之和为16,X、Y、Z三种元素的常见单质在常温常压下都是无色气体,在适当的条件下可以发生如下图所示的变化:(08龙岩一中三模)(15分)我国第二代身份证采用的是具有绿色环保性能的PETG新材料,PETG新材料可以回收再利用,而且对周边环境不构成任何污染。PETG的结构简式如下:

这种材料可采用如下图所示的合成路线

(1) ![]()
(2)RCOORl+R2OH→RCOOR2+R1OH(R、R1、R2表示烃)
试回答下列问题:
(1)反应②④加入的试剂X是______________________
(2)⑦的反应类型是______________________
(3)写出结构简式:B ____________________、I ____________________
(4)合成时应控制的单体的物质的量
n(D)∶n(E)∶n(H)= _____∶______∶______(用m、n表示)
(5)写出化学方程式:
反应②: ;
反应⑤: 。
选择题答案表:
题号
1
2
3
4
5
6
7
8
答案
A
C
A
C
C
A
D
D
题号
9
10
11
12
13
14
答案
B
AD
C
D
BD
AD
15、(12分)Ⅰ(4分)①②④⑥
Ⅱ(8分)⑴用冰水冷却有利于析出更多的晶体,黑暗可以防止晶体分解(2分)
⑵过滤、洗涤(1分)
⑶100mL容量瓶、酸式滴定管(2分) (紫)红(1分) ⑷3 (2分)
 16、(8分(1)NaClO(1分)(2)
16、(8分(1)NaClO(1分)(2) (1分)
(1分)
(3)2NaCl +2H2O
 H2↑+ Cl2↑+2NaOH (2分) 氯碱工业(1分)
H2↑+ Cl2↑+2NaOH (2分) 氯碱工业(1分)
(4)2Fe3+ + 3ClO? + 10OH? = 2FeO42? + 3Cl? + 5H2O(2分)
②本身被还原成Fe3+而发生水解生成Fe(OH)3胶体吸附水中杂质以达到净化水的目的。(1分)
17、(10分)(1)FeSO4?7H2O (写FeSO4晶体也给分)
(2)防止Fe2+氧化; 取副产品甲少许溶于水,滴加适量KSCN溶液,观察溶液是否变为血红色。
(3)稀盐酸(或稀硫酸等) (4)TiO2  Ti+O2↑
(每空2分,共10分)
Ti+O2↑
(每空2分,共10分)
18、(10分)⑴2NO3-+5Mg+6H2O==N2↑+5Mg(OH)2+2OH-(2分)
⑵①快速方便易行(2分,相近合理答案也给分)
②空白对照实验(2分,相近合理答案也给分)
③将水样先稀释一定倍数后再重复实验(2分)
⑶ 800 (2分)
19、(12分)(1)加成 (1分)(2)13(2分)
(3)(4分) (4)(5分)
(4)(5分)

20、(10分)⑴ 0.01 mol?L-1(2分) 不变(1分)
⑵ <(2分)
⑶ 设焙烧炉中消耗空气的物质的量为5x,鼓风炉中消耗空气物质的量为5y,则:
 Zn(g)+CO2(g)
Zn(g)+CO2(g)
y 2y 1mol 2y×62.5% 1mol
2y×62.5%=1mol y=0.8mol 5y=4mol(2分)
2ZnS + 3O2 = 2ZnO + 2SO2 △n
2mol 1mol
1mol 0.5mol
4x/(5x-0.5mol)=82.5% x=3.3mol 5x=16.5mol(2分)
5x+5y=4mol+16.5mol=20.5mol
V(空气)=20.5×
 21、(12分)
21、(12分)
(1)CD(2分) (2) H3AsO4(1分);第四周期元素,原子核外只有四个电子层。按能量最低原理,4s上排2个电子,3d上排10个电子,4p上排6个电子,共对应18种元素,若4d排电子,就出现了第五电子层,就不是第四周期元素了,所以第四周期只有18种元素。(2分) (2)+3(1分);正四面体(1分);3d74s2(1分) (3)BC(2分)
(4)N2O或CO2或CS2或BeCl2;SCN-或OCN-(2分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com