
题目列表(包括答案和解析)
|
在一个密闭容器中盛有N2和H2,它们的起始浓度分别是1.8 mol/L和5.4 mol/L,在一定的条件下它们反应生成NH3,10 min后测得N2的浓度是0.8 mol/L,则在这10 min内NH3的平均反应速率是 | |
| [ ] | |
A. |
0.1 mol/(L·min) |
B. |
0.2 mol/(L·min) |
C. |
0.3 mol/(L·min) |
D. |
0.6 mol/(L·min) |
在一个密闭容器中盛有N2和H2,它们的起始浓度分别是1.8 mol /L和5.4 mol /L,在一定的条件下它们反应生成NH3,10 min后测得N2的浓度是0.8 mol /L,则在这10 min内用NH3来表示的平均反应速率是
A.0.1 mol /(L·min) B.0.2 mol /(L·min)
C.0.3 mol /(L·min) D.0.6 mol /(L·min)
在一个密闭容器中盛有N2和H2,它们的起始浓度分别是1.8 mol /L和5.4 mol /L,在一定的条件下它们反应生成NH3,10 min后测得N2的浓度是0.8 mol /L,则在这10 min内用NH3来表示的平均反应速率是( )
A.0.1 mol /(L·min) B.0.2 mol /(L·min)
C.0.3 mol /(L·min) D.0.6 mol /(L·min)
在一个密闭容器中盛有N2和H2,它们的起始浓度分别是1.8 mol /L和5.4 mol /L,在一定的条件下它们反应生成NH3,10 min后测得N2的浓度是0.8 mol /L,则在这10 min内用NH3来表示的平均反应速率是
A.0.1 mol /(L·min) B.0.2 mol /(L·min)
C.0.3 mol /(L·min) D.0.6 mol /(L·min)
在体积为l L的密闭容器中,充入lmol CO2和3mol H2,一定条件下发生反应:
CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g) + 49.0 kJ
CH3OH(g)+H2O(g) + 49.0 kJ
测得CO2和CH3OH(g)的浓度随时间变化如图所示:
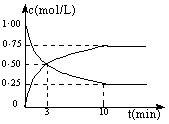
(1)从反应开始到第10 min,氢气的平均反应速率v(H2)= ,在这段时间内,反应放出的热量=
(2)在该条件下,反应的平衡常数K的值 = (保留2位小数),如果在某一时刻保持温度不变,只改变浓度,使c(CO2) =1.00 mol/L,c(H2) = 0.40 mol/L,c(CH3OH) = c(H2O) = 0.80 mol/L,则平衡 (填写序号)。
a.向正反应方向移动 b.向逆反应方向移动
c.不移动 d.无法确定平衡移动方向
(3)下列措施中能使n(CH3OH)/n(CO2)增大的是 (填写序号)。
a.升高温度 b.充入He(g),使体系压强增大
c.将H2O(g)从体系中分离 d.再充入l mol CH3OH(g)
(4)在催化剂的作用下,CO2与H2能够合成许多物质,如甲醇.烃类.二甲醚等,但反应体系中混入杂质,则反应很难进行,可能的原因是 。
1.D 2.A 3.A 4.C 5.C 6.AC 7.D 8.D 9.BD 10.AB 11.B
12.D 13.B 14.B 15.A 16.B 17.B 18.B 19.A 20.B 21.C 22.D
23.(1)< (2)右侧的3处
(3)< B相当于减压了,减压后平衡向 分解的方向移动,使B中
分解的方向移动,使B中 的量减少了.
的量减少了.
24.①提高,降低;②b=4;③ ;④
;④ 或
或 或ac+bc=ab
或ac+bc=ab
25.(1)B.根据反应:

 ,
,

 ,若要充分利用原料,显然要求原料与
,若要充分利用原料,显然要求原料与 反应产生的
反应产生的 和
和 物质的量之比等于或接近于3∶1,上述反应趋于恰好反应,原料得以充分利用.
物质的量之比等于或接近于3∶1,上述反应趋于恰好反应,原料得以充分利用. w.w.w.k.s.5.u.c.o.m
w.w.w.k.s.5.u.c.o.m




(2)①

 ②不合理.因为BiOCl中,Cl的化合价为-1价.③浓NaOH溶液中,
②不合理.因为BiOCl中,Cl的化合价为-1价.③浓NaOH溶液中, 抑制
抑制 的溶解,使
的溶解,使 的浓度减小,盐酸中
的浓度减小,盐酸中 抑制
抑制 的水解.
的水解.
26.(1)2、1、3、2 (2)A为气态,B为固态或气态,D为气态 (3)放热
27.(1)按1分钟计,生成0.5 mol C产生热量45 kJ,而容器散热
 ,所以应用加热器每分钟提供热量120
kJ-45 kJ=75 kJ
,所以应用加热器每分钟提供热量120
kJ-45 kJ=75 kJ
(2)容器半径和高度都变为原来10倍,则表面变为原来1000倍,平均每分钟生成C为0.5 mol×1000=500 mol,放出热量45000kJ,而容器散热12000 kJ,所以冷却器每分钟吸收热量45000 kJ-12000 kJ=33000 kJ
(3)不变
28.a=1 b=2
29.(1) (2)1/10500 (3)10
(2)1/10500 (3)10
30.①39% ②12.5% 31.(1)① 体积
体积
②当活塞由C向B移动时,因体积扩大使平衡:

 向体积扩大方向移动以至混合气体物质的量增大.增大的物质的量可由下式求出
向体积扩大方向移动以至混合气体物质的量增大.增大的物质的量可由下式求出



起始:0.08 mol 0
平衡:

因平衡时混合气体总的物质的量为0.07 mol,由于活塞由C移至B,体积扩大,故 ,可知充入
,可知充入 物质的量必小于0.01
mol
(2)
物质的量必小于0.01
mol
(2)
 www.ks5u.com
www.ks5u.com
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com