
äãá¢êÅÝÚ(¯■â´ÇÞ¯¡¤ë§ãö—)
§þÆÅØ£ñÇÆÎaA+bB![]() C,åÖ25 ÀÌòÝȘ§¨AÀÂBàÉؤ¯Çý£ë˜é´Ñࣚ¤üȘçûüôêÅòçîÕò»ƒï,ñøö—Øåüôò»ƒïȘúµ°—aÀÂbçáøçÀÈ
C,åÖ25 ÀÌòÝȘ§¨AÀÂBàÉؤ¯Çý£ë˜é´Ñࣚ¤üȘçûüôêÅòçîÕò»ƒï,ñøö—Øåüôò»ƒïȘúµ°—aÀÂbçáøçÀÈ
Açáé´Ñà/molÀÊL-1 | Bçáé´Ñà/molÀÊL-1 | ñÇÆÎùìôò/ molÀÊ(LÀÊs)-1 |
1.0 | 1.0 | 1.2Àê10-2 |
1.0 | 4.0 | 1.92Àê10-2 |
4.0 | 1.0 | 4.8Àê10-2 |
ƒÙ¿»°ÊóÖò祪Șàùûúæɧð—ñÇÆÎùìôò¤ëñÇÆÎöÿé´ÑàøÛ¥ðÇÌåÖѴꢿÄüçȤ¤ÐöôüôȘÑ奷çËñÇÆÎâÇùçȘ£₤îÏñÇÆÎùìôòë˜ñÇÆÎöÿé´Ñàçáñ§Çöçá°ù£»°èí»ÝàÈ´ñÇÆÎöÿé´Ñàçáñ§ÇöçàÆÖ£₤îÏñ§°äò§øÅ¡¼öÿøòçá£₤îÏ¥óê¢ò»ÈˋÀÈàÓÑåÆÖñÇÆÎmA+nB?ïæCâÇùçȘv=kÈÜcÈ´AÈˋÈïmÈÜcÈ´BÈˋÈïnȘóðøÅköˆ°Èò»ÀÈ
§þÆÅØ£ñÇÆÎȤaA+bB CȘåÖ25ÀÌòÝȘ§¨AÀÂBàÉؤ¯Çý£ë˜é´Ñࣚ¤üȘçûç§üôêÅòçîÕò»ƒïȤȴ¥«üôÝÚÈˋ
CȘåÖ25ÀÌòÝȘ§¨AÀÂBàÉؤ¯Çý£ë˜é´Ñࣚ¤üȘçûç§üôêÅòçîÕò»ƒïȤȴ¥«üôÝÚÈˋ
ñøö—Øåèüò»ƒïȘúµaÀÂbçáøçÀÈ
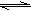 CâÇùçȘv=kcmÈ´AÈˋcnÈ´BÈˋȘóðøÅköˆ°Èò»ÀÈ
CâÇùçȘv=kcmÈ´AÈˋcnÈ´BÈˋȘóðøÅköˆ°Èò»ÀÈ CȘåÖ25ÀÌòÝȘ§¨AÀÂBàÉؤ¯Çý£ë˜é´Ñࣚ¤üȘçûç§üôêÅòçîÕò»ƒïÈ´¥«üôÝÚÈˋȤ
CȘåÖ25ÀÌòÝȘ§¨AÀÂBàÉؤ¯Çý£ë˜é´Ñࣚ¤üȘçûç§üôêÅòçîÕò»ƒïÈ´¥«üôÝÚÈˋȤ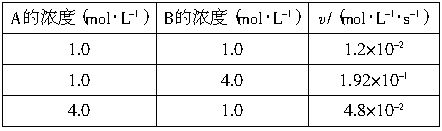
 ȘóðøÅköˆ°Èò»ÀȧþÆÅØ£ñÇÆÎaAȨbBȧCȘåÖ25ÀÌòÝȘ§¨AÀÂBàÉؤ¯Çý£ë˜é´Ñࣚ¤üȘçûüôêÅòçîÕò»ƒï
ȘóðøÅköˆ°Èò»ÀȧþÆÅØ£ñÇÆÎaAȨbBȧCȘåÖ25ÀÌòÝȘ§¨AÀÂBàÉؤ¯Çý£ë˜é´Ñࣚ¤üȘçûüôêÅòçîÕò»ƒï
ƒÙ¿»°ÊóÖò祪Șàùûúæɧð—ñÇÆÎùìôò¤ëñÇÆÎöÿé´Ñà¥ðѴꢿÄüçȤåÖ¤ÐöôüôȘÑ奷çËñÇÆÎâÇùçȘ£₤îÏñÇÆÎùìôòë˜ñÇÆÎöÿé´Ñàñ§Çö°ù£»°èí»Ýà(ñÇÆÎöÿé´Ñàçáñ§ÇöçàÆÖñÇÆÎò§øÅ¡¼ñøæÆò§ú¯çá¥óê¢ò»)ÈÛàÓÑåÆÖñÇÆÎò§mAȨnB![]() CñÇÆÎȘvȧk[A]mÀÊ[B]nȘóðøÅköˆ°Èò»ÈÛ
CñÇÆÎȘvȧk[A]mÀÊ[B]nȘóðøÅköˆ°Èò»ÈÛ
§þÆÅØ£ñÇÆÎaAȨbB![]() CȘåÖ25ÀÌòÝȘ§¨AÀÂBàÉؤ¯Çý£ë˜é´Ñࣚ¤üȘçûüôêÅòçîÕò»ƒïȤ
CȘåÖ25ÀÌòÝȘ§¨AÀÂBàÉؤ¯Çý£ë˜é´Ñࣚ¤üȘçûüôêÅòçîÕò»ƒïȤ

ñøö—Øåèüò»ƒïȘúµ°—aÀÂbçáøçÈÛ
1ÈÛDÀÀ2ÈÛAÀÀ3ÈÛAÀÀ4ÈÛCÀÀ5ÈÛCÀÀ6ÈÛACÀÀ7ÈÛDÀÀ8ÈÛDÀÀ9ÈÛBDÀÀ10ÈÛABÀÀ11ÈÛBÀÀ
12ÈÛDÀÀ13ÈÛBÀÀ14ÈÛBÀÀ15ÈÛAÀÀ16ÈÛBÀÀ17ÈÛBÀÀ18ÈÛBÀÀ19ÈÛAÀÀ20ÈÛBÀÀ21ÈÛCÀÀ22ÈÛD
ÀÀÀÀ23ÈÛÈ´1ÈˋÈ¥ÀÀÈ´2ÈˋÆØýÁçá3ÇÎ
ÀÀÀÀÈ´3ÈˋÈ¥ÀÀBüÁçÝÆÖ¥¾î¿êùȘ¥¾î¿¤µó§¤ãü· ñø§ãçáñ§ü·ØóÑ₤Șò¿BøÅ
ñø§ãçáñ§ü·ØóÑ₤Șò¿BøÅ çáꢥ¾èìêùÈÛ
çáꢥ¾èìêùÈÛ
ÀÀÀÀ24ÈÛÂìäáÔȘ§ççëÈ£ÂÖbȧ4È£ÂÜ È£ÂÉ
È£ÂÉ £·
£· £·acȨbcȧab
£·acȨbcȧab
ÀÀÀÀ25ÈÛÈ´1ÈˋBÈÛ¡ªƒïñÇÆÎȤ

 Ș
Ș

 Șà¶Øˆ°ðñøâ«ÆûåÙêüȘüåà£ØˆúµåÙêüÆŠ
Șà¶Øˆ°ðñøâ«ÆûåÙêüȘüåà£ØˆúµåÙêüÆŠ ñÇÆÎýºèºçá
ñÇÆÎýºèºçá ¤ë
¤ë öÿøòçáê¢øÛÝàçàÆÖ£·§Æ§■ÆÖ3Àû1Șèüò—ñÇÆÎú¼ÆÖúÀ¤ûñÇÆÎȘåÙêüçûØå°ðñøâ«ÆûÈÛ
öÿøòçáê¢øÛÝàçàÆÖ£·§Æ§■ÆÖ3Àû1Șèüò—ñÇÆÎú¼ÆÖúÀ¤ûñÇÆÎȘåÙêüçûØå°ðñøâ«ÆûÈÛ w.w.w.k.s.5.u.c.o.m
w.w.w.k.s.5.u.c.o.m
ÀÀÀÀ ÀÀÀÀ
ÀÀÀÀ
ÀÀÀÀ ÀÀÀÀ
ÀÀÀÀ
ÀÀÀÀÈ´2ÈˋÂì

 ÀÀÂÖý£¤üâÚÈÛØ·öˆBiOCløÅȘClçá£₤¤ü¥Üöˆ-1¥ÜÈÛÂÜé´NaOHàÉؤøÅȘ
ÀÀÂÖý£¤üâÚÈÛØ·öˆBiOCløÅȘClçá£₤¤ü¥Üöˆ-1¥ÜÈÛÂÜé´NaOHàÉؤøÅȘ Øøøó
Øøøó çáàɧãȘò¿
çáàɧãȘò¿ çáé´ÑॾÅÀȘîöùÃøÅ
çáé´ÑॾÅÀȘîöùÃøÅ Øøøó
Øøøó çáùÛ§ãÈÛ
çáùÛ§ãÈÛ
ÀÀÀÀ26ÈÛÈ´1Èˋ2ÀÂ1ÀÂ3ÀÂ2ÀÀÈ´2ÈˋAöˆó½ä˜È˜Böˆ¿ä䘣·ó½ä˜È˜Döˆó½ä˜ÀÀÈ´3Èˋñéàà
ÀÀÀÀ27ÈÛÈ´1Èˋ¯Ç1ñøøÆ¥óȘ躰è0.5 mol Cýºèºààê¢45 kJȘѽàïó¼èÂàà
 ȘùªØåÆÎÆû¥Æààó¼û¢ñøøÆäÿˋààê¢120
kJ-45 kJȧ75 kJ
ȘùªØåÆÎÆû¥Æààó¼û¢ñøøÆäÿˋààê¢120
kJ-45 kJȧ75 kJ
ÀÀÀÀÈ´2Èˋàï󼯊ƒÑ¤ë¡ÔÑàÑ¥ÝðöˆåÙâÇ10ÝÑȘå·ÝÚûÌÝðöˆåÙâÇ1000ÝÑȘ󧃪û¢ñøøÆ躰èCöˆ0.5 molÀê1000ȧ500 molȘñé°—ààê¢45000kJȘѽàïó¼èÂàà12000 kJȘùªØåâðàÇó¼û¢ñøøÆö■òíààê¢45000 kJ-12000 kJȧ33000 kJ
ÀÀÀÀÈ´3Èˋý£Ýð
ÀÀÀÀ28ÈÛaȧ1ÀÀÀÀbȧ2
ÀÀÀÀ29ÈÛÈ´1Èˋ ÀÀÈ´2Èˋ1È₤10500ÀÀÈ´3Èˋ10
ÀÀÈ´2Èˋ1È₤10500ÀÀÈ´3Èˋ10
ÀÀÀÀ30ÈÛÂì39ÈËÀÀÂÖ12.5ÈË ÀÀÀÀ31ÈÛÈ´1ÈˋÂì äÍ£»
äÍ£»
ÂÖçÝ£Ÿà«ÆèCü·BØóÑ₤òÝȘطäÍ£»âˋǵò¿ó§¤ãȤ

 ü·äÍ£»âˋǵñ§ü·ØóÑ₤Øåø꣚¤üó½äÍöÿøòçáê¢å—ǵÈÛå—ǵçáöÿøòçáꢢèÆèüôò§úµ°—ÀÀÀÀÀÀÀÀÀÀ
ü·äÍ£»âˋǵñ§ü·ØóÑ₤Øåø꣚¤üó½äÍöÿøòçáê¢å—ǵÈÛå—ǵçáöÿøòçáꢢèÆèüôò§úµ°—ÀÀÀÀÀÀÀÀÀÀ
 ÀÀ
ÀÀ  ÀÀ
ÀÀ

óÞò¥È¤0.08 molÀÀÀÀÀÀÀÀ 0
ó§¤ãȤ ÀÀÀÀ
ÀÀÀÀ
ÀÀÀÀØ·ó§¤ãòÝ£š¤üó½äÍæÉçáöÿøòçáê¢öˆ0.07 molȘÆèÆÖ£Ÿà«ÆèCØóøêBȘäÍ£»âˋǵȘ¿ò Ș¢èøˆ°ðàŠ
Ș¢èøˆ°ðàŠ öÿøòçáê¢ÝÄÅÀÆÖ0.01
mol
ÀÀÀÀÈ´2Èˋ
öÿøòçáê¢ÝÄÅÀÆÖ0.01
mol
ÀÀÀÀÈ´2Èˋ
 www.ks5u.com
www.ks5u.com
¿º¥òîÏÅÈÆéîÀ - êñü¯ýÃêÅÝÚ - òåäãêÅÝÚ
¤±ÝÝòÀ£Ëêˆë½öËñ´¤ëý£ê¥ÅéüƒìÝ´ó§ä´ | ë½èüÆŤÎÅéüƒìÝ´æ´ú½ | çÓÅéíˋóÙƒìÝ´æ´ú½ | èÌâºòñÅÕößø¼ØÍÆŤÎÅéüƒìÝ´æ´ú½ | èÌóµúøà´ƒìÝ´æ´ú½
öËñ´¤ëý£ê¥ÅéüƒìÝ´çÓ£¯È¤027-86699610 ƒìÝ´ÆòüðȤ58377363@163.com