
题目列表(包括答案和解析)
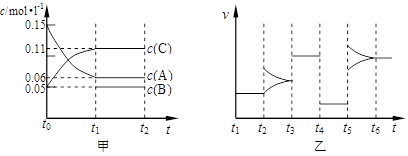
向某密闭容器中加入0.15mol/L A、0.05mol/L C和一定量的B三种气体。一定条件下发生反应,各物质浓度随时间变化如下图中甲图所示[t0时c( B)未画出,t1时增大到0.05mol/L]。乙图为 t2时刻后改变反应条件,平衡体系中正、逆反应速率随时间变化的情况。

(1)若t4时改变的条件为减小压强,则B的起始物质的量浓度为 mol/L;
该反应的平衡常数表达式为K= 。
(2)若t5时改变的条件是升温,此时v(正) > v(逆),平衡常数K的值将 (选填“增大”、“减小”或“不变”)。
(3)若 t1= 15s,则t0~ t1阶段以C 浓度变化表示的平均反应速率为v(C)=
mol/L·s。t3 时改变的某一反应条件可能是 (选填序号)。
a.使用催化剂 b.增大压强 c.增大反应物浓度 d.降低产物浓度
(4)若A的物质的量减少0.02mol时,容器与外界的热交换总量为a kJ,写出该反应的热化学方程式 。
向某密闭容器中加入0.15mol/L A、0.05mol/L C和一定量的B三种气体。一定条件下发生反应,各物质浓度随时间变化如下图中甲图所示[t0时c( B)未画出,t1时增大到0.05mol/L]。乙图为 t2时刻后改变反应条件,平衡体系中正、逆反应速率随时间变化的情况。
(1)若t4时改变的条件为减小压强,则B的起始物质的量浓度为 mol/L;
该反应的平衡常数表达式为K= 。
(2)若t5时改变的条件是升温,此时v(正) > v(逆),平衡常数K的值将 (选填“增大”、“减小”或“不变”)。
(3)若 t1= 15s,则t0~ t1阶段以C 浓度变化表示的平均反应速率为v(C)=
mol/L·s。t3时改变的某一反应条件可能是 (选填序号)。
a.使用催化剂 b.增大压强 c.增大反应物浓度 d.降低产物浓度
(4)若A的物质的量减少0.02mol时,容器与外界的热交换总量为a kJ,写出该反应的热化学方程式 。
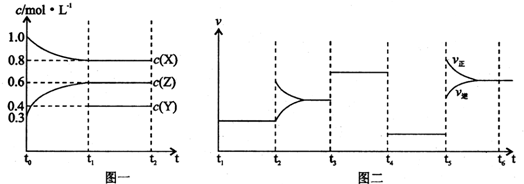
| A、Y的起始物质的量为1.0 mol | ||||
| B、t4-t5阶段改变的条件为减小压强;t5-t6是升高温度 | ||||
| C、此温度下该反应的化学方程式为2X(g)+Y(g)?2Z(g) | ||||
D、在相同条件下,若起始时容器中加入a mol X b mol Y和c mol Z,要达到t1时刻同样的平衡,a,b,c要满足的条件为a+
|
向一体积不变的密闭容器中加入2mol A、0.6mol C和一定量的B三种气体。一定条件下发生反应,各物质浓度随时间变化如图一所示。图二为t2时刻后改变反应条件,平衡体系中反应速率随时间变化的情况,且四个阶段都各改变一种不同的条件。已知t3~t??4阶段为使用催化剂;图一中t0~t1阶段c(B)未画出。
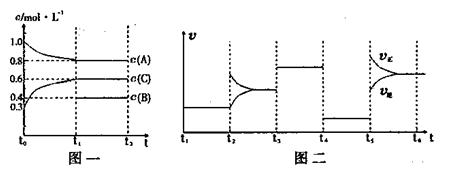
下列说法不正确的是( )
A.此温度下该反应的化学方程式2A(g)+B(g)![]() 2C(g)
2C(g)
B.t4~t5阶段改变的条件为减小压强
C.B的起始物质的量为1.0mol
D.在相同条件下,若起始时容器中加入a mol A、bmol B和cmol C,要达到t1时刻同样的平衡,a、b、c要满足的条件为a+![]() =2.4 和 b+
=2.4 和 b+![]() =1.2
=1.2
一、选择题(每小题6分,共78分)
1
2
3
4
5
6
7
8
9
10
11
12
13
B
C
D
C
B
B
B
A
A
C
D
D
B
二、选择题(全部选对的给6分,选对但不全的给3分,有选错的给0分。共48分)
题号
14
15
16
17
18
19
20
21
答案
B
B
AD
B
CD
A
B
D
22、(1)×10(填“×10或×
换挡后未进行电阻调零,读出的欧姆表示数未乘以倍率 4分
(2)电源内阻较小且滑线变阻器阻值较大 4分
E=1.5V r=2.6Ω < < 各2分
23.(16分)解析:(1)由图象知,s1=
即 ………………………………………………………………4分
………………………………………………………………4分
代入数据解得:k=62.5N/m………………………………………………………2分
(2)当s2=
 …………………………………………………………4分
…………………………………………………………4分
代入数据解得: ……………………………………………………2分
……………………………………………………2分
(3)由机械能守恒定律得: =1.8
=1.8 4 J…………………4分
4 J…………………4分
24.(18分)解析:(1)以物块为研究对象,根据牛顿第二定律可得:
 Ff1=μ2mg=ma1…………………1分
Ff1=μ2mg=ma1…………………1分
代入数据解得:a1=
以木板为研究对象,受力如图。
竖直方向合力为零,可得:F2=F1+Mg…………………1分
又有Ff2=μ
根据牛顿第二定律得:Ff1‘- Ff2=Ma2…………………1分
代入数据解得: a2=
(2)当物块滑到木板右端时,两者恰好有共同速度。…………………2分
设运动时间为t1,物块和木板运动的位移分别为s1 、s2。
根据题意得:v0-a1t1=a2t1 …………………2分
s1 -s2=L …………………2分
s1=v0t1- a1t12 …………………2分
a1t12 …………………2分
s2= a2t12 …………………2分
a2t12 …………………2分
代入数据解得:v0=
25.(20分)解析:(1)带电微粒从O点射入磁场,运动轨迹如图。
第一次经过磁场边界上的A点
由 得:
得:
 m………………2分
m………………2分
A点位置坐标(-4×10
 (2)设带电微粒在磁场中做圆周运动的周期为T
(2)设带电微粒在磁场中做圆周运动的周期为T
则t=tOA+tAC= ………………3分
………………3分
T= ……………… 2分
……………… 2分
代入数据解得:T=1.256×10-5s
所以 t=1.256×10-5s ………………1分
(3)微粒从C点沿y轴正方向进入电场,做曲线运动
 ………………2分
………………2分
 ………………2分
………………2分
 ………………2分
………………2分
代入数据解得: m………………1分
m………………1分
y= -2r=0.2-2×4×10
-2r=0.2-2×4×10
离开电、磁场时的位置坐标
(0,
26、(14分)本题答案有开放性,合理即可给分。
⑴①C(或Fe) ②
⑶①CaC2+2H2O=Ca(OH)2+C2H2↑ ;②麦芽糖;
⑷①Na2CO3+CO2+H2O=2NaHCO3 ;②红褐色固体。
27、(15分)
(1)6MnO4-+5CuS+28H+=5Cu2++5SO2↑+6Mn2++14H2O 6
(2)19.6 500 mL容量瓶和天平
(3)设Cu2S、CuS的物质的量分别为x、y
与Cu2S、CuS反应后剩余KMnO4的物质的量:
|