
题目列表(包括答案和解析)
A.73.33 B.73 C.72 D.70.6
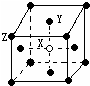 (1)氮元素基态原子核外未成对电子数为
(1)氮元素基态原子核外未成对电子数为(1)实验室里有已配制好的NaOH溶液,一瓶所贴标签为6 mol·L-1,另一瓶所贴标签为12%(密度为1.12 g·mL-1).则12%的NaOH溶液的物质的量浓度为________.
(2)在50 mL NaNO3和Na2SO4的混合溶液中,c(Na+)=1 mol/L,往其中加入50 mL BaCl2溶液恰好完全反应,得到2.33 g白色沉淀,则原混合溶液中c(NO3-)=________.
(3)实验室里常用KMnO4与浓盐酸反应制取少量氯气,其化学方程式为:
2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
1、用双桥式表示电子转移的方向和数目.
2、产生标况下11.2 L Cl2,则被氧化的HCl的物质的量为________摩.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com