
题目列表(包括答案和解析)
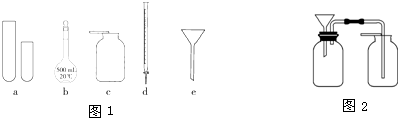
| 仪器编号 | a | b | c | d | e |
| 名称 | 试管 | 溶量瓶 | 集气瓶 | 碱式滴定管 | 普通漏斗 |
| 改正的名称 |
下列图象中,纵坐标为沉淀物的量,横坐标为溶液中加入反应物的物质的量,试按题意将相应的字母序号填入表中的顺序为( )
|


| 水 |
| 水 |

 +CH3CH2Cl
+CH3CH2Cl +HCl
+HCl +CH3CH2Cl
+CH3CH2Cl +HCl
+HCl

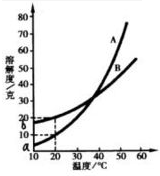 A、B两种化合物的溶解度曲线如右图.现要用结晶法从A、B混和物中提取A.(不考虑A、B共存时,对各自溶解度的影响)
A、B两种化合物的溶解度曲线如右图.现要用结晶法从A、B混和物中提取A.(不考虑A、B共存时,对各自溶解度的影响)
题号
1
2
3
4
 5
5
6
7
8
9
答案
D
C
C
A
D
B
BC
C
B
题号
10
11
12
 13
13
14
15
16
17
18
答案
AD
C
A
B
B
B
A
D
B
19.(9分)
(1)A MnO2 浓盐酸 B 饱和食盐水 D NaOH溶液
(2)分液漏斗
(3)2NaBr+Cl2=2NaCl+Br2
(4)90%
20.(8分)
(1)B
(2)① 过氧化钠容易吸收空气中的H2O和CO2,不宜暴露在空气中称量,并且过氧化钠为粉末状不易全部转移到锥形瓶中。
(3)A 偏大
(4)
21.(6分)
(1)2Cl2+2Ca(OH)2 = CaCl2+Ca(ClO)2+2H2O
(2)Ca(ClO)2
(3)Ca(ClO)2 + CO2 + H2O == CaCO3↓+ 2 HClO
(4)碱性
 22.(8分)(1)B:Na2O2 E:NaHCO3;
22.(8分)(1)B:Na2O2 E:NaHCO3;
(2)2Na+2H2O=2NaOH+H2↑。
(3)CO2+2OH-=CO32-+H2O。
(4)2NaHCO3+2Na2O2 2Na2CO3+2NaOH+O2↑。
2Na2CO3+2NaOH+O2↑。
23.(11分)
(1)A.HCl(或浓HCl) C.Cl2 D.KBr G.KI
(2)C+D:Cl2+2KBr=2KCl+Br2 ;A+B:4HCl+MnO2 MnCl2+Cl2↑+2H2O;②;C
MnCl2+Cl2↑+2H2O;②;C
(3)5:1
24.(5分)(1)2Fe2++Cl2=2Fe3++2Cl-; (2)2x=3n; (3)x>;(4)1.5n。
25.(6分)(1)
26.(6分)(1)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com