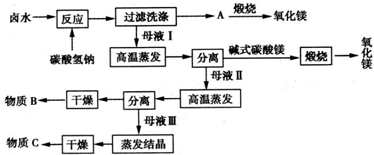
氧化铜有多种用途,如用作玻璃着色剂、油类脱硫剂等,为获得纯净的氧化铜并探究其性质,某同学用工业硫酸铜(含硫酸亚铁等杂质)进行如下实验:
(1)制备氧化铜:
工业CuSO
4CuSO
4溶液
CuSO
4?5H
2O…CuO
①步骤Ⅰ的目的是除去不溶性杂质.操作是
加适量水溶解,搅拌,过滤
加适量水溶解,搅拌,过滤
.
②步骤Ⅱ的目的是除去硫酸亚铁.操作是:滴加H
2O
2溶液,稍加热;Fe
2+转化完全后,慢慢加入Cu
2(OH)
2CO
3粉末,搅拌,以控制溶液pH=3.5;加热煮沸一段时间,过滤,用稀硫酸酸化滤液至pH=1.滴加H
2O
2的目的是
将Fe2+氧化为Fe3+
将Fe2+氧化为Fe3+
,加入Cu
2(OH)
2CO
3粉末的目的是
调节溶液的酸性,使Fe3+水解全部转化为Fe(OH)3沉淀
调节溶液的酸性,使Fe3+水解全部转化为Fe(OH)3沉淀
.
③步骤Ⅲ的目的是得到CuSO
4?5H
2O晶体,操作是将CuSO
4?5H
2O溶液加热蒸发至有晶膜出现时,停止加热,
冷却结晶
冷却结晶
,水浴加热烘干.采用水浴加热的原因是
防止CuSO4?5H2O晶体分解
防止CuSO4?5H2O晶体分解
.
(2)探究氧化铜性质:
①取A、B两支试管,往A中先加入适量CuO粉末,再分别向A和B中加入等体积的3%H
2O
2溶液,只观察到A中有大量气泡,结论是
CuO对H2O2的分解有催化作用
CuO对H2O2的分解有催化作用
.
②为探究试管A中反应的速率,收集气体并测定其体积必需的实验仪器除导管、橡皮塞、水槽外还必须有
量筒、秒表(或计时器、手表)
量筒、秒表(或计时器、手表)
.