
题目列表(包括答案和解析)
| 编号 | 实验 | 现象 |
| ① | 往盛有5 mL 5% H2O2溶液的试管中,伸入带火星的木条, | 木条不复燃 |
| ② | 往盛有5 mL 5% H2O2溶液的试管中,加入a g MnO2,伸入带火星的木条, | 木条复燃 |
| 实验次序 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| MnO2粉末用量(g) | O.1 | 0.2 | 0.3 | 0.4 | 0.5 | O.6 | 0.7 | 0.8 | O.9 | 1.O |
| 所用时间(s) | 17 | 8 | 7 | 5 | 4 | 3 | 2 | 2 | 2 | 2 |
| 实验编号 | 实验1 | 实验2 | 实验3 | 实验4 |
| 加入KNO3的质量(g) | 40 | 50 | 60 | 70 |
| 溶液质量(g) | 90 | 100 | 105 | 105 |
| 实验步骤和操作 | 实验现象和结论 |
(1)如图所示: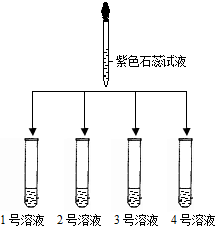 |
①2号溶液由无色变为红色,则2号溶液是 稀盐酸 稀盐酸 ②另三支试管中溶液均由无色变蓝色 |
(2)另取1、3、4、号溶液,分别滴加2号溶液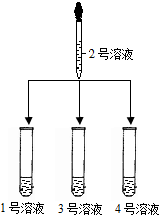 |
①3号溶液中有气泡放出,则3号溶液是 碳酸钠溶液 碳酸钠溶液 ②另二支试管中溶液无明显变化 |
| (3)另取1、4号溶液,分别滴加 碳酸钠溶液 碳酸钠溶液 |
①1号溶液中有白色沉淀析出,则反应的 化学方程式为 Ca(OH)2+Na2CO3=2NaOH+CaCO3↓ Ca(OH)2+Na2CO3=2NaOH+CaCO3↓ ②另一支试管中溶液无明显变化 |
| 实验操作 | 实验现象 | 实验结论 |
| 任取三种溶液 于三支试管中, 分别滴加第四 中溶液 |
一支试管中有气泡放出, 其余二支试管中溶液无明显变化 |
第四种溶液为稀盐酸 |
| 一支试管中有白色沉淀析出, 其余二支试管中溶液无明显变化 |
第四种为碳酸钠溶液 | |
| 三支试管中溶液均无明显变化 | 第四种为氢氧化钠溶液 |
| 实验操作 | 实验现象 | 实验结论 |
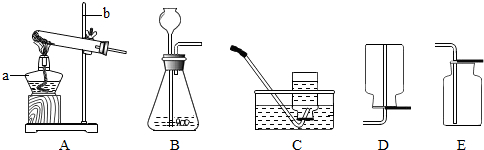
(1)如图所示: |
①A、B、C均无明显变化 ②D中有沉淀析出 |
标号为1、2、3、4的 溶液依次为(用化学式 表示): NaOH、Na2CO3、HCl、Ca(OH)2 NaOH、Na2CO3、HCl、Ca(OH)2 或HCl、Ca(OH)2、NaOH、Na2CO3 HCl、Ca(OH)2、NaOH、Na2CO3 |
| ||
| ||
| ||
| ||
| 实验次序 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| 二氧化锰(MnO2)和粉末用量(g) | 0.1 | 0.2 | 0.3 | 0.4 | 0.5 | 0.6 | 0.7 | 0.8 |
| 所用时间 | 17 | 8 | 7 | 5 | 4 | 3 | 2 | 1 |
| 实验步骤和操作 | 实验现象和结论 |
(1)如图所示: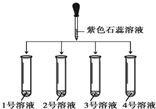 |
①2号溶液由无色变为红色, 则2号溶液是 稀盐酸 ②另三支试管中溶液均由无色变蓝色 |
(2)另取1、3、4号溶液,分别滴加2号溶液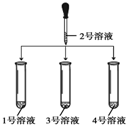 |
①3号溶液中有气泡放出, 则3号溶液是 碳酸钠 ②另外二支试管中溶液无明显变化 |
| (3)另取1,4号溶液,分别滴加 3号溶液 |
①1号溶液中有白色沉淀析出, 则反应的化学方程式为 Na2CO3+Ca(OH)2=CaCO3↓+2NaOH ②另一支试管中溶液中无明显变化 |
| 实验操作 | 实验现象 | 实验结论 |
任取三种溶液于三支试管中,分别滴加第四种溶液 |
①一支试管中有气泡放出 其余二支试管中溶液无明显变化 |
①第四种溶液为稀盐酸 |
| ②一支试管中有白色沉淀析出, 其余二支试管中溶液无明显变化 |
②第四种为Na2CO3溶液 | |
| ③三支试管中溶液均无明显变化 | ③第四种为NaOH溶液 |
| 实验操作 | 实验现象 | 实验结论 |
如图所示: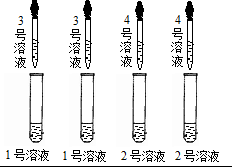 |
①A,B,C均无明显变化 ②D中有沉淀析出 |
标号为1,2,3,4的溶液依次为(用化学式表示): NaOH、Ca(OH)2、HCl、Na2CO3 或HCl、Na2CO3、NaOH、Ca(OH)2 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com