
题目列表(包括答案和解析)
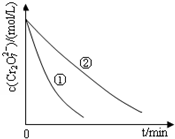 某酸性工业废水中含有K2Cr2O7.光照下,草酸(H2C2O4)能将其中的Cr2O72-转化为Cr3+.某课题组研究发现,少量铁明矾[Al2Fe(SO4)4?4H2O]即可对该反应起催化作用.为进一步研究有关因素对该反应速率的影响,探究如下
某酸性工业废水中含有K2Cr2O7.光照下,草酸(H2C2O4)能将其中的Cr2O72-转化为Cr3+.某课题组研究发现,少量铁明矾[Al2Fe(SO4)4?4H2O]即可对该反应起催化作用.为进一步研究有关因素对该反应速率的影响,探究如下| 实验编号 | 初始 pH |
废水样品 体积/mL |
草酸溶液 体积/mL |
蒸馏水 体积/mL |
| ① | 4 | 10 | 30 | |
| ② | 5 | 60 | 10 | |
| ③ | 60 | 20 |
| 实验方案(不要求写具体操作过程) | 预期实验结果和结论 |
| 取 |
反应进行相同时间后 若溶液中的Cr2O72-浓度 若溶液中的Cr2O72-浓度 |
(6分)某反应体系中的物质有:Cr2(SO4)3、K2S2O8、K2Cr2O7、K2SO4、H2SO4、H2O。已知K2S2O8的氧化性比K2Cr2O7强。
(1)请将以上反应物与生成物编写成一个氧化还原反应方程式(要求配平) 。
(2)反应中,被还原的物质是 ,Cr2(SO4)3是 。
(3)在酸性条件下K2Cr2O7与草酸(H2C2o4)反应的产物是:Cr2(SO4)3、CO2、K2SO4和H2O,则还原剂与氧化剂物质的量之比为 。
某反应体系中的物质有:Cr2(SO4)3、K2S2O8、K2Cr2O7、K2SO4、H2SO4、H2O。
已知K2S2O8的氧化性比K2Cr2O7强。
(1)请将以上反应物与生成物编写成一个氧化还原反应方程式(不要求配平)
(2)反应中,被还原的物质是 ,Cr2(SO4)3是 。
(3)请将氧化剂与还原剂的化学式及配平后的系数填入下列空格中,并标出电子转移方向和数目:
+ +……
(4)在酸性条件下K2Cr2O7与草酸(H2C2O4)反应的产物是:Cr2(SO4)3、CO2、K2SO4和H2O,则还原剂与氧化剂物质的量之比为 。
某反应体系中的物质有:Cr2(SO4)3、K2S2O8、K2Cr2O7、K2SO4、H2SO4、H2O。
已知K2S2O8的氧化性比K2Cr2O7强。
(1)请将以上反应物与生成物编写成一个氧化还原反应方程式(不要求配平)
(2)反应中,被还原的物质是 ,Cr2(SO4)3是 。
(3)请将氧化剂与还原剂的化学式及配平后的系数填入下列空格中,并标出电子转移方向和数目:
|
|||||||
|
|
||||||
|
|||||||
+ +……
(4)在酸性条件下K2Cr2O7与草酸(H2C2O4)反应的产物是:Cr2(SO4)3、CO2、K2SO4和H2O,则还原剂与氧化剂物质的量之比为 。
(6分)某反应体系中的物质有:Cr2(SO4)3、K2S2O8、K2Cr2O7、K2SO4、H2SO4、H2O。已知K2S2O8的氧化性比K2Cr2O7强。
(1)请将以上反应物与生成物编写成一个氧化还原反应方程式(要求配平) 。
(2)反应中,被还原的物质是 ,Cr2(SO4)3是 。
(3)在酸性条件下K2Cr2O7与草酸(H2C2o4)反应的产物是:Cr2(SO4)3、CO2、K2SO4和H2O,则还原剂与氧化剂物质的量之比为 。
一、选择题(本题共10分),每小题2分,选对得2分,选错得0分。
1―5DDCDB
二、选择题(本题共36分),每小题3分,选对得3分,选错得0分
6―10CDCAB 11―15BCDDC 16―17BD
三、选择题(本题共20分),每小题4分,若正确答案啼包括一个选项,选对得4分,错选若多选时,该题为0分;若正确答案包括两个选项,只选一个且正确的给2分,选两个且都正确的给4分,但只要选错一个,该小题就为0分。
18.AC 19.B 20.BD 21.AC 22.C
四、(本题共24分)
(1)3s23p4,14。(1分×2)
(2)2Al+2OH-+2H2O→2AlO2-+3H2↑,小于。(1分×2)
|