
题目列表(包括答案和解析)
反应
FeO(s)+CO(g)将一定量的FeO、CO、Fe、CO2四种物质放入密闭容器中,在1273 K下发生如下反应:FeO(s)+CO(g)![]() Fe(s)+CO2(g),其平衡常数Kc=0.5.若起始浓度c(CO)=0.05 mol/L,c(CO2)=0.01 mol/L.
Fe(s)+CO2(g),其平衡常数Kc=0.5.若起始浓度c(CO)=0.05 mol/L,c(CO2)=0.01 mol/L.
(1)通过计算判断该条件下化学反应进行的方向.
(2)求平衡时CO的转化率?
(3)增加FeO的量,对平衡有无影响?
将一定量的FeO、CO、Fe、CO2四种物质放入密闭容器中,在1273 K下发生如下反应:FeO(s)+CO(g)![]() Fe(s)+CO2(g),其平衡常数Kc=0.5.若起始浓度c(CO)=0.05 mol/L,c(CO2)=0.01 mol/L.
Fe(s)+CO2(g),其平衡常数Kc=0.5.若起始浓度c(CO)=0.05 mol/L,c(CO2)=0.01 mol/L.
(1)通过计算判断该条件下化学反应进行的方向.
(2)求平衡时CO的转化率?
(3)增加FeO的量,对平衡有无影响?
已知可逆反应N2O4(g) 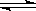 2NO2(g) 在873K时,平衡常数K1=1.78×104,转化率为a%,在1273 K时,平衡常数K2 = 2.8×104,转化率为b%,则下列叙述正确的是
2NO2(g) 在873K时,平衡常数K1=1.78×104,转化率为a%,在1273 K时,平衡常数K2 = 2.8×104,转化率为b%,则下列叙述正确的是
| A.由于K2>K1,所以a>b |
| B.由于K随温度升高而增大,所以此反应的△H>0 |
| C.由于K随温度升高而增大,所以此反应的△H<0 |
| D.其它条件不变时,将盛有该混合气体的容器置于热水中,体系颜色变浅 |
已知可逆反应N2O4(g) 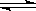 2NO2(g)
在873K时,平衡常数K1=1.78×104,转化率为a%,在1273 K时,平衡常数K2 = 2.8×104,转化率为b%,则下列叙述正确的是
2NO2(g)
在873K时,平衡常数K1=1.78×104,转化率为a%,在1273 K时,平衡常数K2 = 2.8×104,转化率为b%,则下列叙述正确的是
A.由于K2>K1,所以a>b
B.由于K随温度升高而增大,所以此反应的△H>0
C.由于K随温度升高而增大,所以此反应的△H<0
D.其它条件不变时,将盛有该混合气体的容器置于热水中,体系颜色变浅
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com