
题目列表(包括答案和解析)
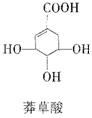
目前世界各国都在抗击甲型H1N1流感,达菲(Tamiflu)被世界卫生组织推荐作为治疗和预防甲型H1N1流感的有效药物之一,它是以我国特有中药材八角的提取物—莽草酸(shikimicacid)为原料经过十多步反应合成的。已知莽草酸和达菲的结构简式如下:

![]()
请完成下列问题:
(1)写出莽草酸的分子式___________。
(2)写出莽草酸分子中官能团的名称___________________________
(3)达菲可能发生的反应类型有_________________
A.氧化反应 B.水解反应 C.加成反应 D.消去反应
(4)1 mol莽草酸最多能与_______ mol金属钠反应,最多可与______ mol碳酸氢钠反应。
(5)请写出莽草酸与乙醇在浓硫酸作用下发生酯化反应的化学方程式
(有机物用结构简式表示):_________________________________________________
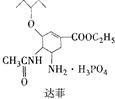
(6)莽草酸通过消去反应可以得到B(B的结构简式为:![]() ),B在浓硫酸加热作用下可得到缩聚物C,C的结构简式是______________;水杨酸是一种与B具有相同官能团的同分异构体,且苯环上的取代基相邻,请写出水杨酸与乙酸酐合成阿司匹林(乙酰水杨酸)的化学方程式(有机物用结构简式表示):______________________________________;B的同分异构体中既含有酚羟基又含有酯基的共有三种,写出其中一种同分异构体的结构简式 _________________________。
),B在浓硫酸加热作用下可得到缩聚物C,C的结构简式是______________;水杨酸是一种与B具有相同官能团的同分异构体,且苯环上的取代基相邻,请写出水杨酸与乙酸酐合成阿司匹林(乙酰水杨酸)的化学方程式(有机物用结构简式表示):______________________________________;B的同分异构体中既含有酚羟基又含有酯基的共有三种,写出其中一种同分异构体的结构简式 _________________________。
(16分)化学发展史上,有许多偶然事件引起科学发现的事例,碘的发现也得益于Courtoris对意外现象的注意。碘是人类发现的第二个生物必需微量元素,它以碘化物形式存在于海水、海藻及人体甲状腺中。人类缺碘会引起甲状腺肿大,我国已全面实施加碘盐方案。
3-1 单质碘的制备方法之一是在酸性条件下通Cl2于NaI溶液中,指出运用该法时应注意的问题?分析其原因,写出有关反应方程式。
3-2 在100%硫酸中,I2可被HIO3氧化成I3+,写出配平的离子方程式。
3-3 为什么在日照强、温度高的海区,表层水碘浓度往往要低一些?
3-4 人体缺碘会影响正常的生命活动。儿童缺碘会造成身体畸形,智力低下。成年人缺碘会因新陈代谢能力降低而导致全身无力,提早出现衰老现象。为提高人体素质,食物补碘已引起人们的重视。据报道,人从食物中摄取碘后便在甲状腺中积存下来,通过一系列化学反应形成甲状腺素。甲状腺素的结构:
(1)写出甲状腺素的化学式 ;
(2)在甲状腺内,甲状腺素的主要合成过程如下:
A(氨基酸)![]() B
B![]() 甲状腺素+C(氨基酸)
甲状腺素+C(氨基酸)
请写出A、B、C的结构简式。
3-5 科研表明,人的一生只要能摄入一小茶匙的碘就能正常发育,健康生活。目前预防缺碘的有效办法是食用含碘食盐。目前国内食盐加碘加的主要是碘酸钾。
(1)写出工业上以KI为原料制备碘酸钾的化学方程式;
(2)如何用简易操作检验食盐是否加碘。写出离子反应方程式。
3-6 已知反应H2+I2![]() 2HI,分两步完成I2
2HI,分两步完成I2![]() 2I H2+2I
2I H2+2I![]() 2HI
2HI
式中k,k1,k2,k3是分别为各反应相应的速率常数,若用Ea,E1,E2,E3分别表示各反应相应的活化能,请找出Ea和E1,E2,E3间的关系。已知公式如下:
①对于反应aA+bB→eE+f F,反应速率为:v=k[A]a[B]b
②速率常数与活化能之间满足阿仑尼乌斯公式:k=Ae-Ea/RT
③对于反应I2![]() 2I满足:v正=v逆
2I满足:v正=v逆

| A.氧化反应 | B.水解反应 | C.加成反应 | D.消去反应 |
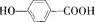 ),B在浓硫酸加热作用下可得到缩聚物C,C的结构简式是______________;水杨酸是一种与B具有相同官能团的同分异构体,且苯环上的取代基相邻,请写出水杨酸与乙酸酐合成阿司匹林(乙酰水杨酸)的化学方程式(有机物用结构简式表示):______________________________________;B的同分异构体中既含有酚羟基又含有酯基的共有三种,写出其中一种同分异构体的结构简式 _________________________。
),B在浓硫酸加热作用下可得到缩聚物C,C的结构简式是______________;水杨酸是一种与B具有相同官能团的同分异构体,且苯环上的取代基相邻,请写出水杨酸与乙酸酐合成阿司匹林(乙酰水杨酸)的化学方程式(有机物用结构简式表示):______________________________________;B的同分异构体中既含有酚羟基又含有酯基的共有三种,写出其中一种同分异构体的结构简式 _________________________。(13分)绿矾(化学式FeSO4?7H2O)是硫酸法生产钛白粉的主要副产物,每生产1吨钛白粉,副产4.5~5.0吨绿矾,目前全国每年约副产绿矾75万吨,除极少量被用于制备新产品外,绝大部分作为废料弃去,对环境造成污染。因此开发综合利用绿矾的工艺,是一项很有意义的工作。某研究者提出如下图所示的绿色工艺流程。
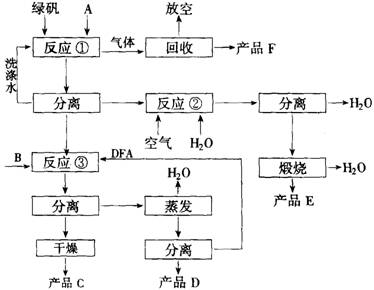
其中A是碳铵,B是氯化物,C是不含氯的优质钾肥,D是一种氮肥,E是红色颜料,F是常见的气体化合物。该工艺实现了原料中各主要成分的利用率均达94% 以上,可望达到综合利用工业废弃物和防治环境污染的双重目的。
9-1 写出B、C、D、E、F的化学式。
9-2 写出反应①、②、③的化学方程式。
9-3 指出反应③需要加入DFA(一种有机溶剂)的理由。
9-4 判断DFA是否溶于水。
有些化学反应的化学能能直接转化成电能
I.利用 Fe + CuSO4 = FeSO4 + Cu反应,设计一个原电池:
(1)在下框中画出装置图(标明电解质溶液、正、负极和电极材料)

(2)下列说法中,正确的是 。(填字母)
A.电解质溶液中阳离子向负极移动 B.电子通过外导线由负极流向正极
C.当导线中有1mol电子通过时,理论上正极放出1g气体
D.若所选电极的质量相等,理论上两极质量差为60g,导线中有1 mol电子通过
II.三套装置如下图所示, A、B、C烧杯中分别盛有相同物质的量浓度的稀硫酸。
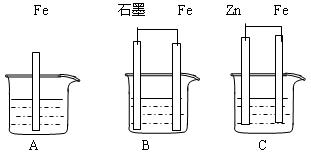
(1)比较A、B、C中铁被腐蚀的速率,由快到慢的顺序为 ;
(2)若C中电解质溶液是氯化钠溶液,则Fe电极的电极反应式为 ;
III.目前常用的镍(Ni)镉(Cd)电池,其电池总反应可以表示为:
![]()
已知Ni(OH)2和Cd(OH)2均难溶于水但能溶于酸。
(1)以下说法中正确的是
①以上反应是可逆反应 ②以上反应不是可逆反应
③充电时化学能转变为电能 ④放电时化学能转变为电能
(2)废弃的镍镉电池已成为重要的环境污染物,资料表明一节废镍镉电池可以使一平方米面积的耕地失去作用价值。在酸性土壤中这种污染特别严重,这是因为
(3)另一种常用的电池是锂电池,锂是一种碱金属元素,其相对原子质量为7,由于它的比容量(单位质量电极材料所能转换的电量)特别大而广泛应用于心脏起搏器,一般使用时间可长达十年,它的负极用金属锂制成,电池总反应可表示为Li+ MnO2 = LiMnO2。
锂电池中的电解质溶液需用非水溶剂配制,为什么这种电池不能使用电解质的水溶液(请用化学方程式表示其原因) 。
一、选择题(共10分)
1.D 2.B 3.A 4.D 5.C
二、选择题(共45分)
6.A 7.C 8.C 9.D 10.D 11.A 12.B 13.A
14.C 15.A 16.D 17.B 18.A 19.C 20.D
三、填空题(38分)
21.(2分)方案3 22.(2分)解法3
23.(6分)(1)C、Fe F、H2
|