
题目列表(包括答案和解析)
某些化学键键能数据如下:
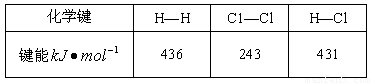
则下列热化学方程式不正确( )
A.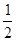 H2(g)+
H2(g)+ 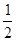 Cl2(g)HCl(g);
Cl2(g)HCl(g);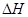 =
-91.5
=
-91.5
B.H2(g)+ Cl2(g)2HCl(g);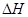 =
-183
=
-183
C.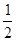 H2(g)+
H2(g)+ 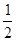 Cl2(g)HCl(g);
Cl2(g)HCl(g);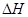 =
+91.5
=
+91.5
D.2HCl(g)H2(g)+ Cl2(g);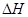 = +183
= +183
某些化学键键能数据如下:

则下列热化学方程式不正确( )
A.![]() H2(g)+
H2(g)+ ![]() Cl2(g)HCl(g);
Cl2(g)HCl(g);![]() = -91.5
= -91.5![]()
B.H2(g)+ Cl2(g)2HCl(g);![]() = -183
= -183![]()
C.![]() H2(g)+
H2(g)+ ![]() Cl2(g)HCl(g);
Cl2(g)HCl(g);![]() = +91.5
= +91.5![]()
D.2HCl(g)H2(g)+ Cl2(g);![]() = +183
= +183![]()
某些化学键键能数据如下:
则下列热化学方程式不正确( )
A.H2(g)+
Cl2(g)HCl(g);
=-91.5
B.H2(g)+ Cl2(g)2HCl(g);=-183
C.H2(g)+
Cl2(g)HCl(g);
=+91.5
D.2HCl(g)H2(g)+ Cl2(g);= +183
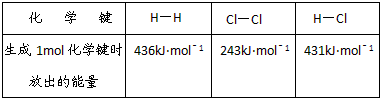
已知下列数据
| 化学键w.w.^w.k.&s.5*u.c.#om | H—H | Cl—Cl | H—Cl |
| 生成(拆开)1mol化学键放出(吸收)的能量 | 436kJ | 243kJ | 431kJ |
则下列热化学方程式不正确的是( )
A.![]() H2(g)+
H2(g)+![]() Cl2(g)==HCl(g) ;△H=-91.5kJ·mol-1
Cl2(g)==HCl(g) ;△H=-91.5kJ·mol-1
B.H2(g)+ Cl2(g)==2HCl(g) ;△H=-183kJ·mol-1
C.![]() H2(g)+
H2(g)+![]() Cl2(g)==HCl(g) ;△H=+91.5kJ·mol-1
Cl2(g)==HCl(g) ;△H=+91.5kJ·mol-1
D.2HCl(g) ==H2(g)+ Cl2(g) ;△H=+183kJ·mol-1
第I卷
一、选择题
题号
1
2
3
4
5
6
7
8
9
10
11
12
答案
A
B
B
C
C
B
B
B
A
B
D
13.(8分)
(1)①非极性 二氧化碳电子式略。 (各1分)
② C(s) + O2(g) = CO2(g) △H = -393.6kJ/mol 2分
(2) ① Al3+ + 4OH- = AlO2- + 2H2O 2分
② Al3+ + 3AlO2- + 6H2O = 4Al(OH)3↓ 2分
14.(10分)
(1)1nm~100nm(1分)
(2)Fe FeS H2SO4(稀)(3分)
(3)①H H(1分)
H(1分)
②2Fe2++H2O2+2H+=2Fe3++2H2O(2分)
(4)取少量E于试管中,用胶头滴管入NaOH溶液,加热试管,可观察到试管口处
湿润的红色石蕊试纸变蓝。(或其他合理答案)(3分)
15.(8分)
(1)K= (2分) 放热 (1分)
(2)b (1分) 1.5×10-3mol?L-1?s-1 (2分)
(3)bc (1分) (4)c (1分)
16.(10分)
方案一 (1) 保证NaHCO3全部分解 (1分)
方案二
(2)①检查装置的气密性(1分) 硫酸 (1分)
防止空气中水蒸气、CO2进入C管被吸收(1分)
② C (1分)
③需设计一将A、B中的CO2全部吹入C中吸收的气体装置(1分)
方案三
(3)①玻璃棒(1分)
②取少量滤液,再滴加BaCl2少许,如无白色沉淀说明沉淀完全(1分)
③ 51%(2分)
17.(18分)
(1)加成反应 (还原反应)(1分);
(2) CH3COOH 1分
 Br2CH― ―OOCCH3 ;
2分
Br2CH― ―OOCCH3 ;
2分
|