
题目列表(包括答案和解析)
| ||
| ||
| ||
| ||
 CaSO3,②2CaSO3+O2
CaSO3,②2CaSO3+O2  CaSO4,③2SO2+O2
CaSO4,③2SO2+O2 2SO3,④SO3+CaO
2SO3,④SO3+CaO CaSO4,根据以上条件回答:
CaSO4,根据以上条件回答:
| ||
| ||
| ||
| ||
 CaSO3,②2CaSO3+O2
CaSO3,②2CaSO3+O2 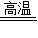 CaSO4,③2SO2+O2
CaSO4,③2SO2+O2 2SO3,④SO3+CaO
2SO3,④SO3+CaO CaSO4,根据以上条件回答:
CaSO4,根据以上条件回答:
说明:1.本答案仅供评分时参考使用
2.对于有多种答案的试题,这里只给一种或几种答案,其它答案若合理请参照此评分标准给分。
3.试题满分80分。
1
2
3
4
5
6
7
8
9
10
11
12
C
A
B
D
B
C
A
A
D
C
D
B
13.(1)2N (2)3OH― (3)CaSO4 (4)4SO2
14. (1) CH4 (2) CO (3) Ca(OH)2 (4) H2(每空1分,共4分)
15.(1)在
16.(1)10 (2)蓝 (3)NaCl和HCl(或氯化钠和盐酸)
17.化汞受热分解成氧气和汞;一滴水中含有15万亿亿个水分子。(各1分)
18.⑴化合反应 ⑵吸收煤燃烧时产生的SO2,以减少对大气的污染。(各1分)
19.(1)有机物 (2)苯酚有毒性和腐蚀性 (3)②③ (各1分)
(4)C6H6O+7O2 6CO2+3H2O(2分)
6CO2+3H2O(2分)
20.(1)2NH4HCO3+H2SO4= (NH4)2SO4+2H2O+CO2↑(2分)
理由:1、碳铵在农村是典型的化肥,材料易得。2、碳铵在与酸反应后会产生铵盐,碳铵作为氮肥的肥效不受影响。3、碳铵溶于水,与废酸反应充分;石灰石与废酸反应生成的CaSO4微溶,会覆盖在石灰石的表面,阻止反应的继续进行。(回答2点即可得2分)
(2)因为CO2密度比空气大,使CO2能与植物的叶片充分接触。(1分)
21.(6分)(1)C:CuO D:C G:NaOH H:Zn (各1分)
(2)Na2CO3+Ca(OH)2=CaCO3↓+2NaOH(2分)
22.(1)红磷燃烧时产生大量“白烟”(1分);打开止水夹时,可观察到烧杯中的水倒流进集气瓶中,流入集气瓶的水约占原空气体积的1/5。(1分)
(2)
可能出现的现象
实验结果
一
烧杯中的导气管口有气泡冒出
偏大
二
烧杯中的水进入集气瓶中将红磷浇灭
偏小
上面两种情况学生回答出任何一种即可,如果“可能出现的现象”未答对,即便“实验结果”答对也不得分。
(影响集气瓶内压强的因素:①红磷燃烧时放热,使集气瓶内气体的温度升高,集气瓶内的气体受热膨胀;②红磷燃烧消耗集气瓶内的氧气导致集气瓶内压强降低。当因素①的作用大于因素②的作用时,集气瓶内压强增大。当因素①的作用小于因素②的作用时,集气瓶内压强减小)
(3)ABD(2分,只写一个或两个正确选项得1分,如果有错误选项就不得分)
23.(化学方程式每个2分,其余每空1分)(1)催化
2KClO3 2KCl+3O2↑
2KCl+3O2↑
②③⑤(少选、错选不得分)
(2)实验室制取氢气(或实验室制取二氧化碳;用双氧水制取氧气)
(3)
设计方案
实验名称
将酒精灯加网罩(或换酒精喷灯)
木炭还原氧化铜
或去掉酒精灯,将试管竖起
制取氢气或二氧化碳
取下塞子,导管伸到试管底部药品上方
氢气还原氧化铜
24.[提出问题]铝片放到稀硫酸中为什么没有现象? (1分)
[猜想]可能是铝片表面生成的致密氧化膜阻碍了反应的发生;
或可能与稀硫酸的浓度有关;
或可能是铝片与稀硫酸反应需要加热;
或Cl-可以加快铝与酸的反应。 (1分)
[设计方案]
方案一
操作步骤(用图示说明或文字叙述均可) (2分)
可能观察到的实验现象
(1分)
相应的结论
(1分)
将打磨后的铝片放入试管中,加入10%的稀硫酸
若有气泡产生
若没有气泡产生
猜想正确
猜想错误
方案二
操作步骤(用图示说明或文字叙述均可) (2分)
可能观察到的实验现象
(1分)
相应的结论
(1分)
取一支试管,放入一块铝片,加入30%的稀硫酸少许
若有气泡产生
若没有气泡产生
猜想正确
猜想错误
方案三
操作步骤(用图示说明或文字叙述均可) (2分)
可能观察到的实验现象
(1分)
相应的结论
(1分)
取一支试管,放入一块铝片,加入10%的稀硫酸少许,然后加热
若有气泡产生
若没有气泡产生
猜想正确
猜想错误
方案四
操作步骤(用图示说明或文字叙述均可) (2分)
可能观察到的实验现象
(1分)
相应的结论
(1分)
取一支试管,放入一块铝片,加入10%的稀硫酸少许,然后加入氯化钠
若有气泡产生
若仍然没有气泡产生
猜想正确
猜想错误
(只要猜想合理,且设计的方案与猜想一致均得分)
[评价与反思]: 善于发现问题,大胆质疑,勇于探究 (1分)
( 其他答案合理均得分)
25.(1) 89 (2)15.7%
26.解:设该脱氧保鲜剂最多能够吸收氧气的质量为x。
4Fe+6H2O+3O2=== 4Fe(OH)3 (1分)
224 96
 (1分)
(1分)
x=
能够吸收氧气的体积= (1分)
(1分)
包装盒内的空气所含氧气的体积为
答:一袋脱氧保鲜剂能将包装盒内的氧气吸收干净。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com