
题目列表(包括答案和解析)


(12分)Q、W、X、Y、Z是原子序数逐渐增大的短周期元素。已知Q在所有原子中的原子半径最小,W是形成化合物种类最多的元素,Y的最外层电子数是内层电子数的3倍,Y和Z能形成原子个数比为1:1和1:2的两种离子化合物。(注:答题应根据题目要求,用元素符号或化学式来表示对应元素或物质)
(1)Z的离子结构示意图
(2)为了提高工业合成XQ3产率(该反应为放热反应),下列措施合理的是
a.升高温度
b.加入催化剂
c.将XQ3分离出去
d.增大反应体系压强
(3)WQ4与Y2反应通过下图装置可将化学能转化为电能。b电极反应式为

(4)标况下2.24LWY2被200mL 1 mol/LZYQ溶液吸收,所得溶液阴离子浓度从大到小的顺序是
(5)下图为某反应体系各物质(均为气体)的量及能量关系,该反应的热化学方程式为 。

(6)X和Z组成的一种离子化合物,能与水反应生成两种碱,其化学方程式是 。
(12分)Q、W、X、Y、Z是原子序数逐渐增大的短周期元素。已知Q在所有原子中的原子半径最小,W是形成化合物种类最多的元素,Y的最外层电子数是内层电子数的3倍,Y和Z能形成原子个数比为1:1和1:2的两种离子化合物。(注:答题应根据题目要求,用元素符号或化学式来表示对应元素或物质)
(1)Z的离子结构示意图
(2)为了提高工业合成XQ3产率(该反应为放热反应),下列措施合理的是
a.升高温度
b.加入催化剂
c.将XQ3分离出去
d.增大反应体系压强
(3)WQ4与Y2反应通过下图装置可将化学能转化为电能。b电极反应式为
(4)标况下2.24LWY2被200mL 1 mol/LZYQ溶液吸收,所得溶液阴离子浓度从大到小的顺序是
(5)下图为某反应体系各物质(均为气体)的量及能量关系,该反应的热化学方程式为 。
(6)X和Z组成的一种离子化合物,能与水反应生成两种碱,其化学方程式是 。
(12分)Q、W、X、Y、Z是原子序数逐渐增大的短周期元素。已知Q在所有原子中的原子半径最小,W是形成化合物种类最多的元素,Y的最外层电子数 是内层电子数的3倍,Y和Z能形成原子个数比为1:1和1:2的两种离子化合物。(注:答题应根据题目要求,用元素符号或化学式来表示对应元素或物质)
是内层电子数的3倍,Y和Z能形成原子个数比为1:1和1:2的两种离子化合物。(注:答题应根据题目要求,用元素符号或化学式来表示对应元素或物质)
(1)Z的离子结构示意图
(2)为了提高工业合成XQ 3产率(该反应为放热反应),下列措施合理的是
3产率(该反应为放热反应),下列措施合理的是
a.升高温度
b.加 入催化剂
入催化剂
c.将XQ3分离出去
d.增大反应体系压强
(3)WQ4与Y2反应通过下图装置可将化学能转化为电能。b电极反应式为 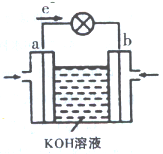
(4)标况下2.24LWY2被200mL 1 mol/LZYQ溶液吸收,所得溶液阴离子浓度从大到小的顺序是 
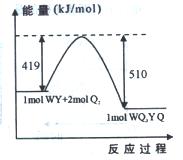
(5)下图为某反应体系各物质(均为气体)的量及能量关系,该反应的热化学方程式为 。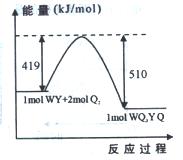
(6)X和Z组成的一种离子化合物,能与水反应生成两种碱,其化学方程式是 。
 是内层电子数的3倍,Y和Z能形成原子个数比为1:1和1:2的两种离子化合物。(注:答题应根据题目要求,用元素符号或化学式来表示对应元素或物质)
是内层电子数的3倍,Y和Z能形成原子个数比为1:1和1:2的两种离子化合物。(注:答题应根据题目要求,用元素符号或化学式来表示对应元素或物质) 3产率(该反应为放热反应),下列措施合理的是
3产率(该反应为放热反应),下列措施合理的是  入催化剂
入催化剂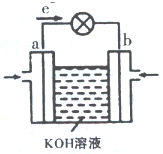

一、选择题
题号
1
2
3
4
5
6
7
8
答案
C
D
B
C
D
C
A
B
二、非选择题
.files/image014.jpg) 26. (1)HClO4
(2分)
26. (1)HClO4
(2分)
(2) (2分)离子键和非极性共价键(2分)
(3) Cl2+2OH-==Cl-+ClO-+H2O (3分) (4) 2Cl-+2H2O电解Cl2+H2+2OH- (3分)
(5) 2HCl(g)==H2(g)+Cl2(g);DH=+184.6kJ×mol-1 (3分)
27.(1)沸腾炉(2分) H2O2 (2分)O=C=O(2分)
(2)4FeS2+11O2高温2Fe2O3+8SO2 (2分) (3) C+H2O高温CO+H2 (2分)
(4) bh (2分) (5) CO2 +2NH3 高压CO(NH2)2+H2O (3分)
28.(1)检查装置气密性(2分)
(2)药品:碱石灰 (2分) 作用:吸收NH4Cl 受热分解产生的HCl(3分)
(3)防止倒吸(2分) (4)D (2分)
(5)A中石蕊变红且不褪色说明生成了HCl;(2分)D中酚酞变红说明生成了NH3
29.(1)①②④(3分) (2)羧基(2分)
(3)CH3CH2CH2CH=CH2+Br2 ®CH3CH2CH2CHBrCH2Br (3分)
(4) CH3CH(CH3)CH2COOH CH3CH2CH(CH3)COOH (4分)
(5) (3分)
CH3CH2CH2CH2CHO+2Ag(NH3)2OH.files/image016.jpg) CH3CH2CH2CH2COONH4+3NH3+2Ag¯+H2O
CH3CH2CH2CH2COONH4+3NH3+2Ag¯+H2O
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com