
题目列表(包括答案和解析)
下表为元素周期表的一部分。请回答下列问题:
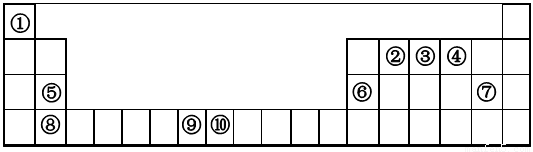
根据元素在周期表中的相对位置可知①~⑩分别是H、C、N、O、Mg、Al、Cl、Ca、Mn、Fe。
(1)上述元素中,属于s区的是____________(填元素符号)。
(2)写出元素④的基态原子的价电子排布图____________________。
(3)元素第一电离能为⑨________⑩ (填“大于”或“小于”)。
(4)元素③气态氢化物的VSEPR模型为________;该分子为________分子(填“极性”或“非极性”)。向硫酸铜溶液中逐滴加入其水溶液,可观察到的现象为_____________________________。
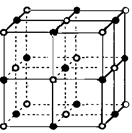
(5)⑥单质的晶体中原子的堆积方式如下图甲所示,其晶胞特征如下图乙所示,原子之间相互位置关系的平面图如下图丙所示。
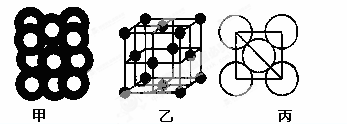
若已知⑥的原子半径为dcm,NA代表阿伏加德罗常数,元素⑥的相对原子质量为M,请回答:晶胞中⑥原子的配位数为 ,该晶体的密度为 (用字母表示)
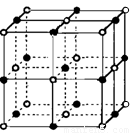
(6)实验证明:⑤和⑧的氧化物、KCl、TiN这4种晶体的结构与NaCl晶体结构相似(如下图所示),已知3种离子晶体的晶格能数据如下表:
|
离子晶体 |
NaCl |
KCl |
CaO |
|
晶格能/kJ·mol-1 |
786 |
715 |
3401 |
则该4种离子晶体(不包括NaCl)熔点从高到低的顺序是: (用化学式填写)。
其中⑧的氧化物晶体中一个阳离子周围和它最邻近且等距离的阳离子有 个。
下表为元素周期表的一部分。请回答下列问题:
根据元素在周期表中的相对位置可知①~⑩分别是H、C、N、O、Mg、Al、Cl、Ca、Mn、Fe。
(1)上述元素中,属于s区的是____________(填元素符号)。
(2)写出元素④的基态原子的价电子排布图____________________。
(3)元素第一电离能为⑨________⑩ (填“大于”或“小于”)。
(4)元素③气态氢化物的VSEPR模型为________;该分子为________分子(填“极性”或“非极性”)。向硫酸铜溶液中逐滴加入其水溶液,可观察到的现象为_____________________________。
(5)⑥单质的晶体中原子的堆积方式如下图甲所示,其晶胞特征如下图乙所示,原子之间相互位置关系的平面图如下图丙所示。
若已知⑥的原子半径为dcm,NA代表阿伏加德罗常数,元素⑥的相对原子质量为M,请回答:晶胞中⑥原子的配位数为 ,该晶体的密度为 (用字母表示)
(6)实验证明:⑤和⑧的氧化物、KCl、TiN这4种晶体的结构与NaCl晶体结构相似(如下图所示),已知3种离子晶体的晶格能数据如下表:
| 离子晶体 | NaCl | KCl | CaO |
| 晶格能/kJ·mol-1 | 786 | 715 | 3401 |

| 离子晶体 | NaCl | KCl | CaO |
| 晶格能/kJ·mol-1 | 786 | 715 | 3401 |
| B | C | D | ||
| A | E |
| ||
| ||
(9分)短周期主族元素A、B、C、D、E在元素周期表中的位置如图所示。请回答下列问题:
| | B | C | D | |
| A | | | | E |
1D 2 D 3B 4D 5A
6、A 7、C 8、B 9、D 10、D 11、A 12、B 13、D
14.D 15.A 16.D 17.ABD 18.D 19.B 20.AD 21.BC
22.⑴(4分)1.880~1.882mm ,23.20mm
⑵(4分)C
⑶①(3分)A、C、E ②(3分)A表外接、变阻器分压接法(如图) ③(4分)(如图)

23.(15分)
设x1表示未加F时弹簧的压缩量,由胡克定律和牛顿运动定律可知
 ①(2分)
①(2分)
设x2表示B刚要离开地面时弹簧的伸长量,a表示此时A的加速度,由胡克定律和牛顿运动定律可知
 ②(3分)
②(3分)
 ③(3分)
③(3分)
由②③式可得  ④(2分)
④(2分)
由题意得d=x1+x2 ⑤(2分)由①②⑤可得 ⑥(3分)
⑥(3分)
24.(19分)
所以EkxO=EkxO′=20 J(4分)
因竖直方向做自由落体运动,且tOA=tO′A,
所以yOA∶yAO′=1∶3;所以yOA∶yOO′=1∶4 (4分)
v =2gy,所以
=2gy,所以 mv
mv =mgy(3分)
=mgy(3分)
EkyA∶EkyO′=1∶4(3分)
EkyA=50 J,所以EkyO′=200 J(3分)
所以O′点的动能:EkO′=EkxO′+EkyO′=220 J(2分)
25.(20分)
解:(1)(8分)由题意可知:
m 、M之间的最大静摩擦力f=μ(mg+qE)=4N (2分)
m 、M一起运动的最大加速度 (2分)
(2分)
 (2分)
(2分)
 (2分)
(2分)
⑵(12分) 








S=2m 
 26(14)
26(14)
(1) Al Cl2 (各2分,共4分)

27(14分)
(1)Cu
(2)4Al+3O2 2Al2O3, 3CuO+2Al
2Al2O3, 3CuO+2Al 3Cu+Al2O3
3Cu+Al2O3
(3)Al2O3+6H+===2Al3+3H2O
(4)0.1 5.4g c(Cl-)>c(Al3+)>c(K+)+c(H+)>c(OH-)
28、(15分,方程式每空3分,别的每空2分)
(1)B:O C:Na 
(2) (3)H2O2+SO32- = SO42- + H2O
(3)H2O2+SO32- = SO42- + H2O

29. (15分,方程式每空3分,别的每空2分,以此为准)
注意:有的H打成了n,或位置对得不准,请各老师自行纠正。

(2)水解(取代)反应、消去反应、加聚反应
|