
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
ЮвЙњЛЗОГПеЦјжЪСПБъзМжаЖдSO2ЕФзюИпХЈЖШЯожЕШчЯТБэЃК
| ХЈЖШЯожЕ(mg•m-3) | ||
| вЛМЖБъзМ | ЖўМЖБъзМ | Ш§МЖБъзМ |
| 0.15 | 0.50 | 0.70 |
ДгПЮБОЩЯСЫНтЕНЫсгъЕФЮЃКІКЭГЩвђКѓЃЌЭЌбЇУЧЯыЕНЃК
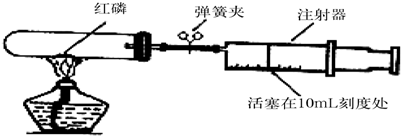
[ЬсГіЮЪЬт]ФГЛ№СІЗЂЕчГЇжмЮЇЕФПеЦјжаSO2КЌСПгІЪєгкМИМЖБъзМЃПЫћУЧОіЖЈШЅЪЕЕиВтЪдЁЃГіЗЂЧАЃЌЫћУЧзіСЫвдЯТзМБИЙЄзїЃК
[ВщдФзЪСЯ] ЂйЛ№СІЗЂЕчГЇЭЈГЃгУКЌСђУКЮЊдСЯЗЂЕчЁЃ
ЂкSO2ФмБЛЕтЕЅжЪ(I2)бѕЛЏЃК
SO2+I2+2H2OЃНH2SO4+2HIЁЃ
ЂлПеЦјжаЕФЦфЫћГЩЗжВЛгыЕтЫЎЗДгІЁЃ
[ЩшМЦЪЕбщ]Ђйдк5mLвЛЖЈжЪСПЗжЪ§ЕФЕтЫЎжаЕЮШы2ЁЂ3ЕЮЕэЗлШмвКЃЌЕУЕН ЁЁЁЁ ЩЋЕФШмвКAЃЈЕэЗлЪЧЧЁКУЭъШЋЗДгІЕФжИЪОМСЃЉЃЛ
ЂкНЋAШмвКГщШывЛжЇ500mLзЂЩфЦїжаЃЛ
ЂлГщШЁД§ВтЦјЬхЃЌгУНКШћЖТзЁеыПзГфЗжеёЕДКѓЃЌНЋзЂЩфЦїЮќПкГЏЩЯаЁаФХХГігрЦјЃЈВЛвЊАбШмвКХХГіЃЉЁЃЗДИДГщЦјеёЕДЃЌЕБШмвКБфЮЊЮоЩЋЪБЭЃжЙЁЃ
[ЪЕЕиВтЪд]РДЕНЗЂЕчГЇИННќЃЌЭЌбЇУЧЗжГЩМзЁЂввСНзщЃЌгУЯрЭЌЕФЪЕбщзАжУКЭШмвКAЃЌАДЩЯЪіЗНЗЈдкЭЌвЛЕиЕуЭЌЪБВтСПЃЌВЂЭЌЪБЭъГЩЪЕбщЁЃМЧТМГщЦјДЮЪ§ЃЌзМШЗЛЛЫуГЩУПСЂЗНУзПеЦјжаЫљКЌSO2ЕФжЪСПЁЃЪЕбщЪ§ОнЬюШыСЫЯТБэЃЈУПДЮГщЦјЬхЛ§ЮЊ450mLЃЉЃК
| Зжзщ | Мззщ | ввзщ |
| ГщЦјДЮЪ§/ДЮ | 100 | 120 |
| SO2КЌСП/(mg•m-3) | 0.53 | 0.46 |
[НЛСїгыЬжТл]ЭЌбЇУЧЗжЮіЪЕбщВйзїЙ§ГЬКЭВтЪдЪ§ОнКѓЗЂЯжЃЌ ЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁ ЃЈбЁЬюЁАМззщЁБЛђЁАввзщЁБЃЉЕФЪЕбщНсЙћЮѓВюНЯДѓЃЌВњЩњЮѓВюЕФдвђЪЧЃК
ЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЃЈСНзщЫљгУЕФзАжУКЭвЉЦЗОљЮоЮЪЬтЃЉЁЃ
[ЬНОПНсТл]ЭЌбЇУЧИљОнздШЯЮЊНЯзМШЗЕФЪ§ОнХаЖЯЃЌИУЛ№СІЗЂЕчГЇжмЮЇПеЦјжаSO2ЕФКЌСПЪєгк
МЖБъзМЁЃ
[ЗДЫМгыЦРМл]РЯЪІдкСЫНтЭЌбЇУЧЕФећИіЬНОПЙ§ГЬКѓжИГіЃКЁАвђЮЊФуУЧЕФВтЪдЕиЕуКЭЪБМфЕЅвЛЃЌЫљвдЕУГіЕФНсТлЕФПЩаХЖШВЛИпЁЃЁБЭЌбЇУЧШЯЮЊРЯЪІЕФЦРМлЪЧЖдЕФЃЌгкЪЧЖдздМКЕФЪЕЕиВтЪдЗНАИзїГіСЫвдЯТЕїећЃК
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
дкАДЪщБОзАжУВтЖЈПеЦјжабѕЦјКЌСПЕФЪЕбщЪБЃЌЕБзАжУФкЕФбѕЦјЕЭгквЛЖЈКЌСПЪБЃЌКьСзОЭВЛдйгыбѕЦјЗДгІЃЌДгЖјЕМжТВтСПНсЙћЦЋаЁЁЃгаРЯЪІЖдИУЪЕбщНјааСЫИФНјЃЌзАжУШчЭМЫљЪОЁЃдквЛШнЦїжаЕЙШЫИеВ№ЗтЕФЁАХЏБІБІЁБКкЩЋЗлФЉЃЌдйдкЩЯУцЗХзуСПЕФАзСзЃЌбИЫйПлЩЯЩеБЃЌЫцКѓАзСзздШМЃЌРћгУетвЛзАжУПЩИќзМШЗЕиВтЖЈПеЦјжабѕЦјЕФЬхЛ§ЗжЪ§ЁЃ
ЃЈ1ЃЉКкЩЋЗлФЉЕФжївЊГЩЗжЪЧЪВУД?ЖдДЫЭЌбЇУЧзіГіСЫвдЯТСНжжВТЯыЃК
ВТЯывЛЃКИУЗлФЉПЩФмЪЧФОЬПЗлЃЛ
ВТЯыЖўЃКИУЗлФЉПЩФмЪЧЬњЗлЁЃ
ИљОнбЇЙ§ЕФПЦбЇжЊЪЖЃЌгаЭЌбЇШЯЮЊВТЯывЛПЯЖЈЪЧДэЮѓЕФЃЌФуШЯЮЊЫћЕФРэгЩЪЧ ЁЃ
ЃЈ2ЃЉЭЈЙ§ЪЕбщжЄУїМгШыЕФКкЩЋЗлФЉЪЧЬњЗлЁЃМгШыЬњЗлКѓЪЙВтЖЈНсЙћИќМгзМШЗЃЌдвђЪЧ ЁЃ
дкАДЪщБОзАжУВтЖЈПеЦјжабѕЦјКЌСПЕФЪЕбщЪБЃЌЕБзАжУФкЕФбѕЦјЕЭгквЛЖЈКЌСПЪБЃЌКьСзОЭВЛдйгыбѕЦјЗДгІЃЌДгЖјЕМжТВтСПНсЙћЦЋаЁЃЎгаРЯЪІЖдИУЪЕбщНјааСЫИФНјЃЌзАжУШчЭМЫљЪОЃЌдквЛШнЦїжаЕЙШыИеВ№ЗтЕФЁАХЏБІБІЁБКкЩЋЗлФЉЃЌдйдкЩЯУцЗХзуСПЕФАзСзЃЌбИЫйПлЩЯЩеБЃЌЫцКѓАзСзздШЛЃЌРћгУетвЛзАжУПЩИќзМШЗЕиВтЖЈПеЦјжабѕЦјЕФЬхЛ§ЗжЪ§ЃЎ
ЃЈ1ЃЉКкЩЋЗлФЉЕФжївЊГЩЗжЪЧЪВУДЃПЖдДЫЭЌбЇУЧзіГіСЫвдЯТСНжжВТЯыЃК
ВТЯывЛЃКИУЗлФЉПЩФмЪЧФОЬПЗлЃЛ
ВТЯыЖўЃКИУЗлФЉПЩФмЪЧЬњЗлЃЎ
ИљОнбЇЙ§ЕФПЦбЇжЊЪЖЃЌгаЭЌбЇШЯЮЊВТЯывЛПЯЖЈЪЧДэЮѓЕФЃЌФуШЯЮЊЫћЕФРэгЩЪЧЁЁ
ЃЈ2ЃЉЭЈЙ§ЪЕбщжЄУїМгШыЕФКкЩЋЗлФЉЪЧЬњЗлЃЎМгШыЬњЗлКѓЪЙВтЖЈНсЙћИќМгзМШЗЃЌдвђЪЧЁЁ 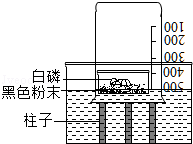
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com