(2007?海淀区一模)某种抗消化性溃疡的药品是碳酸钙和碳酸氢钠的混合物.某校课外小组同学设计实验验证该药品的成分,并探究各组分的质量比.
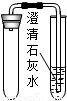
【查阅资料】部分内容如下:碳酸钙是白色固体,不溶于水;碳酸氢钠是白色固体,溶于水.碳酸氢钠受热易分解,反应方程式为2NaHCO
3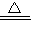
Na
2CO
3+H
2O+CO
2↑.
【实验验证】
(l)验证该药品中含有碳酸钙.
①称取4.2g该药品,加入50g水,充分溶解.(该温度下,碳酸氢钠的溶解度8.4g.)
②过滤步骤①得到的混合物,分别得到澄清透明的滤液和白色固体.①和②都要用到的玻璃仪器有______和______.
③将白色固体烘干,称量,质量为2.1g.
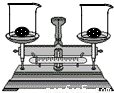
④将白色固体放入左侧试管中,加入稀盐酸,有无色气体生成,右侧试管中看到的现象是______.
【实验结论】该药品中含有碳酸钙.
根据此实验,推断该药品中碳酸钙和碳酸氢钠的质量比是______.
(2)验证该药品中含有碳酸氢钠.该小组同学提出了几种不同的方案.
方案1:取少量(l)中得到的滤液,滴加稀盐酸,生成一种可使燃着木条熄灭的无色气体.你认为该方案能否验证该药品中含有碳酸氢钠,并说明理由.______.
方案2:将(1)中得到的滤液加热蒸发,称量得到的白色固体质量为1.3g.白色固体质量远小于预测质量的原因是______.
该现象能够说明该药品中含有的另一种成份是碳酸氢钠.
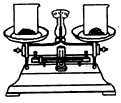
方案3:(如图)
①调节天平平衡.
②在左侧烧杯加入4.2g该药品,右侧烧杯中加入______,此时天平保持平衡.
③分别向两个烧杯中滴加等量的稀盐酸,至不再有固体剩余.天平仍保持平衡.
该现象能够说明该药品中含有的另一种成份是碳酸氢钠.
你认为再学习哪些知识,也可以用来验证该药品中含有的另一种成份是碳酸氢钠.

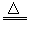 Na2CO3 +H2O +CO2 ↑ 。
Na2CO3 +H2O +CO2 ↑ 。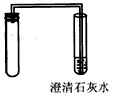
 Na2CO3+H2O+CO2↑.
Na2CO3+H2O+CO2↑. 
