
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
ЫЎКЭШмвКдкбЇЯАКЭЩњЛюжаЦ№зХЪЎЗжживЊЕФзїгУЃЎ
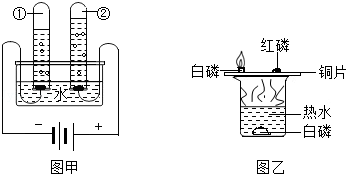
ЃЈ1ЃЉздШЛНчЕФЫЎОЙ§вЛЯЕСаОЛЛЏДІРэКѓЃЌГЩЮЊБШНЯЧхНрЕФздРДЫЎЃЎздРДЫЎВЛЪЧДПЫЎЃЌШєвЊжЦШЁДПЫЎЃЌгІВЩШЁЕФОЛЛЏЗНЗЈЪЧЁЁ ЁЁЃЎЭыЕњЩЯЕФгЭЮлгУздРДЫЎКмФбЯДОЛЃЌЭљЫЎжаЕЮМгЩйСПЯДЕгМСКѓЃЌОЭКмШнвзЯДОЛЃЌЫЕУїЯДЕгМСОпгаЁЁ ЁЁЙІФмЃЎ
ЃЈ2ЃЉЫЎдкЪЕбщЪвжагаВЛЭЌгУЭОЃЎ
ЂйШчЭММзЮЊЕчНтЫЎЕФзАжУЭМЃЌЦфЗДгІЗНГЬЪНЮЊЁЁ ЁЁЃЛ
ЂкШчЭМввЮЊЬНОПШМЩеЬѕМўЪЕбщЃЌЦфжаШШЫЎзїгУЁЁ ЁЁЃЎ
ЃЈ3ЃЉХЉвЕЩњВњГЃгУШмжЪЕФжЪСПЗжЪ§ЮЊ10%ЁЋ20%ЕФNaClШмвКРДбЁжжЃЎЯжНЋ200g 25%ЕФNaClШмвКЯЁЪЭЮЊ10%ЕФNaClШмвКЃЌашвЊМгЫЎЕФжЪСПЮЊЁЁ ЁЁgЃЎ
ЃЈ4ЃЉ20ЁцЪБЃЌNaClШмНтгкЫЎЕФЪЕбщЪ§ОнШчЯТБэЃЎдђЯТСаа№Ъіе§ШЗЕФЪЧЁЁ ЁЁЃЎ
|
ЪЕбщађКХ |
ЫЎЕФжЪСПЃЈgЃЉ |
МгШыNaClжЪСП |
ШмвКЕФжЪСП |
|
Ђй |
10 |
2 |
12 |
|
Ђк |
10 |
3 |
13 |
|
Ђл |
10 |
4 |
13.6 |
|
Ђм |
10 |
5 |
13.6 |
AЃЎЂйЫљЕУШмвКжаШмжЪжЪСПЗжЪ§ЮЊ16.7%
BЃЎЂкжаЫљЕУШмвКЪЧВЛБЅКЭШмвК
CЃЎ20ЁцЪБNaClЕФШмНтЖШЪЧ3.6ПЫ
DЃЎЂмШмвКжаШмжЪжЪСПЗжЪ§БШЦфгрШмвКжаШмжЪжЪСПЗжЪ§ЖМДѓЃЎ

| ЪЕбщађКХ | ЫЎЕФжЪСПЃЈgЃЉ | МгШыNaClжЪСП | ШмвКЕФжЪСП |
| Ђй | 10 | 2 | 12 |
| Ђк | 10 | 3 | 13 |
| Ђл | 10 | 4 | 13.6 |
| Ђм | 10 | 5 | 13.6 |
гавЛЦПШмвКЃЌПЩФмгЩBa(NO3)2ЁЂNaClЁЂNa2CO3ЁЂCuSO4ЁЂNa2SO4ЁЂCaCl2ЁЂNaOHЁЂHClЁЂFeCl3жаЕФвЛжжЛђМИжжзщГЩЃЎЯжНјааШчЯТЪЕбщЃК
(1)ШЁШмвКЩйаэЃЌЙлВьШмвКЮЊЮоЩЋЃЎ
(2)гУЪЏШяЪджНМьВтШмвКЃЌЪЏШяЪджНБфЮЊРЖЩЋЃЎ
(3)дкЩЯЪіШмвКМгШызуСПЯЁбЮЫсЃЌгаЮоЩЋЦјЬхВњЩњЃЎ
(4)дк(3)ЫљЕУШмвКжаМгШыЯѕЫсвјЃЌгаАзЩЋГСЕэВњЩњЃЎ
(5)дк(3)ЫљЕУШмвКжаМгШыТШЛЏБЕЃЌгаАзЩЋГСЕэВњЩњЃЎ
(6)АбдШмвКеєЗЂЃЌЕУЕНАзЩЋЙЬЬхЃЌАзЩЋЙЬЬхТЖжУгкПеЦјжаЃЌНсЙћБфГЩСЫЁАЫЎЁБЃЌАбЁАЫЎЁБЕЮдкЯДОЛЕФМІзІЩЯЃЌМІзІБЛИЏЪДСЫЃЁИљОнвдЩЯЯжЯѓЃЌХаЖЯИУШмвКзщГЩЃК
ПЯЖЈДцдкЕФ________ЃЛ
ПЯЖЈВЛДцдкЕФ________ЃЎ(ЖрЬюВЛЕУЗжЃЁ)
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com