
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
ФГаЃЛЏбЇаЁзщЖдШШЫЎКјЕзВПЫЎЙИЕФжївЊГЩЗнНјааСЫШчЯТЬНОПЃЌЧыЭъГЩвдЯТЛюЖЏЃЌВЂЛиД№ЯрЙиЮЪЬтЁЃ
ЁОВщдФзЪСЯЁПЬьШЛЫЎжаКЌгаCa2+ЁЂMg2+ЁЂHCO3-ЕШРызгЃЌдкМгШШЬѕМўЯТЃЌетаЉРызгЧїгкЩњГЩШмНтЖШИќаЁЕФЮяжЪ----ЫЎЙИЃЈжївЊГЩЗнЮЊЬМЫсбЮКЭМюЃЉЁЃгаЙиЮяжЪЕФШмНтадМћЯТБэЃК
ВПЗжИЦЁЂУОЛЏКЯЮяШмНтадБэЃЈ20ЁцЃЉ
| вѕРызг бєРызг | OH- | CO32- | HCO3- |
| Ca2+ | ЮЂШм | ВЛШм | ПЩШм |
| Mg2+ | ВЛШм | ЮЂШм | ПЩШм |
ЁОЬсГіВТЯыЁП
ВТЯывЛЃКЫЎЙИЕФГЩЗжЪЧ_______________
ВТЯыЖўЃКЫЎЙИЕФГЩЗжЪЧCaCO3ЁЂMg(OH)2ЁЂCa(0H)2
ВТЯыШ§ЃКЫЎЙИЕФГЩЗжЪЧCaCO3ЁЂMg(OH)2ЁЂMgCO3
ВТЯыЫФЃКЫЎЙИЕФГЩЗжЪЧCaC O3ЁЂMg(OH)2ЁЂCa(0H)2 MgCO3
O3ЁЂMg(OH)2ЁЂCa(0H)2 MgCO3
ЁОЗНАИЩшМЦЁП
ЃЈ1ЃЉШЗЖЈЫЎЙИжаЪЧЗёКЌгаЧтбѕЛЏИЦЃЈ2ЃЉШЗЖЈЫЎЙИжаЪЧЗёКЌгаЬМЫсУО
ЁОЪЕбщВНжшЁП
ЃЈ1ЃЉ
| ЪЕбщВНжш | ЪЕбщЯжЯѓ | ЪЕбщНсТл |
| дкЩйСПбаЫщЕФЫЎЙИжаМгШыЪЪСПЕФеєСѓЫЎГфЗжНСАшЃЌЙ§ТЫЃЌдйТЫвКжаМгШы_ | га___________ВњЩњ | ЫЎЙИжага ЧтбѕЛЏИЦ |
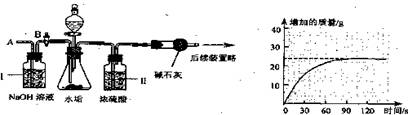
ЃЈ2ЃЉРћгУЯТЭМЪЕбщзАжУЭъГЩЃЈ2ЃЉЕФЬНОПЃЌЦфжївЊЪЕбщВНжшШчЯТЃК
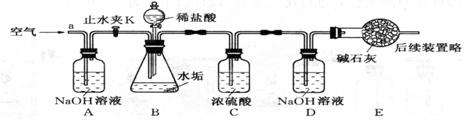
Ђё.ГЦСПDЁЂEзАжУзмжЪСПЮЊ400.00g
Ђђ.АДЩЯЭМзщзАКѓЃЌНЋ3gЫЎЙИбљЦЗЗХШызЖаЮЦПжаЃЌМгШызуСПЯЁбЮЫсжСзЖаЮЦПжаВЛдйВњЩњЦјХнЃЌЙиБеЗжвКТЉЖЗЛюШћ
Ђѓ.ДђПЊжЙЫЎМаKЃЌДгЕМЙмaДІЛКЛКЙФШыПеЦјЃЌвЛЖЮЪБМфКѓГЦСПзАжУDЁЂEЕФзмжЪСПЮЊ401.54gЃЈМюЪЏЛвжївЊГЩЗнЮЊCaOКЭNaOHЃЌВЛПМТЧзАжУФкПеЦјЖдЪЕбщЕФгАЯьЃЉЁЃ
ИљОнЪЕбщЛиД№ЯТСаЮЪЬтЃК
ЂйМгШыбљЦЗЧАЛЙгІ___________________ЃЌзАжУCЕФзїгУЪЧ__________,ЗДгІНсЪјКѓДђПЊжЙЫЎМаKЃЌЛКЛКЙФШыПеЦјЕФФПЕФЪЧ______________________________ ___________
___________
ЂкзАжУDжаЕФЛЏбЇЗНГЬЪНЮЊ_____________________________
ЂлзАжУBжаЩњГЩCO2ЕФжЪСПЮЊ_________gЃЌЫЎЙИжа______КЌMgCO3 ЁЃ
AЃЎвЛЖЈ B.вЛЖЈВЛ C.ПЩФм D.ЮоЗЈШЗЖЈ
ЁОЗДЫМбгЩьЁП
ШчКЮжЄУїЫЎЙИжаШЗЪЕгаЧтбѕЛЏУОЃЌаЁЛЊЬсГіСЫздМКЕФЯыЗЈЃК
СэШЁжЪСПЮЊ3gЕФЫЎЙИЃЌМгШы3.65%ЕФЯЁбЮЫсгыжЎЗДгІЃЌВтЕУЯћКФЯЁбЮЫсWgЃЌНсКЯвдЩЯЪЕбщНсТлЃЌХаЖЯWЕФжЕТњзу_____________ЬѕМўЪБЃЌЫЎЙИжавЛЖЈКЌгаMg(OH)2ЁЃ
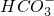 ЕШРызгЃЎ
ЕШРызгЃЎ| ЮяжЪ | CaЃЈHCO3ЃЉ2 | MgЃЈHCO3ЃЉ2 | CaЃЈOHЃЉ2 | MgЃЈOHЃЉ2 | CaCO3 | MgCO3 |
| ШмНтад | ПЩШм | ПЩШм | ЮЂШм | ВЛШм | ВЛШм | ЮЂШм |
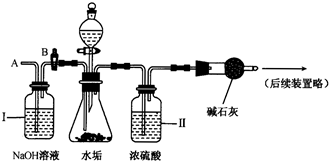
ФГаЃЛЏбЇаЁзщЖдШШЫЎКјЕзВПЫЎЙИЕФжївЊГЩЗжНјааСЫ'ШчЯТЬНОПЃЌЧыЭъГЩвдЯТЛюЖЏВЂЛиД№ЯрЙиЮЪЬтЁЃ
ЁОВщдФзЪСЯЁП
ЬьШЛЫЎжаКЌга![]() ЁЂ
ЁЂ![]() ЁЂ
ЁЂ![]() ЕШРызгЃЌдкМгШШЬѕМўЯТЃЌетаЉРызгЧїгкЩњГЩШмНтЖШИќаЁЕФЮяжЪЈDЈDЫЎЙИЃЈжївЊГЩЗжЮЊЬМЫсбЮКЭМюЃЉЁЃгаЙиЮяжЪЕФШмНтадМћЯТБэЃК
ЕШРызгЃЌдкМгШШЬѕМўЯТЃЌетаЉРызгЧїгкЩњГЩШмНтЖШИќаЁЕФЮяжЪЈDЈDЫЎЙИЃЈжївЊГЩЗжЮЊЬМЫсбЮКЭМюЃЉЁЃгаЙиЮяжЪЕФШмНтадМћЯТБэЃК
ВПЗжИЦЁЂУОЛЏКЯЮяШмНтадБэЃЈ20ЁцЃЉ
| вѕРызг бєРызг |
|
|
|
|
| ЮЂШм | ВЛШм | ПЩШм |
|
| ВЛШм | ЮЂШм | ПЩШм |
ЁОЬсГіВТЯыЁП
ЫЎЙИЕФжївЊГЩЗжжавЛЖЈКЌга КЭ ЃЌПЩФмКЌгаCaЃЈOHЃЉ2КЭMgCO3ЃЈЬюЛЏбЇЪНЃЉЁЃ
ЁОЩшМЦЗНАИЁП
ЪЕбщ1ЃКШЗЖЈЫЎЙИжаЪЧЗёКЌCaЃЈOHЃЉ2КЭCaCO3ЁЃ
| ЪЕбщВНжш | ЪЕбщЯжЯѓ | НсТл |
| дкЩйСПбаЫщЕФЫЎЙИжаЃЌМгШыЪЪСПЕФеєСѓЫЎГфЗжНСАшЃЌЙ§ТЫЃЌдкТЫвКРяМгШыNa2CO3ШмвК | УЛгаАзЩЋГСЕэВњЩњ | _________________________ |
ЪЕбщ2ЃКШЗЖЈЫЎЙИЪЧЗёКЌMgCO3ЁЃ
РћгУЯТСаЪЕбщзАжУЃЌЭъГЩЪЕбщ2ЬНОПЁЃЦфжївЊЪЕбщВНжшШчЯТЃК
ГЦСПDЁЂEзАжУзмжЪСПЮЊ600.00gЃЌАДЩЯЭМзщзАКѓЃЌНЋ2.50gЫЎЙИЪдбљЗХШызЖаЮЦПжаЃЌМгШызуСПЯЁбЮЫсШмвКЃЌД§зЖаЮЦПжаВЛдйВњЩњЦјХнЪБЃЌДђПЊжЙЫЎМаKЃЌДгЕМЙмaДІЛКЛКЙФШыПеЦјЃЌвЛЖЮЪБМфКѓГЦСПзАжУDЁЂEЕФзмжЪСПЮЊ601.25gЃЈМюЪЏЛвжївЊГЩЗжЮЊCaOКЭNaOHЃЌВЛПМТЧзАжУФкПеЦјЖдЪЕбщЕФгАЯьЃЉЁЃ
ЁОЪЕбщЬжТлЁП
ЃЈ1ЃЉМгШыбљЦЗЧАЛЙгІ ЃЌзАжУBжаЪЂЗХЯЁбЮЫсЕФвЧЦїУћГЦЮЊ ЃЌзАжУCЕФзїгУЪЧ ЃЌЗДгІНсЪјКѓДђПЊжЙЫЎМаKЃЌЛКЛКЙФШыПеЦјЕФФПЕФЪЧ ЃЌзАжУAЕФзїгУЪЧ ЁЃAЁЂBзАжУжЎМф ЩшжУИЩдязАжУЃЈЬюЁАвЊЁБЁЂЁАВЛвЊЁБЃЉЃЌЦфРэгЩЪЧ ЁЃ
ЃЈ2ЃЉзАжУBжаЩњГЩЦјЬхЕФЛЏбЇЗДгІЗНГЬЪНЮЊ ЃЈжЛвЊЧѓаДвЛжжЃЉЃЌзАжУDжаЕФЛЏбЇЗДгІЗНГЬЪНЮЊ ЁЃ
ЃЈ3ЃЉзАжУBжаЩњГЩCO2ЕФжЪСПЮЊ gЁЃЭЈЙ§МЦЫуЫЕУїЫЎЙИжа КЌMgCO3ЃЈЬюзжФИЃЉЁЃ
AЃЎвЛЖЈ BЃЎвЛЖЈВЛ CЃЎПЩФм DЃЎЮоЗЈШЗЖЈ
МЦЫуЙ§ГЬЃЈвбжЊЮяжЪЯрЖдЗжзгжЪСПCaCO3ЃК100ЃЌMgCO3ЃК84ЃЉЃК
ЪЕбщ3ЃКШЗЖЈЫЎЙИжаЪЧЗёКЌгаMgЃЈOHЃЉ2ЁЃ
СэШЁжЪСПЮЊ2.50gЫЎЙИЃЌМг3.65ЃЅЯЁбЮЫсгыжЎЗДгІЃЌВтЕУЯћКФЯЁбЮЫс![]() gЁЃНсКЯвдЩЯЪЕбщНсТлЃЌХаЖЯЕБ
gЁЃНсКЯвдЩЯЪЕбщНсТлЃЌХаЖЯЕБ![]() ЕФжЕТњзу ЬѕМўЪБЃЌЫЎЙИжавЛЖЈКЌгаMgЃЈOHЃЉ2ЃЈЧыЭЈЙ§МЦЫуЫЕУїЃЉЁЃ
ЕФжЕТњзу ЬѕМўЪБЃЌЫЎЙИжавЛЖЈКЌгаMgЃЈOHЃЉ2ЃЈЧыЭЈЙ§МЦЫуЫЕУїЃЉЁЃ
 ЕШРызгЃЎ
ЕШРызгЃЎ| ЮяжЪ | CaЃЈHCO3ЃЉ2 | MgЃЈHCO3ЃЉ2 | CaЃЈOHЃЉ2 | MgЃЈOHЃЉ2 | CaCO3 | MgCO3 |
| ШмНтад | ПЩШм | ПЩШм | ЮЂШм | ВЛШм | ВЛШм | ЮЂШм |

ЁОбаОППЮЬтЁПЃКЬНОПШШЫЎКјЕзВПЫЎЙИЕФжївЊГЩЗж
ЁОВщдФзЪСЯЁПЃКИУаЁзщЭЌбЇЭЈЙ§ВщдФзЪСЯжЊЕРЃЌЬьШЛЫЎжавЛАуЖМКЌгаCa2+ЁЂMg2+ЁЂHCO3-ЕШРызгЃЌдкМгШШЪБЃЌетаЉРызгЧїгкЩњГЩШмНтЖШИќаЁЕФЮяжЪЈDЈDЫЎЙИЃЈжївЊГЩЗжЮЊЬМЫсбЮЁЂМюЕФЛьКЯЮяЃЉЁЃЭЌЪБЃЌЫћУЧЛЙВщдФЕНЯТСагаЙиЮяжЪЕФШмНтадЃК
| ЮяжЪ | CaЃЈHCO3ЃЉ2 | MgЃЈHCO3ЃЉ2 | CaЃЈOHЃЉ2 | MgЃЈOHЃЉ2 | CaCO3 | MgCO3 |
| ШмНтад | ПЩШм | ПЩШм | ЮЂШм | ВЛШм | ВЛШм | ЮЂШм |
ЁОЬсГіВТЯыЁПЃКЫЎЙИЕФжївЊГЩЗжвЛЖЈКЌгаMgЃЈOHЃЉ2КЭ ЃЌПЩФмКЌгаCaЃЈOHЃЉ2КЭ ЁЃ
ЁОЩшМЦЗНАИЁПЃК
ЃЈ1ЃЉМзЭЌбЇдкЩеБжаЗХШыЩйСПбаЫщЕФЫЎЙИЃЌМгШыЪЪСПеєСѓЫЎГфЗжНСАшЃЌШЁЩЯВуЧхвКМгШы ЃЌУЛгаАзЩЋГСЕэЃЌЫЕУїЫЎЙИжаЮоCaЃЈOHЃЉ2ЃЛ
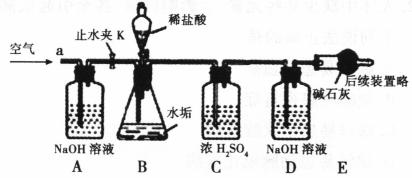
ЃЈ2ЃЉввЭЌбЇЩшМЦЯТСаЪЕбщзАжУЃЌНјвЛВНШЗЖЈЫЎЙИжаКЌгаЬМЫсбЮЕФГЩЗжЃЌВНжшШчЯТЃК
ЂйАДЭМзщзАвЧЦїЃЌНЋ50gЫЎЙИЪдбљЗХШызЖаЮЦПжаЃЌМгШызуСПФГЫсШмвКЃЛ
ЂкВтСПвЛЖЈЪБМфФкИЩдяЙмФкЮяжЪдіМгЕФжЪСПЃЈМћЯТСаЧњЯпЃЉЃЛ
ЂлД§зЖаЮЦПжаВЛдйВњЩњЦјХнЪБЃЌДђПЊЛюШћBЃЌДгЕМЙмAДІЛКЛКЙФШывЛЖЈСПЕФПеЦјЃЛ
ЂмдйДЮГЦСПИЩдяЙмФкЮяжЪдіМгЕФжЪСПЃЛ
ЂнжиИДЂлКЭЂмЕФВйзїЃЌжБжСИЩдяЙмФкЮяжЪжЪСПВЛБфЁЃ
aЃЎВНжшЂйЫљМгЕФЫсШмвКЪЧ ЃЛ
bЃЎзАжУЂђЕФзїгУЪЧ ЃЛДгЕМЙмAДІЛКЛКЙФШЫвЛЖЈСПЕФПеЦјЪБЃЌзАжУIЕФзїгУЪЧ ЃЛ
cЃЎбаОПадаЁзщЕФЭЌбЇОЙ§МђЕЅМЦЫуЃЌШЯЮЊЫЎЙИжавЛЖЈКЌгаMgCO3ЃЌРэгЩЪЧ ЁЃ
ЁОЪЕбщНсТлЁПЭЈЙ§ЩЯЪіЬНОППЩжЊЃКЫЎЙИЕФжївЊГЩЗжга ЁЃ
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com