
题目列表(包括答案和解析)

| ||
| ||
| ||
| ||
 过氧化氢(化学式H2O2)溶液在MnO2作催化剂的条件下能迅速分解生成O2和H2O.分液漏斗可以通过调节活塞控制液体的滴加速度.
过氧化氢(化学式H2O2)溶液在MnO2作催化剂的条件下能迅速分解生成O2和H2O.分液漏斗可以通过调节活塞控制液体的滴加速度.
| ||
| ||
| ||
| 实验步骤 | 实验现象 | 实验结论 |
| ①将等体积的两种无色液体分别加入A、B两个试管中. ②分别向A、B两试管中同时加入等质量(少量)的二氧化锰,观察现象. 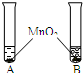 |
A试管中无明显现象 B试管中有气泡产生 |
A试管中的无色液体是: H2O H2O ;B试管中的无色液体是: H2O2 H2O2 ; |
| ||
| ||
| ||
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com