
题目列表(包括答案和解析)
按要求写出下列反应的化学方程式,并说明该反应在实际中的一种应用。
| 化学方程式 | 实验中的就用 | |
| 有红磷参加的化合反应 | ||
| 有氧化钙生成的分解反应 |
学习热情和学习方法是成才的必备条件,灵活掌握不同的学习方法可以取得事半功倍的效果.请用以下方法解决下列问题:
(1)分类法:利用下列4组物质请按要求填写下表空白(填写物质的化学式或分类标准)
(分类标准包括:酸、碱、盐、金属氧化物、非金属氧化物、金属单质、非金属单质)
A.ZnO、MgO、CO2、Na2O B.Cu、N2、C、Cl2
C.KNO3、NaHCO3、KClO3、Fe(OH)3 D.H2SO4、H2O、HCl、HNO3
| A | B | C | D | |
| 分类标准 | 金属氧化物 | 盐 | ||
| 不属于该类别的物质 | Cu | H2O |
(2)对比法:
A.通过对CO2+H2O→H2CO3 和 6CO2+6H2O 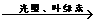 C6H12O6+6O2两个化学反应的
C6H12O6+6O2两个化学反应的
 对比,你能得出的结论是:相同的反应物在不同的条件下
对比,你能得出的结论是:相同的反应物在不同的条件下
.
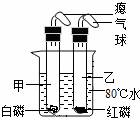
B.如图所示:小海同学将盛有干燥白磷的甲试管和干燥红磷的乙
试管插入盛有80℃的烧杯里(甲、乙试管均套有气球密封).过
一会后,发现甲试管中的白磷燃烧,乙试管中的红磷没有燃烧.请
根据小海同学的实验现象,对比得出可燃物燃烧所需的条件之
一: 。
(3)归纳演绎法:
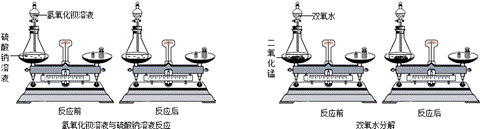
某同学通过对大量化学反应前后各物质的质量总和的测定分析(如上图中的氢氧化钡溶
液与硫酸钠溶液,用少量的双氧水和二氧化锰分解),得出参加化学反应的各物质的质量总和 (填“大于”、“小于”或“等于”)反应后生成的各种物质的质量总和.根据该同学得出的结论可推出:高温煅烧含有杂质的石灰石125g(杂质不发生反应),
充分反应后剩余固体质量为81g,则反应过程中生成二氧化碳的质量为 g。
请根据化学反应方程式列式计算①该石灰石中含碳酸钙的物质的量是多少?②该石灰石
中含碳酸钙的质量分数是多少?
请按要求填空。
(1)请写出相应的化学符号或名称
①2个磷原子 ;②+2价的锌元素 ;③2SO42- ;④2 H2O 。
(2)请在H、O、N、S、Cl、Na等6种元素中选择恰当的元素,组成符合下列要求的物质,并将其化学式填写在相对应的位置上
①一种重要化工产品,能使湿润的红色石蕊试纸变蓝的气体是 ;
②一种大气污染物,容易造成硫酸型酸雨的气体是 ;
③空气中含量最高的气体是 ;
④海水中含量最高的盐是 ;
⑤既可作为消毒剂,也可用于实验室制取氧气的液体试剂是 。
(3)请用化学方程式表示下列反应
①生石灰与水反应转变成熟石灰 ;
②高锰酸钾受热分解制氧气 ;
③盐酸和氢氧化钠的反应 。
一、 选择题(本大题共10题,每小题2分,共20分)每小题给出的四个选项中,只有一个最符合题意,请将其序号涂在答题卡上。
题号
1
2
3
4
5
6
7
8
9
10
答案
B
C
D
B
D
B
B
A
D
C
二、选择题(本大题共5题,每小题2分,共10分)每小题给出的四个选项中,有1~2个符合题意。只有一个选项符合题意的多选不给分;有2个选项符合题意的只选一个且符合题意给1分,若选2个有一个不符合题意则不给分。
题号
11
12
13
14
15
答案
BD
BC
AC
C
D
三、(本大题共5题 共23分)
16.(6分)(每空1分) (1)CO (2)干冰(3)排水法(4)石墨具有导电性(5)80(6)+5
17.(4分)(每空1分) (1)天然 合成 (2)铁 (3)③
18.(5分)(每空1分) (1)40(2)乙 甲 丙 (3)升高温度或加入丙物质或恒温蒸发水
(4)甲 丙
19.(5分)(每空1分) (1)CO2 (2)CO2 CH3COOH (3)石蕊试液 (4)2
20.(2分) 15:2
四、(本大题共4题 共37分)
(1)4P+5O2======2P2O5
(3)CO+CuO====Cu+CO2
(4)CuSO4+2NaOH ====Cu(OH)2↓+Na2SO4 (2)
22.(11分) (每空1分,化学方程式2分,最后一空2分)(1) CO2 Cu (2) Cu、Na2CO3、Cu(OH)2、CuO;Cu、Na2CO3、CuO;Cu、Na2CO3、Cu(OH)2;(3)CuSO4、H2SO4(4)CuO+H2SO4==CuSO4+H2O或Cu(OH)2+H2SO4==CuSO4+2H2O(5)NaOH,取溶液B少许滴加过量的BaCl2溶液静置(或过滤),取上层清液滴入酚酞,若变红色则含有NaOH,反之则无NaOH。
 23.(9分) (每空1分,化学方程式2分)(1)H2 Zn+H2SO4====ZnSO4+H2↑(2)①②③④⑥ (3)黑色粉末变红,试管内壁出现水珠 (4)酒精灯
23.(9分) (每空1分,化学方程式2分)(1)H2 Zn+H2SO4====ZnSO4+H2↑(2)①②③④⑥ (3)黑色粉末变红,试管内壁出现水珠 (4)酒精灯
2KMnO4=====K2MnO4+MnO2+O2↑ 将带火星的木条插入集气瓶中,若木条复燃,证明是氧气。
24.(9分)(每空1分) 实验一 B烧杯中的无色酚酞溶液变红
实验二 验证水和二氧化碳分别是否能使紫色石蕊变色 B
实验三
1
加入等体积的蒸馏水和氢氧化钠溶液,盖紧瓶塞,振荡。
加入氢氧化钠溶液的软塑料瓶比加入蒸馏水的软塑料瓶变得更瘪
2
加入足量的盐酸(或氯化钡溶液或澄清石灰水或氯化钙溶液或硝酸钡溶液……
冒气泡(或有白色沉淀生成……)
(说明:所写步骤、现象要匹配,其他合理答案均可给分)
方案1:通过密闭容器内气体压强变化的程度的对比来判断反应的发生(或通过反应物量的减少来判断反应的发生。)
方案2:通过验证生成物的存在来判断反应的发生。
五、(本大题共2题 共10分)
25.(3分)(每空1分)(1) (2)1290
(2)1290
(3)解法一: 解法二:
解法二:
26.(7分)(1) 碱 ;酸 (每空1分) (2)溶液的红色刚好褪去(1分)
(3)消耗掉的硫酸溶液质量:24.5mL×
消耗掉的硫酸溶液中溶质的质量:
解: 设待测液溶质质量为x
2NaOH + H2SO4 ===== Na2SO4+2 H2O
80 98
x
80 :98 = x :
x=
待测液溶质质量分数为
答: 待测液溶质质量分数为3.6%
本资料由《七彩教育网》www.7caiedu.cn 提供!
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com