
3.(13分)某研究性学习小组对过量炭粉与氧化铁反应的气体产物成分进行研究。
(1)提出假设:该反应的气体产物全部都是二氧化碳
(2)设计方案:如下图所示,将一定量的氧化铁在隔绝空气的条件下与过量炭粉完全反应,测量参加反应的碳元素与氧元素的质量比
(2)不正确 (1分)、 将
NH3+H2O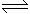 NH3?H2O
NH3?H2O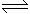 NH4++OH-平衡向左移动,有利于NH3挥发放出。
NH4++OH-平衡向左移动,有利于NH3挥发放出。
(4)NH3+CO2+NaC1+H2O=NaHCO3↓+NH
(5)C
II.(1)温度升高,促进NaHCO3水解
8.8
请你帮助乙同学完成下列内容:
(1)乙同学对产生上述现象原因的预测之一是:加热时NaHCO3受热分解生成了Na2CO3。
原因预测之二是 。
(2)查阅资料发现NaHCO3的分解温度为
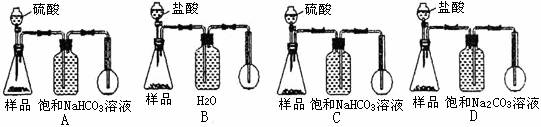
解析:本实验将定性分析和定量考查进行了有效融合,可很好的考查分析或处理实验数据,得出合理结论以及知识迁移和再加工的能力。 Ⅰ.由模拟实验的目的,结合NH3和CO2在饱和NaCl溶液中的溶解度的差异知,应先向饱和NaCl溶液中通入NH3至饱和,然后再通入CO2,这样可吸收大量的CO2,利于形成NaHCO3。结合装置可知A装置产生CO2中常混有HCl,应通入D装置中洗气,除去CO2中混有的HCl杂质后在通入C装置;装置B产生NH3可直接通入C装置,但因NH3极易溶解,应防止倒吸,故应接c(靠干燥管的球形部分防倒吸),故装置的连接顺序为:a→f→e→d;b→c。(5)本实验是通过测量液体的体积求出一定量的Na2CO3样品产生CO2的体积,进而求出Na2CO3样品的纯度。装置A、B是长进短出,故无法排出液体;D中Na2CO3可与CO2作用,故应选C装置。Ⅱ.(1)pH升高的另一原因是促进了HCO3-的水解;(2)因NaHCO3分解需要
答案:I.(1)f e d c (2分,错一项不得分)
(2)饱和NaHCO3溶液 (1分) 、防止发生倒吸 (1分) 、 漏斗 (1分)
(3)生石灰与水反应,放出大量热,生成物是强碱,都使
8.5
8.4
8.3
|