
33ЃЎЃЈ8ЗжЃЉ[ЛЏбЇ——гаЛњЛЏбЇЛљДЁ]
КЯГЩPЃЈвЛжжПЙбѕМСЃЉЕФТЗЯпШчЯТ
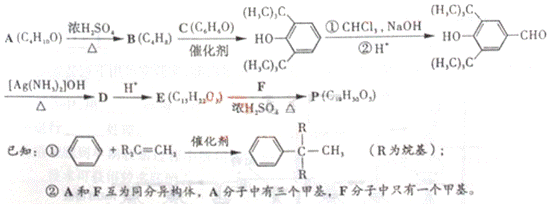
 ЃЈ1ЃЉAЁЁЁЁ BЕФЗДгІРраЭЮЊ______ЁЃBОДпЛЏМгЧтЩњГЩGЃЈC4H10ЃЉЃЌGЕФЛЏбЇУћГЦЪЧ_____ЁЃ
ЃЈ1ЃЉAЁЁЁЁ BЕФЗДгІРраЭЮЊ______ЁЃBОДпЛЏМгЧтЩњГЩGЃЈC4H10ЃЉЃЌGЕФЛЏбЇУћГЦЪЧ_____ЁЃ
ЃЈ2ЃЉAгыХЈHBrШмвКвЛЦ№ЙВШШЩњГЩHЃЌHЕФНсЙЙМђЪНЮЊ______ЁЃ
ЃЈ3ЃЉЪЕбщЪвжаМьбщCПЩбЁдёЯТСаЪдМСжаЕФ_______ЁЃ
aЃЎбЮЫсЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ b.FeCl3ШмвКЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ c.NaHCO3ШмвКЁЁЁЁЁЁЁЁ d.ХЈфхЫЎ
ЃЈ4ЃЉPгызуСПNaOHШмвКЗДгІЕФЛЏбЇЗДгІЗНГЬЪНЮЊ__________ЃЈгаЛњЮягУНсЙЙМђЪНБэЪОЃЉ.ЁЁ
32ЃЎЃЈ8ЗжЃЉ[ЛЏбЇ——ЮяжЪНсЙЙгыаджЪ]
Н№ЪєФјдкЕчГиЁЂКЯН№ЁЂДпЛЏМСЕШЗНУцгІгУЙуЗКЁЃ
ЃЈ1ЃЉЁЁЁЁЁЁ ЯТСаЙигкН№ЪєМАН№ЪєМќЕФЫЕЗЈе§ШЗЕФЪЧ_______ЁЃ
a.ЁЁЁЁЁЁ Н№ЪєМќОпгаЗНЯђадКЭБЅКЭад
b.ЁЁЁЁЁЁ Н№ЪєМќЪЧН№ЪєбєРызггыздгЩЕчзгМфЕФЯрЛЅзїгУ
c.ЁЁЁЁЁЁ Н№ЪєЕМЕчЪЧвђЮЊдкЭтМгЕчГЁзїгУЯТВњЩњздгЩЕчзг
d.ЁЁЁЁЁЁ Н№ЪєОпгаЙтдѓЪЧвђЮЊН№ЪєбєРызгЮќЪеВЂЗХГіПЩМћЙт
ЃЈ2ЃЉЁЁЁЁЁЁ NiЪЧдЊЫижмЦкБэжаЕк28КХдЊЫиЃЌЕкЖўжмЦкЛљЬЌдзгЮДГЩЖдЕчзгЪ§гыNiЯрЭЌЧвЕчИКадзюаЁЕФдЊЫиЪЧ______ЁЃ
ЃЈ3ЃЉЁЁЁЁЁЁ Й§ЖЩН№ЪєХфКЯЮяNiЃЈCOЃЉЕФжааФдзгМлЕчзгЪ§гыХфЬхЬсЙЉЕчзгзмЪ§жЎКЭЮЊ18ЃЌдђn=______ЁЃCOгыN2НсЙЙЯрЫЦЃЌCOЗжзгФкo- МќгкІаМќИіЪ§жЎБШЮЊ________ЁЃ
ЃЈ4ЃЉЁЁЁЁЁЁ МзШЉЃЈH2C=OЃЉдкNiДпЛЏзїгУЯТМгЧтПЩЕУМзДМЃЈCH2OHЃЉЁЃМзДМЗжзгФкCдзгЕФдгЛЏЗНЪНЮЊ________ЃЌМзДМЗжзгФкЕФO—C—HМќНЧ_______ЃЈЬюЁАДѓгкЁБЁАЕШгкЁБЛђЁАаЁгкЁБЃЉМзШЉЗжзгФкЕФO—C—HМќНЧЁЃ
31ЃЎЃЈ8ЗжЃЉ[ЛЏбЇ——ЛЏбЇгыММЪѕ]
ЪЏгЭКЭУКЬПМгЙЄЙ§ГЬЩцМАЖржжММЪѕКЭЩшБИЁЃ
ЃЈ1ЃЉЁЁЁЁЁЁ ЪЏгЭЗжСѓЪБЃЌдкВЛЖЯЯђ______ЃЈЬюЙЄвЕЩшБИУћГЦЃЉФкЭЖЗХдСЯЕФЭЌЪБЛёЕУВњЦЗЃЌИУЙ§ГЬЮЊ_______ВйзїЙ§ГЬЁЃ
ЃЈ2ЃЉЁЁЁЁЁЁ ЪЏгЭСбЛЏЗжЮЊШШСбЛЏЁЂ_______КЭМгЧтСбЛЏЃЌСбЛЏЕФФПЕФЪЧЬсИп_______ЕФВњСПЁЃ
ЃЈ3ЃЉЁЁЁЁЁЁ УКЕФЯДбЁЪЧЮЊСЫНЕЕЭдУКжаЛвЗжКЭ______ЕФКЌСПЁЃУКЕФСїЛЏДВШМЩеЪЧжИПеЦјДгЕзВПДЕЯђУКЬППХСЃЃЌВЂЪЙШЋВПУКЬППХСЃ_______НјааШМЩеЕФЙ§ГЬЁЃ
ЃЈ4ЃЉУКЕФжБНгвКЛЏЪЧУКгыЪЪЕБШмМСЛьКЯКѓдкИпЮТКЭ_______ДцдкЯТгы_______зїгУЩњГЩвКЬхШМСЯЕФЙ§ГЬЁЃ
30ЃЎЃЈ14ЗжЃЉЪЕбщЪвВЩгУMgCl2ЁЂAlCl3ЕФЛьКЯШмвКгыЙ§СПАБЫЎЗДгІжЦБИMgAl2O4ЃЌжївЊСїГЬШчЯТ
 ЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
MgCl2ЁЂAlCl3ЕФЛьКЯШмвКЃЈAЃЉ
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
MgCl2ЁЂAlCl3ЕФЛьКЯШмвКЃЈAЃЉ
 ЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
АБЫЎЃЈBЃЉ
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
АБЫЎЃЈBЃЉ





|
|
|
|
|
|
 ЁЁ
ЁЁ
ЃЈ1ЃЉЁЁЁЁЁЁ ЮЊЪЙMg2+ЁЂAl13+ЭЌЪБЩњГЩГСЕэЃЌгІЯШЯђГСЕэЗДгІЦї
жаМгШы________ЃЈЬюЁАAЁБЛђЁАBЁБЃЉЃЌдйЕЮМгСэвЛЗДгІЮяЁЃ
ЃЈ2ЃЉЁЁЁЁЁЁ ШчгвЭМЫљЪОЃЌЙ§ТЫВйзїжаЕФвЛДІДэЮѓЪЧ________ЁЃ
ЃЈ3ЃЉЁЁЁЁЁЁ ХаЖЯСїГЬжаГСЕэЪЧЗёЯДОЛЫљгУЕФЪдМСЪЧ________ЁЃ
ИпЮТБКЩеЪБЃЌгУгкЪЂЗХЙЬЬхЕФвЧЦїУћГЦЪЧ________ЁЃ
ЃЈ4ЃЉЁЁЁЁЁЁ ЮоЫЎAlCl3ЃЈ183ЁуCЩ§ЛЊЃЉгіГБЪЊПеЦјМДВњЩњДѓСПАзЮэЃЌ
ЪЕбщЪвПЩгУЯТСазАжУжЦБИЁЃ
ЁЁ
ЁЁ
ЁЁ
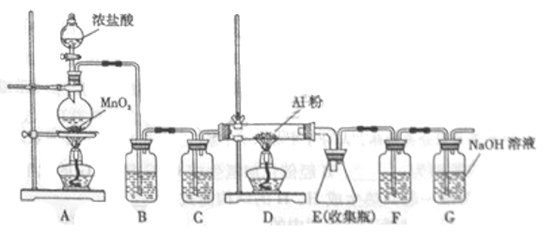
зАжУ BжаЪЂЗХБЅКЭNaClШмвКЃЌИУзАжУЕФжївЊзїгУЪЧ______ЁЃFжаЪдМСЕФзїгУЪЧ__________ЁЃ
гУвЛМўвЧЦїзАЬюЪЪЕБЪдМСКѓвВПЩЦ№ЕНFКЭGЕФзїгУЃЌЫљзАЬюЕФЪдМСЮЊ__________ЁЃ
[бЁзіВПЗж]
29.ЃЈ16ЗжЃЉЦЋЖўМзыТгыN2O4 ЪЧГЃгУЕФЛ№М§ЭЦНјМСЃЌЖўепЗЂЩњШчЯТЛЏбЇЗДгІЃК
(CH3)2NNH2
(Ђё)+2N2O4 (Ђё)=2CO2 (g)+3N2(g)+4H2O(g)ЃЈЂёЃЉ
(1)ЁЁЁЁ ЗДгІЃЈЂёЃЉжабѕЛЏМСЪЧ_______.
(2)ЁЁЁЁ
Л№М§ВаКЁжаГЃЯжКьзиЩЋЦјЬхЃЌдвђЮЊЃКN2O4 (g) 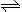 ЁЁ2NO2 (g)ЁЁ ЃЈЂђЃЉ
ЁЁ2NO2 (g)ЁЁ ЃЈЂђЃЉ
(3)ЁЁЁЁ вЛЖЈЮТЖШЯТЃЌЗДгІЃЈЂђЃЉЕФьЪБфЮЊІЄHЁЃЯжНЋ1 mol N2O4 ГфШывЛКубЙУмБеШнЦїжаЃЌЯТСаЪОвтЭМе§ШЗЧвФмЫЕУїЗДгІДяЕНЦНКтзДЬЌЕФЪЧ________.
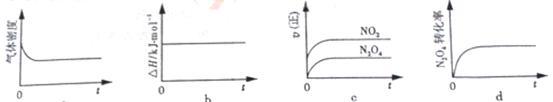
ШєдкЯрЭЌЮТЖШЯТЃЌЩЯЪіЗДгІИФдкЬхЛ§ЮЊ1LЕФКуШнУмБеШнЦїжаНјааЃЌЦНКтГЃЪ§________ЃЈЬюЁАдіДѓЁБЁАВЛБфЁБЛђЁАМѕаЁЁБЃЉЃЌЗДгІ3sКѓNO2ЕФЮяжЪЕФСПЮЊ0.6molЃЌдђ0~3sФкЕФЦНОљЗДгІЫйТЪvЃЈN2O4ЃЉ=________mol·L-1·S-1ЁЃ
ЃЈ4ЃЉNO2ПЩгУАБЫЎЮќЪеЩњГЩNH4NO3 ЁЃ25ЁцЪБЃЌНЋamol NH4NO3ШмгкЫЎЃЌШмвКЯдЫсадЃЌдвђЪЧ_____ЃЈгУРызгЗНГЬЪНБэЪОЃЉЁЃЯђИУШмвКЕЮМгbLАБЫЎКѓШмвКГЪжаадЃЌдђЕЮМгАБЫЎЕФЙ§ГЬжаЕФЫЎЕФЕчРыЦНКтНЋ______ЃЈЬюЁБе§ЯђЁБЁАВЛЁБЛђЁАФцЯђЁБЃЉвЦЖЏЃЌЫљЕЮМгАБЫЎЕФХЈЖШЮЊ_______mol·L-1ЁЃЃЈNH3·H2OЕФЕчРыЦНКтГЃЪ§ШЁKb=2X10-5 mol·L-1ЃЉ
28. ЃЈ12ЗжЃЉ ЙЄвЕЩЯгЩЛЦЭПѓЃЈжївЊГЩЗжCuFeS2ЃЉвБСЖЭЕФжївЊСїГЬШчЯТЃК

ЁЁ
ЃЈ1ЃЉЦјЬхAжаЕФДѓЦјЮлШОЮяПЩбЁгУЯТСаЪдМСжаЕФЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЮќЪеЁЃ
a. ХЈH2SO4ЁЁЁЁЁЁ b.ХЈHNO3 ЁЁЁЁЁЁЁЁc.NaOHШмвКЁЁЁЁЁЁ d.АБЫЎ
ЃЈ2ЃЉгУЯЁH2SO4 НўХнШлдќBЃЌШЁЩйСПЫљЕУШмвКЃЌЕЮМгKSCNШмвККѓГЪКьЩЋЃЌЫЕУїШмвКжаДцдк
ЁЁЁЁЁЁ ЃЈЬюРызгЗћКХЃЉЃЌМьбщШмвКжаЛЙДцдкFe2+ЕФЗНЗЈЪЧ ЁЁЁЁЁЁЁЁЃЈзЂУїЪдМСЁЂЯжЯѓЃЉЁЃ
ЃЈ3ЃЉгЩХнЭвБСЖДжЭЕФЛЏбЇЗДгІЗНГЬЪНЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЃ
ЃЈ4ЃЉвдCuSO4ШмвКЮЊЕчНтжЪШмвКНјааДжЭЃЈКЌAlЁЂZnЁЂAgЁЂPtЁЂAuЕШдгжЪЃЉЕФЕчНтОЋСЖЃЌЯТСаЫЕЗЈе§ШЗЕФЪЧЁЁЁЁЁЁЁЁ ЁЃ
a. ЕчФмШЋВПзЊЛЏЮЊЛЏбЇФмЁЁЁЁЁЁЁЁЁЁЁЁ b.ДжЭНгЕчдДе§МЋЃЌЗЂЩњбѕЛЏЗДгІ
c.ШмвКжаCu2+ЯђбєМЋвЦЖЏЁЁЁЁЁЁЁЁЁЁЁЁЁЁ d.РћгУбєМЋФрПЩЛиЪеAgЁЂPtЁЂAuЕШН№Ъє
ЃЈ5ЃЉРћгУЗДгІ2Cu+O2+ 2H2SO4 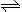 2 CuSO4 + 2H2OПЩвджЦБИCuSO4ЃЌШєНЋИУЗДгІЩшМЦЮЊдЕчГиЃЌЦфе§МЋЕчМЋЗДгІЪНЮЊЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
2 CuSO4 + 2H2OПЩвджЦБИCuSO4ЃЌШєНЋИУЗДгІЩшМЦЮЊдЕчГиЃЌЦфе§МЋЕчМЋЗДгІЪНЮЊЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
27. ЃЈ14ЗжЃЉ МИжжадШОЩЋЬхвьГЃЙћгЌЕФадБ№ЁЂг§адЕШШчЭМЫљЪОЁЃ
ЁЁ
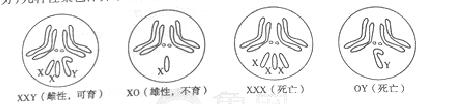
ЃЈ1ЃЉе§ГЃЙћгЌдкМѕЪ§ЕквЛДЮЗжСбжаЦкЕФЯИАћФкШОЩЋЬхзщЪ§ЮЊЁЁЁЁЁЁЁЁ ЁЁЃЌдкМѕЪ§ЕкЖўДЮЗжСбКѓЦкЕФЯИАћжаШОЩЋЬхЪ§ЪЧ ЁЁЁЁЁЁЁЁЁЁЁЁЬѕЁЃ
ЃЈ2ЃЉАзблДЦЙћгЌЃЈXЁЏ XЁЏYЃЉзюЖрФмВњЩњXЁЏЁЂ XЁЏ XЁЏ ЁЁЁЁЁЁЁЁКЭЁЁЁЁЁЁ ЁЁЫФжжРраЭЕФХфзгЁЃИУЙћгЌгыКьблалЙћгЌ ЃЈXRYЃЉдгНЛЃЌзгДњжаКьблДЦЙћгЌЕФЛљвђаЭЮЊЁЁЁЁЁЁЁЁЁЁ ЁЃ
ЃЈ3ЃЉгУКкЩэАзблДЦЙћгЌЃЈaa XЁЏ XЁЏЃЉгыЛвЩэКьблалЙћгЌЃЈAA XRYЃЉдгНЛЃЌF1 ДЦЙћгЌБэЯжЮЊЛвЩэКьблЃЌалЙћгЌБэЯжЮЊЛвЩэАзблЁЃF2жаЛвЩэКьблгыКкЩэАзблЙћгЌЕФБШР§ЮЊЁЁЁЁЁЁЁЁ ЁЁЃЌДгF2ЛвЩэКьблДЦЙћгЌКЭЛвЩэАзблалЙћгЌжаИїЫцЛњбЁШЁвЛжЛдгНЛЃЌзгДњжаГіЯжКкЩэАзблЙћгЌЕФИХТЪЮЊЁЁЁЁЁЁ ЁЁЁЃ
ЃЈ4ЃЉгУКьблДЦЙћгЌЃЈXRXRЃЉгыАзблалЙћгЌЃЈXЁЏYЃЉЮЊЧзБОдгНЛЃЌдкF1ШКЬхжаЗЂЯжвЛжЛАзблалЙћгЌЃЈМЧЮЊЁАMЁБЃЉЁЃMЙћгЌГіЯжЕФдвђгаШ§жжПЩФмЃК ЕквЛжжЪЧЛЗОГИФБфв§Ц№БэЯжаЭБфЛЏЃЌЕЋЛљвђаЭЮДБфЃЛЕкЖўжжЪЧЧзБОЙћгЌЗЂЩњЛљвђЭЛБфЃЛЕкШ§жжЪЧЧзБОДЦЙћгЌдкМѕЪ§ЗжСбЪБЦкXШОЩЋЬхВЛЗжРыЁЃЧыЩшМЦМђБуЕФдгНЛЪЕбщЃЌШЗЖЈMЙћгЌЕФГіЯжЪЧгЩФФвЛжждвђв§Ц№ЕФЁЃ
ЪЕбщВНжшЃКЁЁЁЁЁЁЁЁЁЁ ЁЃ
НсЙћдЄВтЃКЂё. Шє ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃЌдђЪЧЛЗОГИФБфЃЛ
Ђђ. Шє ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃЌдђЪЧЛљвђЭЛБфЃЛ
Ђѓ. Шє ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃЌдђЪЧМѕЪ§ЗжСбЪБXШОЩЋЬхВЛЗжРыЁЃ
ЁЁ
26. ЃЈ8ЗжЃЉгвЭМжаЃЌЧњЯпЂёЁЂЂђЁЂЂѓЗжБ№БэЪОФГвАЩњЖЏЮяжжШКЪ§СПГЌЙ§ЛЗОГШнФЩСПКѓЃЌЦфЮДРДжжШКЪ§СПБфЛЏШ§жжПЩФмЕФЧщПіЁЃ
ЃЈ1ЃЉЭМжаЧњЯпЁЁЁЁЁЁ ЫЕУїИУжжШКЖдЦфЦмЯЂЕиЕФЦЦЛЕГЬЖШНЯЧсЁЃЕБЧњЯпЂѓЧїНќгкСуЪБЃЌЖдИУЖЏЮяжжШКвбВЛвЫВЩШЁЁЁЁЁЁЁ
ЁЁБЃЛЄЕФДыЪЉЁЃЭМжавѕгАВПЗжПЩФмв§Ц№ИУжжШКЕФЁЁЁЁЁЁЁЁ ЗЂЩњБфЛЏЃЌНјЖјЕМжТЮя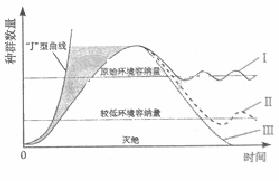 жжБфЛЏЁЃ
жжБфЛЏЁЃ
ЃЈ2ЃЉШєЭМжаЮяжжДІгкзюИпгЊбјМЖЃЌЕБЦфЪ§СПЯТНЕЃЌЧвЦфЫћЬѕМўВЛБфЪБЃЌСїЯђИУгЊбјМЖЦфЫћЮяжжЕФФмСПЛсЁЁЁЁЁЁЁЁ ЁЃ ДІгкИУгЊбјМЖЮяжжЕФжжМфЙиЯЕЪЧЁЁЁЁЁЁЁЁ ЁЁЁЃ
ЁЁЃЈ3ЃЉШєЭМжаЮяжжЮЊЪГВнЖЏЮяЃЌЕБПДЕНЧрВнУїЯдМѕЩйЪБЃЌВПЗжИіЬхЛсСэУйШЁЪГЕиЃЌетЬхЯжСЫЩњЬЌЯЕЭГЕФЁЁЁЁЁЁЁЁЁЁ ЁЁЕФЙІФмЁЃ
ЁЁЃЈ4ЃЉШЫРрЖдвАЩњЖЏЮяЦмЯЂЕиЕФЙ§ЖШРћгУвВЛсЕМжТГіЯжЭМжаЕФШ§жжЧщПіЁЃ16ЪРМЭвдРДЃЌЪРНчШЫПкБэЯжЮЊЁАJЁБаЭдіГЄЃЌвђДЫашПижЦЁАJЁБаЭдіГЄЪ§зжЗНГЬЪНжаЁЁЁЁЁЁ ЁЁВЮЪ§ЃЌвдЪЕЯжШЫПкКЭвАЩњЖЏЮязЪдДЕФаЕїЗЂеЙЁЃ
25. ЃЈ10ЗжЃЉШЫЪжжИвтЭтДЅЕНРЏжђЛ№бцЃЌв§Ц№ЧќжтЗДЩфЁЃЦфЗДЩфЛЁЪОвтЭМШчЯТЁЃ
ЃЈ10ЗжЃЉШЫЪжжИвтЭтДЅЕНРЏжђЛ№бцЃЌв§Ц№ЧќжтЗДЩфЁЃЦфЗДЩфЛЁЪОвтЭМШчЯТЁЃ
ЃЈ1ЃЉЭМжаЩёОдЊaВњЩњЕФаЫЗмдкДЋШыЩёОЯЫЮЌЩЯвд ЁЁЁЁЁЁЁЁаЮЪННјааДЋЕМЁЃЕБЩёОГхЕНДЋЕНЩёОФЉЩвЪБЃЌв§Ц№ЭЛДЅЧАФЄФкЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЪЭЗХЩёОЕнжЪЃЌИУЕнжЪгыЩёОдЊbЯИАћФЄЩЯЁЁ ЁЁЁЁЁЁНсКЯЃЌЪЙЩёОдЊbаЫЗмЁЃЩёОдЊbЕФЩёОГхЖЏНјвЛВНв§Ц№ЩёОдЊcаЫЗмЃЌзюжеЕМжТЧќМЁЪеЫѕЁЃ
ЃЈ2ЃЉЭМжаMЕуаЫЗмЪБЃЌДЫДІЩёОЯЫЮЌФЄСНВрЕФЕчЮЛБэЯжЮЊЁЁЁЁЁЁЁЁ ЁЃШєNЕуЪмДЬМЄВњЩњаЫЗмЃЌдђдкЩёОдЊbЩЯ ЁЁЁЁЁЁЁЁЃЈЬюЁАгаЁБЛђЁАЮоЁБЃЉФЄЕчЮЛЕФБфЛЏЃЌЦфдвђЪЧЁЁ ЁЁЁЁЁЁЁЁЁЃ
ЁЁЃЈ3ЃЉ ЪжжИвтЭтДЅЕНЛ№бцв§Ц№ОжВПЦЄЗєКьжзЃЌЪЧвђЮЊЦЄЗєУЋЯИбЊЙмЪцеХКЭЭЈЭИаддіМгЃЌ
ЁЁЁЁЁЁЁЁЁЁ в§Ц№зщжЏМфЯЖвКЬхЛ§ОлЁЃШєЪжжИЩЫПкИаШОЃЌПЩв§Ц№ЬхвКжаЭЬЪЩЯИАћКЫЩБОњЮяжЪЕжгљВЁОњЧжКІЃЌДЫЙ§ГЬЪєгкЁЁЁЁЁЁЁЁ УтвпЁЃ
ЁЁ
24. ЃЈ9ЗжЃЉВИШщЖЏЮяИЮЯИАћФкЬЧДњаЛЕФВПЗжЙ§ГЬШчЭМЫљЪОЁЃ
ЃЈ9ЗжЃЉВИШщЖЏЮяИЮЯИАћФкЬЧДњаЛЕФВПЗжЙ§ГЬШчЭМЫљЪОЁЃ
ЃЈ1ЃЉЭМжаXЮяжЪЮЊЁЁЁЁЁЁ ЁЃдкгабѕЬѕМўЯТЃЌИУЮяжЪКЭЫЎГЙЕзЗжНтГЩЖўбѕЛЏЬМКЭ[H]ЃЌИУЙ§ГЬдкЁЁЁЁЁЁЁЁ жаНјааЁЃ
ЃЈ2ЃЉбЊЬЧХЈЖШЩ§ИпЪБЃЌЦЯЬбЬЧНјШыИЮЯИАћКѓПЩКЯГЩЁЁЁЁЁЁЁЁЁЁЁЁ ЃЌЖргрЕФЦЯЬбЬЧЛЙПЩвдзЊЛЏГЩЁЁЁЁЁЁЁЁЁЁЁЁ вдДЂДцФмСПЁЃ
ЁЁЃЈ3ЃЉвШЯйжаЁЁЁЁЁЁ ЁЁЗжУкЕФвШИпбЊЬЧЫиЃЌгыИЮЯИАћФЄЩЯЕФЪмЬхНсКЯКѓЕїНкЬЧДњаЛЙ§ГЬЃЌетЗДгГСЫЯИАћФЄОпга ЁЁЁЁЁЁЁЁЁЁЁЁЕФЙІФмЁЃ
ЃЈ4ЃЉгУ14CБъМЧЕФЦЯЬбЬЧбаОПИЮЯИАћФкЬЧДњаЛЕФЙ§ГЬжаЃЌЗЂЯжбЊНЌжаЕФАзЕААзврГіЯжЗХЩфадЁЃдкАзЕААзКЯГЩКЭЗжУкЕФЙ§ГЬжаЃЌвРДЮГіЯжЗХЩфадЕФЯИАћЦїЪЧ ЁЁЁЁЁЁЁЁЁЁЁЃ
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com