
12.在容积相同的A、B两个密闭容器中,分别充入amolN2和bmolH2,使它们在同温度下反应,并达平衡,若A容器保持体积不变,B容器保持压强不变,当A中NH3的体积分数为25%时,则B中NH3的体积分数为 ( )
A.12.5% B.25% C.<25% D.>25%
 13.关于右图所示①、②两个装置的叙述,正确的是 ( )
13.关于右图所示①、②两个装置的叙述,正确的是 ( )
A.装置名称:①是原电池,②是电解池
B.硫酸浓度变化:①增大,②减小
C.电极反应式:①中阳极:4OH--4e-=2H2O+O2↑
②中正极:Zn-2e-=Zn2+
D.离子移动方向:①中H+向阴极方向移动
②中H+向负极方向移动
第Ⅱ卷(非选择题,共174分)
11.在稀硫酸中加入铜粉,铜粉不溶,再加入下列固体粉末:①FeCl2;②Fe2O3;③Zn;
④KNO3。铜粉可溶解的是 ( )
A.②④ B.①② C.②③ D.①④
10.将某些化学知识用数轴表示,可以收到直观现象、简明易记的效果,用数轴表示的下列化学知识中不正确的是 ( )
A.常温条件下,石蕊的变色范围:
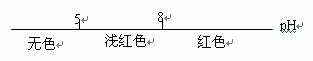
B.分散系的分类
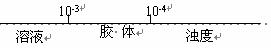 分散质微粒直径
分散质微粒直径
C.AlCl3和NaOH溶液反应后铝元素的存在形式
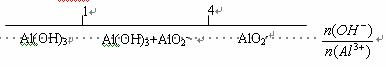
D.CO2与NaOH溶液反应的产物:
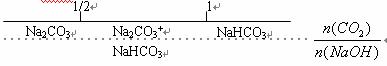
9.用NA表示阿伏加德罗常数的值,下列说法中正确的是 ( )
A.4g重水(D2O)中所含质子数为0.2NA
B.4.48LN2与CO的混合物所含分子数为0.2NA
C.6.2g白磷与红磷的混合物中所含磷原子数为0.2NA
D.12.5mL16mol·L-1浓硫酸与足量铜反应,转移电子数为0.2NA
8.下列离子方程式或化学化学式中正确的是 ( )
A.氯气通入水中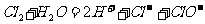
B.向Fe(OH)3中加入氢碘酸: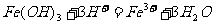
C.一小块金属钠投入盐酸: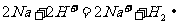
D.向Mg(HCO3)2溶液中加入过量的苛性钠溶液:
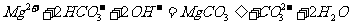
7.某实验报告记录了如下数据,其中数据合理的是 ( )
A.用10mL量筒取5.26mL稀硫酸
B.用托盘天平称量11.7g氧化铜粉末
C.用广泛pH试纸测得某溶液的pH为3.5
D.用酸式滴定管量取10.5mL盐酸溶液
29.(16分)工业上用氨氧化法制硝酸,尾气中氮的氧化物(NO、NO2)是主要的大气污染物之一。
(1)写出氨催化氧化反应的化学方程式,并标出反应中电子转移的方向和数目。
(2)用NOx表示氮氧化物,若用氨催化还原法治理硝酸工业的尾气,该反应的化学方程式为 。
(3)NaOH,吸收法治理硝酸工业尾气的反应原理如下:
2NO2+2NaOH=NaN03+NaN02+H20,NO+NO2+2NaOH=2NaN02+H20
尾气中的N02和NO能够被NaOH溶液完全吸收时,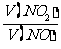 的取值范围是 ,
的取值范围是 ,
当尾气中: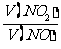 =
=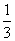 时,要保证尾气被NaOH溶液完全吸收,至少需要向尾气中加入O2的体积占N02和NO总体积的 %(同温同压下)。
时,要保证尾气被NaOH溶液完全吸收,至少需要向尾气中加入O2的体积占N02和NO总体积的 %(同温同压下)。
28.实验室定量分析某样品中亚硫酸钠的一种方法是:
①在1.520g样品中加入碳酸氢钾溶液、0.13% I2的氯仿溶液,在分液漏斗中振荡15min。离子方程式为:SO32-+I2+2HCO3-=SO42-+2I-+2CO2↑+H2O
②取①中所得的水溶液,加入一定量乙酸、足量的饱和溴水溶液,充分振荡,其中碘离子被氧化成碘酸根离子,得到250mL溶液。
③在②所得溶液中取25mL,滴加甲酸,除去其中过量的Br2。
方程式为:Br2+HCOOH=2HBr+CO2↑
④将③所得溶液中加适量的醋酸钠,再加入足量的碘化钾溶液,振荡溶液。
⑤用标准的硫代硫酸钠溶液滴定④中所得溶液,共消耗0.1120mol/L Na2S2O3 15.10mL。离子方程式为:I2+2S2O32-=2I-+S4O62-
回答下列问题:
⑴写出②、④两步操作中所发生反应的离子方程式。
⑵①中为什么要用0.13% I2的氯仿溶液,而不直接用I2的水溶液?
⑶计算样品中亚硫酸钠的质量百分含量
27.(13分)PMMA常被用作光盘的支持基片,PMMA的单体A(C5H802)不溶于水,可以发生以下变化:
已知:E能发生银镜反应,F与NaHCO3溶液反应能产生气体,G的一氯取代产物H有两种不同的结构。请回答:
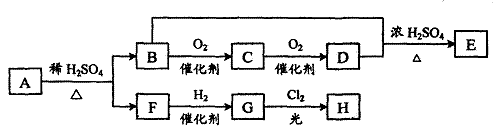
(1)F分子中含有的官能团的名称是: 。
(2)由F转化成G的反应类型属于(选填序号) 。
①氧化反应 ②还原反应 ③加成反应 ④取代反应
(3)由B与D反应生成E的化学方程式为 。
(4)B是-种新型汽车燃料。已知在通常情况下,1gB完全燃烧生成C02和液态水时放热22.7kJ。其热化学方程式 。
(5)由A发生加聚反应可得PMMA,该反应的化学方程式是 。
26.(10分)下图表示各物质之间的转化关系。已知:A、B、I都是XY2型化合物,且阳离子相同,A、B晶体中阴、阳离子个数比都是1∶1,但I晶体中阴、阳离子个数比是2∶1,I常用作干燥剂。
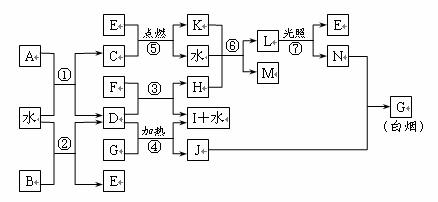
请按要求填空:
⑴G的电子式是_______________;
⑵反应⑥的化学方程式是_____________,反应⑤在空气中发生时的现象是_______,
已知C的燃烧热是1300 kJ·mol-1,表示C的燃烧热的热化学方程式是___________。
⑶根据上图中物质之间的转化关系及题中所给信息判断,B的化学式是_________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com