
30£®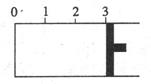 (13·Ö)Ņ»¶ØĪĀ¶ČĻĀ£¬ĻņČēĶ¼ĖłŹ¾µÄ“ųÓŠæÉŅĘ¶Æ»īČūµÄĆܱÕČŻĘ÷ÖŠ³äČĖ2 L
SO2ŗĶ1 L O2µÄ»ģŗĻĘųĢ壬·¢ÉśČēĻĀ·“Ó¦£ŗ2SO2(g)+O2(g)
(13·Ö)Ņ»¶ØĪĀ¶ČĻĀ£¬ĻņČēĶ¼ĖłŹ¾µÄ“ųÓŠæÉŅĘ¶Æ»īČūµÄĆܱÕČŻĘ÷ÖŠ³äČĖ2 L
SO2ŗĶ1 L O2µÄ»ģŗĻĘųĢ壬·¢ÉśČēĻĀ·“Ó¦£ŗ2SO2(g)+O2(g) 2SO3(g)”£
2SO3(g)ӣ
”””” (1)Čō»īČūæÉ×ŌÓÉŅĘ¶Æ£¬Ę½ŗāŗ󣬻īČūĶ£Ö¹ŌŚ”°2.1”±“¦£¬øĆ·“Ó¦ÖŠSO2µÄ×Ŗ»ÆĀŹĪŖ”””””””” ”£
”””” (2)Ļņ(1)Ę½ŗāŗóµÄČŻĘ÷ÖŠ³äČĖ0.2 mol SO3£¬»īČūŅʶÆŗóŌŁ“Ī“ļµ½Ę½ŗāŹ±£¬²āµĆ“Ė¹ż³ĢÖŠ“ÓĶā½ē¹²ĪüŹÕĮĖ1.96 kJČČĮ攣ŹŌŠ“³öSO2·¢ÉśŃõ»Æ·“Ó¦µÄČČ»Æѧ·½³ĢŹ½£ŗ”””””””””””””””””””””””””””””””””””””””””””””””””” ”£
”””” (3)ČōŹ¹»īČū¹Ģ¶ØŌŚ”°3”±“¦£¬³äČĖČŻĘ÷µÄĘšŹ¼ĪļÖŹ·Ö±šŹĒ¢Ł2 L SO2ŗĶl L O2£»¢Ś2 L SO3(g)ŗĶl L N2£»¢Ū1 L SO2”¢l L O2ŗĶ1 L SO3(g)£¬“ļµ½Ę½ŗāŗó£¬ČŻĘ÷ÖŠSO3(g)µÄÅØ¶Č“óŠ”¹ŲĻµŹĒ”””””” (ÓĆŠņŗÅ¢Ł¢Ś¢ŪŗĶ”°<”±»ņ”°=”±»ņ”°>”±±ķŹ¾)”£
”””” (4)Čō³£Ń¹ŗĶt”ęĢõ¼žĻĀ£¬Ź¹»īČū¹Ģ¶ØŌŚ”°3”±“¦£¬·“Ó¦“ÓSO2(g)ŗĶO2(g)æŖŹ¼£¬ĘšŹ¼Ź±c(SO2)=2 mol”¤L-1£¬c(O2)=10.9mol”¤L-1£¬“ļµ½»ÆŃ§Ę½ŗāדĢ¬Ź±£¬SO2µÄ×Ŗ»ÆĀŹĪŖ90%£¬Ōņ³£Ń¹ŗĶt”ęĢõ¼žĻĀ£¬·“Ó¦2SO2(g)+O2(g)=2SO3(g)µÄ»ÆŃ§Ę½ŗā³£ŹżKcĪŖ”””””””””””” ”£
[Ń”×ö²æ·Ö]
”””” ¹²7øöĢā”£æ¼Éś“ÓÖŠŃ”Ōń2øöĪļĄķĢā”¢1øö»ÆѧĢāŗĶ1øöÉśĪļĢā×÷“š”£
29£®(13·Ö)X”¢Y”¢ZŹĒČżÖÖĘųĢåµ„ÖŹ£¬A”¢B”¢C”¢D”¢EŹĒ»ÆŗĻĪļ£¬BµÄĖįŠŌČÜŅŗĻŌĒæŃõ»ÆŠŌ”£ø÷ĪļÖŹĪŹ“ęŌŚĻĀĶ¼ĖłŹ¾×Ŗ»Æ¹ŲĻµ(·“Ó¦Ģõ¼žĪ“×¢Ć÷)£ŗ
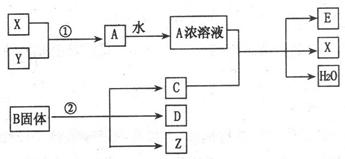
ŹŌ»Ų“šĻĀĮŠĪŹĢā£ŗ
(1)YµÄ»ÆѧŹ½ŹĒ”””””””””””” £¬AĖłŗ¬µÄ»Æѧ¼üĄąŠĶŹĒ”””””””””””””””” ”””””””””””£
(2)ĒėŠ“³ö·“Ó¦¢ŚµÄ»Æѧ·½³ĢŹ½£ŗ”””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””” ”£
(3)Š“³öXŗĶĖ®·“Ó¦µÄĄė×Ó·½³ĢŹ½£ŗ”””””””””””””””””””””””””””””””””””””””””””””””””””””””””””””” ”£
(4)ŹµŃéŹŅÖĘČ”XĘųĢåµÄ×°ÖĆ£¬²ÉÓĆĻĀĶ¼ÖŠµÄ”””””” ”£(ĢīŠ“×ÖÄø±źŗÅ)
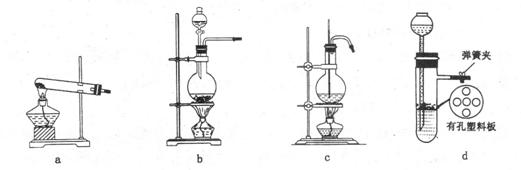
28£®(16·Ö)ĪŖĮĖĢ½¾æ”°¶žŃõ»ÆĢ¼ŹĒ·ńŌŚĖ®“ęŌŚŹ±²ÅÄÜŗĶ¹żŃõ»ÆÄĘ·“Ó¦”±£¬æĪĢāŃŠ¾æŠ”×éµÄĶ¬Ń§ĆĒĄūÓĆČēĻĀŹµŃé×°ÖĆ£¬·Ö±š½ųŠŠ¼×”¢ŅŅĮ½“ĪŹµŃé£ŗ
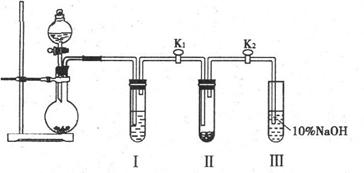
”””” ŹµŃé¼×£ŗøÉŌļµÄ¶žŃõ»ÆĢ¼ŗĶ¹żŃõ»ÆÄʵķ“Ó¦£ŗ
ŌŚøÉŌļµÄŹŌ¹Ü¢ņ֊װČėNaO2£¬ŌŚĶØČėCO2Ö®Ē°£¬¹Ų±ÕK1ŗĶK2”£ŌŚŹŌ¹ÜIČװČėŹŌ¼ĮXŗ󣬓ņæŖK1ŗĶK2£¬ĶØČĖCO2£¬¼ø·ÖÖÓŗ󣬽«“ų»šŠĒµÄľĢõ²åČėŹŌ¹Ü¢óµÄŅŗĆęÉĻ£¬¹Ū²ģµ½Ä¾Ģõ²»ø“Č¼£¬ĒŅ¢ņÖŠ¹ĢĢåµÄŃÕɫƻӊ±ä»Æ”£
”””” ŹµŃéŅŅ£ŗ³±ŹŖµÄ¶žŃõ»ÆĢ¼ŗĶ¹żŃõ»ÆÄʵķ“Ó¦£ŗ
”” ””ŌŚŹŌ¹ÜIČװČėŅŗĢ¬“æ¾»ĪļY£¬ĘäĖū²Ł×÷Ķ¬ŹµŃé¼×£¬¹Ū²ģµ½Ä¾Ģõø“Č¼£¬ĒŅ¢ņÖŠ¹ĢĢåµÄŃÕÉ«Óɵ»ĘÉ«±äĪŖ°×É«”£
ŹŌ»Ų“šĻĀĮŠĪŹĢā£ŗ
(1)ŹµŃé¼×ÖŠ£¬ŌŚ×°ČėNa2O2ŗó£¬ĶØČĖCO2Ö®Ē°£¬¹Ų±ÕK1ŗĶK2µÄÄæµÄŹĒ”””””””””””””””””””” ”£
(2)ŌŚŹµŃé¼×ÖŠ£¬ŹŌ¼ĮXŹĒ”””””””” £¬ŌŚŹµŃéŅŅÖŠ£¬YŹĒ”””””””” ”£
(3)øł¾ŻÉĻŹöĮ½øöŹµŃéĻÖĻó£¬µĆµ½µÄ½įĀŪŹĒ”””””””””””””””””””””””””””””””””””””””””””””””””””””” ”£
(4)ŹŌ¹ÜHIÖŠµÄNaOHČÜŅŗµÄ×÷ÓĆŹĒ”” ”””””””””””””””””””””””””””””””””””””””””””””””””””””””£
(5)ĪŖĮĖČ·±£ŹµŃéĻÖĻóµÄ×¼Č·ŠŌ£¬øł¾ŻĶ¼ÖŠ×°ÖĆ£¬ÖʱøCO2ĖłÓƵķ“Ó¦Īļ×īŗĆŃ”ÓĆ”””””””” (ĢīŠ“×ÖÄø±źŗÅ)
”””””” A£®“óĄķŹÆ”””” B£®Š”ĖÕ“ņ”””” c£®ŃĪĖį”””” D£®Ļ”ĮņĖį
(6)CO2ŗĶNa2O2µÄ·“Ó¦»śĄķæÉÓĆŹ¾×ŁŌ×Ó·ÖĪö¼ÓŅŌÖ¤Ć÷£¬ĒėĶź³ÉĻĀĮŠ·“Ó¦»Æѧ·½³ĢŹ½
Na2O2+C18O2+H218O===”””””””””””””””””””””””””””””””””””””””””””” ””””””””””””””””””””””””””””””””””””””””””
15£®øßĢśµē³ŲŹĒŅ»ÖÖŠĀŠĶæɳäµēµē³Ų£¬ÓėĘÕĶØøßÄܵē³ŲĻą±Č£¬øƵē³ŲÄܳ¤Ź±¼ä±£³ÖĪČ¶ØµÄ·ÅµēµēŃ¹”£øßĢśµē³ŲµÄ×Ü·“Ó¦ĪŖ£ŗ3Zn+2K2FeO4+8H2O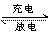 3Zn(OH)2+2Fe(OH)3+4KOH£¬ĻĀĮŠŠšŹö²»ÕżČ·µÄŹĒ
3Zn(OH)2+2Fe(OH)3+4KOH£¬ĻĀĮŠŠšŹö²»ÕżČ·µÄŹĒ
A£®³äµēŹ±Ņõ¼«·“Ó¦ĪŖ£ŗZn(OH)2 Zm+2OH-+2e-
Zm+2OH-+2e-
B£®³äµēŹ±Ńō¼«·“Ó¦ĪŖ£ŗFe(OH)3+5OH FeO42-+4H2O+3e-
FeO42-+4H2O+3e-
C£®·ÅµēŹ±øŗ¼«·“Ó¦ĪŖ£ŗZn+2OH Zn(OH)2+2e-
Zn(OH)2+2e-
D£®·ÅµēŹ±Õż¼«ø½½üČÜŅŗµÄ¼īŠŌŌöĒæ
µŚ¢ņ¾ķ(±Ų×ö120·Ö+Ń”×ö32·Ö£¬¹²152·Ö)
[±Ų×ö²æ·Ö]
14£®·Ö×ÓŹ½ĪŖC4H8O3µÄÓŠ»śĪļ£¬ŌŚŅ»¶ØĢõ¼žĻĀ¾ßÓŠĻĀĮŠŠŌÖŹ£ŗ
¢ŁŌŚÅØĮņĖį“ęŌŚĻĀ£¬ÄÜ·Ö±šÓėCH3CH2OH»ņCH3COOH·“Ó¦£»
¢ŚŌŚÅØĮņĖį“ęŌŚĻĀ£¬ŅąÄÜĶŃĖ®Éś³ÉŅ»ÖÖÖ»“ęŌŚŅ»ÖÖ½į¹¹ŠĪŹ½£¬ĒŅÄÜŹ¹äåĖ®ĶĖÉ«µÄĪļÖŹ£»
¢ŪŌŚÅØĮņĖį“ęŌŚĻĀ£¬»¹ÄÜÉś³ÉŅ»ÖÖ·Ö×ÓŹ½ĪŖC4H6O2µÄĪåŌŖ»·×“»ÆŗĻĪļ”£
øł¾ŻÉĻŹöŠŌÖŹ£¬Č·¶ØC4H8O3µÄ½į¹¹¼ņŹ½ĪŖ
A£®HOCH2COOCH2CH3”””” B£®HOCH2CH2CH2COOH
C£®CH3CH(OH)CH2COOH”””” D£®CH3CH2CH(OH)COOH
13£®Ä³Ņ»ÖÜĘŚ¢ņA×åŌŖĖŲµÄŌ×ÓŠņŹżĪŖx£¬ŌņĶ¬ÖÜĘŚµÄ¢óA×åŌŖĖŲµÄŌ×ÓŠņŹż
A£®Ö»ÓŠx+l”””””””””””””””””””””””” B£®æÉÄÜŹĒx+8
C£®æÉÄÜŹĒx+2”””””””””””””””””””””” D£®æÉÄÜŹĒx+l»ņx+11»ņx+25
12£®ŅŃÖŖNaHSO3ČÜŅŗ³ŹĖįŠŌ£¬NaHCO3ČÜŅŗ³Ź¼īŠŌ”£ĻÖÓŠÅØ¶Č¾łĪŖ0.1 mol”¤L-1µÄNaHSO3ČÜŅŗŗĶNaHCO3ČÜŅŗ£¬ČÜŅŗÖŠø÷Ī¢Į£ĪļÖŹµÄĮæÅØ¶ČµÄ¹ŲĻµŅ»¶ØÕżČ·µÄŹĒ(R±ķŹ¾S»ņC)
A£®c(Na+)>c(HRO3-)>c(H+)>c(RO32-)>c(OH-)
B£®c(Na+)+c(H+)=c(HRO3-)+c(RO32-)+c(OH-)
C£®c(H+)+c(H2RO3)=c(RO32-)+c(OH-)
D£®Į½ČÜŅŗÖŠc(Na+)”¢c(HRO3-)”¢c(RO32-)·Ö±šĻąµČ
11£®ĻĀĮŠø÷×éĄė×ÓŅ»¶ØÄÜ“óĮæ¹²“ęµÄŹĒ
A£®ŌŚŗ¬“óĮæF3+µÄČÜŅŗÖŠ£ŗNH4+”¢F2+”¢Cl-”¢SCN-
B£®³£ĪĀĻĀ£¬ŌŚpH=lµÄČÜŅŗÖŠ£ŗFe3+”¢S2-”¢Br-”¢NO3-
C£®³£ĪĀĻĀ£¬ÓÉĖ®µēĄėµÄc(H+)=10-13mol”¤L-1µÄČÜŅŗÖŠ£ŗNH4+”¢Al3+”¢SO42-”¢HCO3-
D£®ŌŚĒæ¼īŠŌČÜŅŗÖŠ£ŗNa+”¢SO42-”¢[Al(OH)4]-”¢CO32-
10£®ÉčNA±ķŹ¾°¢·ü¼ÓµĀĀŽ³£ŹżµÄÖµ£¬ĻĀĮŠŠšŹöÖŠÕżČ·µÄŹĒ
A£®Čē¹ū5.6 L N2ŗ¬ÓŠnøöµŖ·Ö×Ó£¬ŌņNAŅ»¶ØĪŖ4n
B£®ÓĆŗ¬ÓŠ0.1 mol FeCl3µÄ±„ŗĶČÜŅŗÖʵƵÄĒāŃõ»ÆĢś½ŗĢåÖŠ£¬½ŗĮ£ŹżµČÓŚ0.1 NA
C£®20 gÖŲĖ®(D2O)ÖŠŗ¬ÓŠµÄÖŠ×ÓŹżŹĒl0 NA
D£®±ź×¼×“æöĻĀ£¬CH4ŗĶNH3µÄ»ģŗĻĘųĢå22.4 Lŗ¬ÓŠµÄµē×ÓŹżŹĒNA
9£®ÄæĒ°£¬ĆĄ¹śæĘѧ¼ŅŅŃĢ½²ā³öĖ®ŠĒ“óĘųÖŠŗ¬ÓŠŅ»ÖÖ³ĘĪŖĮņ»ÆōŹ(·Ö×ÓŹ½ĪŖCOS)µÄĪļÖŹ£¬ŅŃÖŖĮņ»ÆōŹÓė¶žŃõ»ÆĢ¼µÄ½į¹¹ĻąĖĘ£¬ĒŅÄÜŌŚŃõĘųÖŠĶźČ«Č¼ÉÕ”£ĻĀĮŠÓŠ¹ŲĖµ·ØÕżČ·µÄŹĒ
A£®1 mol COSŌŚ×ćĮæŃõĘųÖŠ³ä·ÖČ¼ÉÕ£¬×ŖŅĘ4molµē×Ó
B£®Įņ»ÆōŹ·Ö×ÓÖŠø÷Ō×Ó×īĶā²ć¾łĀś×ć8µē×ÓĪČ¶Ø½į¹¹
C£®Įņ»ÆōŹŌŚ×ćĮæŃõĘųÖŠ³ä·ÖČ¼ÉÕŗó£¬Įņ»ÆōŹÖŠø÷ŌŖĖŲµÄ»ÆŗĻ¼Ū¾łÉżøß
D£®Įņ»ÆōŹµÄĦ¶ūÖŹĮæĪŖ60
¹ś¼ŹŃ§Š£ÓÅŃ” - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com