
19、(11分)某无色透明溶液可能含有下列离子:K+、Al3+、Fe3+、Ba2+、NO3-、SO42-、HCO3-、Cl-等,取该溶液进行如下实验:
①用蓝色石蕊试纸检测该溶液,试纸显红色;
②取溶液少许,加入铜片和稀硫酸共热,产生无色气体,该气体遇到空气立即变为红棕色;
③取溶液少许,加入氨水有白色沉淀生成,继续加入过量氨水,沉淀不消失;
④取溶液少许,滴入氯化钡溶液产生白色沉淀;
⑤取实验④后的澄清溶液,滴入硝酸银溶液产生白色沉淀,再加入过量的稀硝酸,沉淀不消失。请回答下列问题: 
⑴ 在实验①中,下图所示的操作中正确的是 ▲ (填代号)



⑵ 根据上述实验判断原溶液中肯定存在的离子是 ▲ ,
肯定不存在的离子是
▲ ;
⑶ 写出与②③三个实验有关的离子方程式:
②: ▲ ; ③: ▲ ;
18、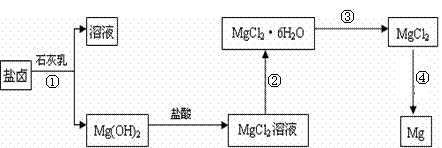 (7分)镁及其合金是一种用途很广的金属材料,目前世界上60%的镁是从海水中提取的。某学校课外兴趣小组从海水晒盐后的盐卤(主要含Na+、Mg2+、Cl-、Br-等)中模拟工业生产来提取镁,主要过程如下:
(7分)镁及其合金是一种用途很广的金属材料,目前世界上60%的镁是从海水中提取的。某学校课外兴趣小组从海水晒盐后的盐卤(主要含Na+、Mg2+、Cl-、Br-等)中模拟工业生产来提取镁,主要过程如下:

回答下列问题:
(1) 工业上从盐卤中获取Mg(OH)2用石灰乳而不用NaOH溶液的原因是 ▲ 。
(2) 从过程①得到的Mg(OH)2沉淀中混有少量的Ca(OH)2 ,除去少量Ca(OH)2的方法是先将沉淀加入到盛有 ▲ 溶液的烧杯中,充分搅拌后经 ▲ 、 ▲ (填操作方法)可得纯净的Mg(OH)2。
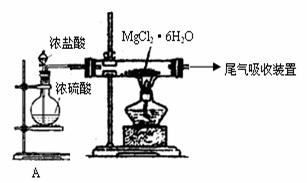 (3)下图是该兴趣小组设计进行过程③的实验装置图:
(3)下图是该兴趣小组设计进行过程③的实验装置图:
其中装置A的作用是 ▲ 。
(4)写出过程④中发生反应的化学方程式 ▲ 。(2分)
17、(10分)
(1)某一反应体系中有反应物和生成物共5种物质:S、H2S、HNO3、NO、H2O。该反应中还原产物是 ▲ ;若反应过程中转移了0.3mol电子,则氧化产物的质量是 ▲ 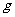 。
。
(2)将a mol Cl2 通入含b mol FeBr2的溶液中,当0< a / b≤1/2 时,反应的离子方程式为:2Fe2+ + Cl2
= 2Fe3+ + 2Cl-
,写出另2个可能发生的离子方程式。
① 当 a / b =1时
▲
;
② 当a / b≥3/2时 ▲
。 
(3)配平离子方程式(配平系数填入方框内),并用双线桥表示电子转移的方向和数目

 □MnO4-+□H2O2+□( ▲ )
□Mn2++□O2十□H2O
□MnO4-+□H2O2+□( ▲ )
□Mn2++□O2十□H2O


16、(8分)现有失去标签的氯化镁、碳酸钠、硫酸、氢氧化钡四种无色溶液,为了确定四种溶液各是什么,将它们随意编号为A,B,C,D后,进行实验,产生的现象如下表所示:
(氯化镁和碳酸钠反应生成的MgCO3是沉淀物质)。
|
实验编号 |
反应物质 |
有关现象 |
|
① |
A+B |
有沉淀生成 |
|
② |
B+C |
有气体放出 |
|
③ |
C+D |
有沉淀生成 |
|
④ |
B+D |
无明显现象 |
|
⑤ |
A+D |
有沉淀生成 |
根据实验现象,回答下列问题:
(1)写出物质化学式:A
▲ ;B ▲ ;C ▲ ;D ▲ 。
(2)写出实验①、②中发生反应的离子方程式:
① ▲ ;② ▲ 。

15、(8分)(1)一定温度下,把相对分子质量为M的可溶性盐Wg(不含结晶水)溶解在VmL水中,恰好形成饱和溶液(密度为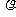 g·cm-3),则溶质质量分数为 ▲ ,物质的量浓度为
▲ ,该温度下此盐的溶解度为
▲ 。
g·cm-3),则溶质质量分数为 ▲ ,物质的量浓度为
▲ ,该温度下此盐的溶解度为
▲ 。
(2)粗盐经提纯后得到NaCl溶液,再经蒸发、结晶、烘干得精盐。
①蒸发操作中使用到的仪器除铁架台(带铁圈)外,还需要仪器的名称为
▲ 。
②该同学将所得精盐配成溶液,用于另一实验。实验中需要用60 mL 1 mol/L-1的NaCl溶液,配制过程中用托盘天平称取的精盐质量为 ▲ ,配制该溶液所需的主要仪器是 ▲ 。

14、多硫化钠Na2Sx(X≥2)在结构上与Na2O2,FeS2等有相似之处,Na2Sx在碱性溶液中可被NaClO氧化成Na2SO4而NaClO被还原为NaCl反应中,Na2Sx与NaClO的物质的量之比为1:16,则X值是
A.2 B.3 C.4 D.5

第Ⅱ卷(共58分)
13、
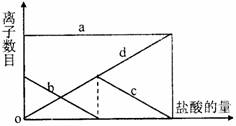 向一定量的K2CO3溶液中缓慢滴加稀盐酸,并不断搅拌。随着盐酸的加入溶液中离子数目也相应地发生变化。如图所示,四条曲线与溶液中的离子的对应关系,完全正确的是
向一定量的K2CO3溶液中缓慢滴加稀盐酸,并不断搅拌。随着盐酸的加入溶液中离子数目也相应地发生变化。如图所示,四条曲线与溶液中的离子的对应关系,完全正确的是
|
|
a |
b |
c |
d |
|
A |
Cl- |
K+ |
CO32- |
HCO3- |
|
B |
K+ |
CO32- |
Cl- |
HCO3- |
|
C |
K+ |
CO32- |
HCO3- |
Cl- |
|
D |
K+ |
HCO3- |
Cl- |
CO32- |
12、铁溶于一定浓度的硝酸溶液时,发生反应的离子方程式为:
aFe+bNO3-+cH+=dFe2++fFe3++gNO↑+hNO2↑+kH2O
下列有关推断中,不正确的是
A.2d+3f = 3g+h B.反应中每消耗5.6 g Fe,转移0.2mol-0.3mol e-
C.HNO3的氧化性大于Fe3+ D.当a不变时,d随着b的增大而增大
11、向一定量的Fe、FeO和Fe2O3的混合物中加入120mL 4mol/L的稀硝酸,恰好使混合物完全溶解,放出1.344L NO(标准状况),往所得溶液中加入KSCN溶液,无血红色出现。若用足量的氢气在加热下还原相同质量的混合物,能得到铁的物质的量为
A.0.24mol B.0.21mol C.0.16mol D.0.14mol
10、实验室保存下列试剂,有错误的是
A.浓盐酸易挥发,盛在无色密封的玻璃瓶中
B.碘易升华,保存在盛有水的棕色试剂瓶中
C.液溴易挥发,盛放在用水密封的用玻璃塞塞紧的棕色试剂瓶中
D.溴化银保存在棕色瓶中
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com