
31.(15分)我市大宝山铁矿的铁矿石主要成分是褐(赤)铁矿(主要成分是Fe2O3和脉石SiO2)。大宝山选矿厂采用最新的“磁化焙烧”工艺,将含脉石的细粒铁矿粉加入磁化焙烧炉中,焙烧温度控制在700-850 ℃之间,利用煤粉不完全燃烧产生的还原性气体CO作还原剂,同时使铁矿粉在焙烧炉内剧烈翻腾,将褐(赤)铁矿转化为磁铁矿(主要成分是Fe3O4),进而将矿石与脉石有效分离。大宝山选矿厂选矿的主要工艺流程如下:
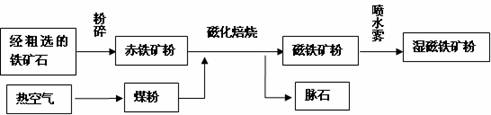
(1)经粗选的铁矿石粉碎的目的是 ;
(2)写出磁化焙烧炉时反应的化学方程式 ;
 (3)实现磁铁矿粉与脉石分离的原理是
;若在实验室除去少量该褐(赤)铁矿中的脉石SiO2,则可向其中加入
溶液,加热,过滤,得到较纯净的Fe2O3;
(3)实现磁铁矿粉与脉石分离的原理是
;若在实验室除去少量该褐(赤)铁矿中的脉石SiO2,则可向其中加入
溶液,加热,过滤,得到较纯净的Fe2O3;
(4)已知煤粉不完全燃烧时还有炭单质产生。
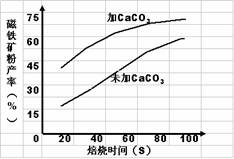
磁化焙烧过程中另外需加入CaCO3进行铁
矿石的脱硫处理,右图为加CaCO3和不加
CaCO3对磁铁矿粉产率的影响,根据图像
分析,CaCO3的另一作用为 ;
0.1 mol·L-1KI、BaCl2稀溶液、品红溶液、蒸馏水。
(1)对该气体成分提出合理假设
假设1:该气体是O2;假设2:该气体是 ;假设3:该气体是 ;
(2)设计实验方案证明你的假设,在答题卡上按下表的格式完成实验步骤、预期现象与结论:
|
实验步骤 |
预期现象与结论 |
|
将气体依次通入盛有
、
的洗气瓶中, 。 |
若
,则假设1成立; 若 ,则假设2成立; 若 ,则假设3成立。 |
II.定量实验探究该新型洗涤剂中Na2CO3和H2O2的质量比:
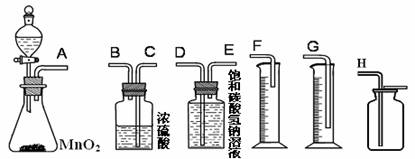
(3)从下图中选择适当的仪器,组装一套最简便的装置,该装置的连接顺序从左至右是(填各接口的字母代号) 接 、 接 ;
(4)分液漏斗中依次加入的试剂是 ,测定的物理量是 。
30.(17分)将Na2CO3和H2O2混合(Na2CO3和H2O2不发生反应)可用作新型洗涤剂,某化学小组对这种新型洗涤剂进行探究。
I.定性探究该新型洗涤剂加入FeCl3固体产生气体的成分:
取该洗涤剂100 ml,加入25 gFeCl3固体,产生大量无色无味气体,用贮气瓶收集气体。请利用实验室常用仪器、用品和以下限选试剂完成该气体成分的探究过程。
限选试剂:0.10 mol·L-1 NaOH、8.0 mol·L-1 NaOH、澄清石灰水、0.01 mol·L-1KMnO4、
23.在容积固定的密闭容器中充入一定量的两种X、Y气体,一定条件下发生可逆反应:3X(g)+3Y(g)≒2Z(g),并达到平衡。已知正反应是放热反应,测得X的转化率为37.5﹪,Y的转化率为25﹪,下列有关叙述正确的是
A.若X的反应速率为0.15 mol/(L·s),则Z的反应速率为0.1 mol/(L·s)
B.若向容器中充入氦气,Y的转化率增大
C.开始充入容器的X、Y物质的量之比为2:3
D.升高温度,正反应速率增大,平衡向正反应方向移动
22.常用的补牙剂中有一种汞合金,它含有几乎等质量的汞、银、锡、铜和锌。补牙剂汞合金中含有组成大致为Ag2Hg3、Ag3Hg、SnxHg(x=7-9)的物质,它们可能发生电极反应为:
3Hg22++4Ag+6e-=2Ag2Hg3;Sn2++3Ag+2e-=Ag3Sn。如果补过的牙不小心咬到包装用的铝箔会产生微电流刺激牙神经引起疼痛,下列有关说法正确的是
A.Ag3Sn的中的Ag和Hg22+中的Hg都显+1价
B.产生疼痛时,铝作负极,发生的电极反应为:Al-3e-=Al3+
C.唾液充当电解液
D.产生微电流刺激牙神经时,电流方向从Al到合金
12.科学家发现,某些高温油炸食品中含有一定量的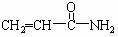 (丙烯酰胺)。食品中过量的丙烯酰胺可能引起令人不安的食品安全问题。关于丙烯酰胺有下列叙述:①能使酸性KmnO4溶液褪色;②能发生加聚反应生成高分子化合物;③只有4种同分异构体;④能与氢气发生加成反应。其中正确的是
(丙烯酰胺)。食品中过量的丙烯酰胺可能引起令人不安的食品安全问题。关于丙烯酰胺有下列叙述:①能使酸性KmnO4溶液褪色;②能发生加聚反应生成高分子化合物;③只有4种同分异构体;④能与氢气发生加成反应。其中正确的是
A.①②③ B.②③④ C.①③④ D.①②④
11.元素X、Y、Z原子序数之和为37,X、Y在同一周期,X+与Z-具有相同的核外电子层结构。下列推测不正确的是
A.同周期元素中X的金属性最强
B.原子半径X>Y,离子半径X+>Z-
C.同族元素中Z的氢化物稳定性最高
D.同周期元素中Y的最高价含氧酸的酸性最强
10.下列有关实验操作的说法正确的是
A.用渗析法分离淀粉中混有的NaCl杂质.
B.用玻璃棒搅拌漏斗中的液体以加快过滤速率
C.加入盐酸以除去硫酸钠中的少量碳酸钠杂质
D.用量筒取5.00mL 10.0mol·L-1硫酸于50mL容量瓶中,加水稀释至刻度,可配制1.00mol·L-1硫酸
9.NA为阿伏加德罗常数,下列说法正确的是
A.1L0.2mol/L的KAl(SO4)2溶液中,含有0.2NA个Al3+
B.0.1molCl2与0.1molNa充分反应,转移的电子数为0.1NA
C.3.6 g碳与3.36 LO2一定条件下恰好完全反应,生成CO分子数一定为0.3 NA
D.某温度下,MgCO3的溶度积Ksp=10-2,则溶液中Mg2+有0.1NA个
8.下列有关N、S、Cl等非金属元素化合物的说法正确的是
A.实验室可用浓硫酸干燥氨气
B.漂白粉的成分为次氯酸钙
C.Al2(SO4)3可除去碱性废水及酸性废水中的悬浮颗粒
D.实验室可用NaOH溶液处理SO2和HCl废气
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com