
7. It’s me a lot of time to find out what I really want to do in the future. (A) paying (B) spending (C) taking (D) using
6. When I heard my baby girl say her first word, my heart was with joy. (A) filled (B) marked (C) prepared (D) shown
5. Marsha thought her friends would do something to celebrate her birthday, but they just
gave her a birthday card. (A) correct (B) honest (C) quick (D) special
4. How can you study in the living room when other people are watching TV?
I think you need a place. (A) cleaner (B) quieter (C) safer (D) smaller
3. The pants I bought last year are too small now. I think I need a new . (A) belt (B) pair (C) shirt (D) space
2. I put the fish in the ice box to keep it . (A) fresh (B) full (C) new (D) young
1. Here’s Mary’s plan for one week during her summer vacation. What kind of plan is this? (A) A trip plan. (B) A party plan. (C) An eating plan. (D) An exercise plan

16、已知有机物中一个碳原子上连有两个羟基时,易脱水形成碳氧双键;物质A→F有如下转化关系:
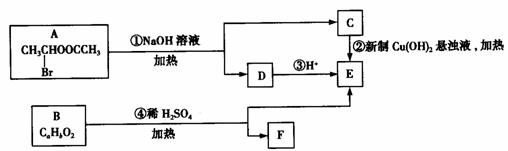
请回答下列问题:
(1)E中含有的官能团的名称是_____________,C跟新制,的氢氧化铜悬浊液反应的化学方程式为:____________________________
(2)已知B的相对分子质量为162,其燃烧产物中n(CO2):n(H2O)=2:1。则B的分子式为_________________
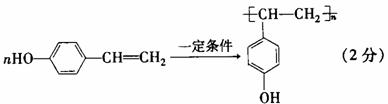
(3)F具有如下特点:①能跟FeCl3溶液发生显色反应;②能发生加聚反应。若F的苯环上的一氯代物只有两种,则F在一定条件下发生加聚反应的化学方程式为__________________________。
(4)化合物G是F的同分异构体,它属于芳香族化合物,能发生银镜反应。则C可能具有______________________种结构,写出其中两种的结构简式_______________________。
解析:(1)由图示及已知信息可得反应①为:
CH3CHClOOCCH3+2NaOH CH3CHO+CH+COONa+H2O
+NaBr。所以物质C是CH3CHO、D是CH3COONa、E是CH3COOH;故E中含有的官能团是羧基,C跟新制的氢氧化铜悬浊液反应的化学方程式为:CH3CHO+2Cu(OH)2
CH3CHO+CH+COONa+H2O
+NaBr。所以物质C是CH3CHO、D是CH3COONa、E是CH3COOH;故E中含有的官能团是羧基,C跟新制的氢氧化铜悬浊液反应的化学方程式为:CH3CHO+2Cu(OH)2 CH3COOH+Cu2O↓+2H2O。
CH3COOH+Cu2O↓+2H2O。
(2)对于B物质,其分子式为CaHbO2;由其相对分子质量为162,燃烧产物中n(CO2) :n(H2O)=2:1,可确定a=b,162-32=130,即(CH)n的式量为130,所以n=10,故B的分子式是C10H10O2.
(3)依据F具有的特点并结合B在稀H2SO4 、加热条件下生成乙酸和F,可判断B为乙酸酯类,进而确定F的结构简式为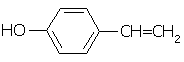 (4)化合物G是F的同分异构体,它属于芳香族化合物,能发生银镜反应。则G中含有醛基和苯环,即可推出其所有结构。
(4)化合物G是F的同分异构体,它属于芳香族化合物,能发生银镜反应。则G中含有醛基和苯环,即可推出其所有结构。
答案:(1)羧基(1分) CH3CHO+2Cu(OH)2 CH3COOH+Cu2O↓+2H2O(2分)
CH3COOH+Cu2O↓+2H2O(2分)
(2)C10H10O2(3分)
(3) 
(4)4 (2分) 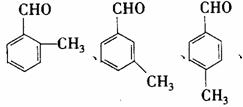 (2分)
(2分)
15.为了节能减排,提高综合经济效益,某工厂采用焦炉气一含硫烟道气联合生产硫酸铵和亚硫酸氢铵两种产品,其工艺流程图如下:
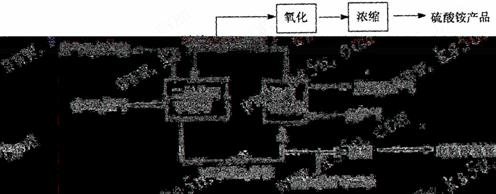
说明:对苯二酚在空气中易被氧化,具有较强的还原性。
(l)下列有关说法正确的是_ _ _。
a、含SO2烟气直接排放易引起酸雨
b、焦炉气若用河水洗涤后直接排放,易引起水体的富营养化
c、脱氨焦炉气可作燃料发电
d、检验硫酸铵产品中是否混有较多的亚硫酸铵杂质,可用溴水作试剂
(2)生产亚硫酸氢铵时,加入少量对苯二酚的作用是_ _
(3)氨气吸收塔中发生反应的离子方程式为:_ _。
(4)已知烟气含SO2 2%,焦炉气中含NH3 4.8%,若只生产硫酸铵一种产品,吸收后的尾气中所含的SO2或NH3可忽略,则含SO2烟气与焦炉气的流量(每分钟流过的体积)比为_ _ 。
解析:本题是以“含硫废气和焦炉气”的综合利用为背景,从工艺流程、实验基础知识、反应原理、简单流量计算等角度考查学生对新知识、新情景的整合,试题关注学生对资源利用和环境保护理念的形成,运用化学知识解决实际问题的能力。
(1)SO2溶于水形成亚硫酸,氧化后又能生成硫酸,a选项正确;焦炉气有含氮化合物能引起水体富营养化,b选项正确;脱氨焦炉气中含有CO、H2等可燃气体,c选项正确;亚硫酸根能使溴水褪色而硫酸氢铵不能,d选项正确。
(2)亚硫酸氢铵易被空气氧化,而使产品纯度降低,加对苯二酚还防止其氧化。
(3)NH4HSO3与氨气或氨水反应的离子方程式
(4)生成一种产品硫酸铵,由流程图可知,SO2、、NH3的物质的量之比为1:2。
设含SO2烟气与焦炉气的流量比为x:y,则2%x : 4.8%y=1:2 ; x:y=1.2∶1
答案:
(1)abcd
(2)对苯二酚作还原剂,保证亚硫酸氢铵不被氧化
(3)HSO3-+NH3·H2O = SO32-+NH4++H2O (或:HSO3-+NH3 = SO32-+NH4+)
(4)1.2∶1(或6∶5)。
14.A、B、C、D、E、F是六种短周期主族元素,它们的原子序数依次增大,其中C、F分别是同一主族元素,A、F两种元素的原子核中质子数之和比C、D两种元素原子核中质子数之和少2,F元素的最外层电子数是次外层电子数的0.75倍。又知B元素的最外层电子数是内层电子数的2倍,E元素的最外层电子数等于其电子层数。请回答:
(1)1 mol由E、F二种元素组成的化合物跟由A、C、D三种元素组成的化合物反应生成两种盐和水,完全反应后消耗后者的物质的量为 。
(2)A、C、F间可以形成甲、乙两种负一价双原子阴离子,甲有18个电子,乙有10个电子,则甲与乙反应的离子方程式为 ;
(3)科学研究证明:化学反应热只与始终态有关,与过程无关。单质B的燃烧热为a kJ/mol。由B、C二种元素组成的化合物BC 14g完全燃烧放出热量b kJ,写出单质B和单质C反应生成BC的热化学方程式: ;
(4)工业上在高温的条件下,可以用A2C与BC反应制取单质A2。在等体积的I、II两个密闭容器中分别充入1 molA2C和1mol BC、2 mol A2C和2 mol BC。一定条件下,充分反应后分别达到平衡(两容器温度相等)。下列说法正确的是。
A.达到平衡所需要的时间:I>II B.达到平衡后A2C的转化率:I=II
C.达到平衡后BC的物质的量:I>II D.达到平衡后A2的体积分数:I<II
(5)用B元素的单质与E元素的单质可以制成电极浸入由A、C、D三种元素组成化合物的溶液中构成电池,则电池负极反应式为 。
解析:依题意,F元素的原子最外层电子数为8×0.75=6,F位于第VIA族,C与F同主族,C为氧, F为硫;B的最外层电子数是内层电子数的2倍,B为碳;短周期中,原子最外层电子数等于电子层数的元素有氢、铍、铝,由原子序数大小知,E的质子数大于8,所以,E为铝。又因为质子数:Z(A)+Z(F)+2=Z(C)+Z(D),有Z(D)-Z(A)=16-8+2=10,得8<Z(D)<13,Z(D)=10+Z(A),若A为氢,则D为钠;若A为氦,则D为镁(A为主族元素,不符合要求,舍去),故A为氢,D为钠。综上所述,A为氢,B为碳,C为氧,D为钠,E为铝,F为硫。
(1)Al2S3+8 NaOH=2 NaAlO2+3 Na2S+4 H2O (2)甲为HS-,乙为OH-:HS-+OH-=S2-+H2O
(3)C(s)+O2(g)=CO2(g);△H=-a kJ/mol··① CO(g)+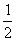 O2(g)=CO2(g);△H= -2b kJ/mol···②
O2(g)=CO2(g);△H= -2b kJ/mol···②
①-②得:C(s)+ 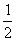 O2(g)=CO(g);△H= -(a-2b) kJ/mol (4) H2O(g)+CO(g)
O2(g)=CO(g);△H= -(a-2b) kJ/mol (4) H2O(g)+CO(g)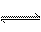 CO2+H2(g)
CO2+H2(g)
|
容器 |
条件 |
H2O |
CO |
CO2 |
H2 |
|
I |
恒温恒容 |
1 mol |
1 mol |
0 |
0 |
|
II |
恒温恒容 |
2 mol |
2 mol |
0 |
0 |
可以将容器II看成是容器I体积压缩一半,该可逆反应是等气体分子数反应。A项,压缩I容器,浓度增大,反应加快,II的反应速率大于I的反应速率,A项正确;B项,由于等气体分子数反应,所以,加压,平衡不移动,I和II容器中水蒸汽的转化率相等,B项正确;C项,II容器中起始反应物的量是I容器的2倍,平衡时,II容器中CO的物质的量是I容器中CO的物质的量2倍(平衡不移动),C项错误;D项,I和II平衡是等效平衡,H2体积分数相等,D项错误;(5)以石墨、铝为电极,用氢氧化钠溶液作电解质溶液构成原电池,铝为负极,石墨为正极:负极反应式:发生反应过程有2Al-6e-=2Al3+,2Al3++8OH-=2AlO2-+4H2O,负电极反应式为
2Al+8OH- -6e-=2AlO2-+4H2O
答案:(1)8 mol (2) HS-+OH-=S2-+H2O
(3) C(s)+ 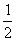 O2(g)=CO(g);△H= -(a-2b) kJ/mol
O2(g)=CO(g);△H= -(a-2b) kJ/mol
(4)A、B (5)2Al+8OH- -6e-=2AlO2-+4H2O
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com