
5Θ°ν« «‘≠Ή”–ρ ΐΉν¥σΒΡ―θΉε‘ΣΥΊΘ§ΆΤ≤βν«ΦΑΤδΜ·ΚœΈοΉν≤ΜΩ…ΡήΨΏ”–ΒΡ–‘÷ «
AΘ°ν« «ΡήΒΦΒγΒΡΙΧΧεΓΓΓΓΓΓ BΘ°ν«ΒΡ»έΒψΫœΗΏ
CΘ°ν«ΒΡ«βΜ·ΈοΚήΈ»Ε®ΓΓΓΓΓΓ DΘ°ν«÷Ν…Ό”–ΝΫ÷÷―θΜ·ΈοΕ‘”ΠΒΡΥ°Μ·Έο
4Θ°ΉνΫϋΩΤ―ßΦ“ΖΔœ÷ΝΥ―θΉε‘ΣΥΊΒΡ“Μ÷÷–¬ΈΔΝΘO4Θ§Ε‘”Ύ’β÷÷–¬ΈΔΝΘΘ§œ¬Ν–ΥΒΖ®≤Μ’ΐ»ΖΒΡ «
AΘ°Υϋ «―θΒΡ“Μ÷÷–¬ΒΡΆ§ΥΊ“λ–ΈΧεΓΓ BΘ°Υϋ «―θΒΡ“Μ÷÷–¬ΒΡΆ§ΈΜΥΊ
CΘ°ΥϋΒΡΡΠΕϊ÷ ΝΩ «64ΓΓΓΓΓΓΓΓΓΓΓΓ DΘ°ΥϋΒΡ―θΜ·–‘±»O3«Ω
3Θ°Ιΐ―θΜ·«βΥΉ≥ΤΥΪ―θΥ°Θ§Υϋ «“Μ÷÷“ΚΧεΘ§“ΉΖ÷ΫβΈΣΥ°ΚΆ―θΤχΘ§≥ΘΉς―θΜ·ΦΝΓΔΤ·ΑΉΦΝΚΆœϊΕΨΦΝΘ§ΈΣ÷ϋ¥φΓΔ‘Υ δΓΔ Ι”ΟΒΡΖΫ±ψΘ§ΙΛ“Β…œ≥ΘΫΪH2O2ΉΣΜ·ΈΣΙΧΧ§ΒΡΙΐΧΦΥαΡΤΨßΧε(ΤδΜ·―ß ΫΈΣ2Na2CO3ΓΛ3H2O2)Θ§ΗΟΨßΧεΨΏ”–Na2CO3ΚΆH2O2ΒΡΥΪ÷Ί–‘÷ ΓΘœ¬Ν–Έο÷ ≤ΜΜα ΙΙΐΧΦΥαΡΤΨßΧε ß–ßΒΡ «
ΓΓ ΓΓAΘ° MnO2ΓΓΓΓ BΘ°H2SΓΓΓΓ CΘ°œΓ―ΈΥαΓΓΓΓ DΘ°NaHCO3
2Θ°Ιΐ―θΜ·«βΒΡΖ–Βψ±»Υ°ΗΏΘ§ΒΪ ή»»»ί“ΉΖ÷ΫβΓΘΡ≥ ‘ΦΝ≥ßœ»÷ΤΒΟ7% - 8% ΒΡΙΐ―θΜ·«β»ή“ΚΘ§‘Ό≈®Υθ≥…30%»ή“Κ ±Θ§Ω…≤…”ΟΒΡ “ΥΖΫΖ® «
ΓΓ AΘ°≥Θ―Ι’τΝσΓΓΓΓΓΓ B.Φθ―Ι’τΝσΓΓΓΓΓΓ C.Φ”…ζ ·Μ“≥Θ―Ι’τΝσΓΓΓΓ D. Φ”―Ι’τΝσ
1Θ°œ¬Ν–ΙΊ”ΎΈχ‘ΣΥΊΒΡ”–ΙΊ–π ω’ΐ»ΖΒΡ «
AΘ°ΈχΜ·«β±»ΝρΜ·«βΈ»Ε®Θ§ΤδΥ°»ή“Κ‘ΎΩ’Τχ÷–ΡήΈ»Ε®¥φ‘Ύ
BΘ°ΒΞ÷ Έχ «“Μ÷÷ΑκΒΦΧε≤ΡΝœΓΓΓΓ CΘ°H2SO4ΓΔH2SeO4ΓΔH2TeO4ΒΡΥα–‘“ά¥Έ‘ω«Ω
DΘ°ΈχΒΡΖ«Ϋπ τ–‘±»―θ»θΘ§ΒΪ±»δε«Ω
3ΓΔΙΐ―θΜ·«β
ΔΌΙΐ―θΜ·«βΒΡΒγΉ” ΫΈΣΓΓΓΓΓΓΓΓΓΓΓΓ Θ§ «“Μ÷÷ΓΓΓΓΓΓ Ζ÷Ή”(ΧνΦΪ–‘ΜρΖ«ΦΪ–‘)ΓΘ
ΔΎΙΐ―θΜ·«βΈΣΈό…Ϊ’≥≥μ“ΚΧεΘ§ΥϋΒΡΥ°»ή“ΚΥΉ≥ΤΥΪ―θΥ°Θ§“Ϋ”ΟΥΪ―θΥ°ΒΡ÷ ΝΩΖ÷ ΐ“ΜΑψΈΣΓΓ ΓΘ
ΔέΜ·―ß–‘÷ ΘΚaΘ° «“Μ÷÷Εΰ‘Σ»θΥαΘ§ΨΏ”–»θΥα–‘Θ§ΒγάκΖΫ≥Χ ΫΈΣΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
ΚΆΓΓ ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΘΜbΘ°―θΜ·–‘Θ§»γΡήΑ―Fe2+―θΜ·≥…Fe3+Θ§Υα–‘ΧθΦΰœ¬ΒΡΖ¥”Π ΫΈΣΘΚ
ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΘΜcΘ°ΜΙ‘≠–‘Θ§»γΡήΖΔ…ζH2O2+Cl2==O2+2HCl Θ§Ρή ΙΥα–‘ΗΏΟΧΥαΦΊ»ή“ΚΆ …Ϊ(άκΉ”ΖΫ≥Χ ΫΘΚΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ )Β»ΘΜdΘ°≤ΜΈ»Ε®–‘( ή»»ΜαΖ÷ΫβΘ§MnO2Ής¥ΏΜ·ΦΝ ±Ζ¥”ΠΗϋΩλ)ΓΘΙΐ―θΜ·«βΩ…”ΟΉς―θΜ·ΦΝΓΔΤ·ΑΉΦΝΓΔœϊΕΨΦΝΓΔΆ―¬»ΦΝΘ§ΜΙΩ…ΉςΈΣΜπΦΐΒΡ»ΦΝœΓΘ
[Βδ–ΆάΐΧβ]
[άΐ1](2005Ρξ±±Ψ©Θ§6)ΗΏ―ΙΒγΜζΓΔΗ¥”ΓΜζΙΛΉς ±Μα≤ζ…ζ≥τ―θΘ§ΗΟΤχΧε”–«Ω―θΜ·–‘ΓΘœ¬Ν––π ω≤Μ’ΐ»ΖΒΡ «
AΘ°≥τ―θΚΆ―θΤχ «―θΒΡΆ§ΥΊ“λ–ΈΧεΓΓΓΓ BΘ°≥τ―θΩ… Ι Σ»σΒΡKIΒμΖέ ‘÷Ϋ±δάΕ
CΘ°≥τ―θΒΡ¥φ‘ΎΕ‘»ΥΧε”–“φΈόΚΠΓΓΓΓΓΓ DΘ°≥τ―θ «ΚήΚΟΒΡœϊΕΨΦΝΚΆΆ―…ΪΦΝ
[άΐ2](2005ΡξΙψΕΪΘ§25)œ¬Ν–ΙΊ”ΎΓΑΙΐ―θΜ·«βΓ±ΒΡΥΒΖ®’ΐ»ΖΒΡ «
AΘ°Ιΐ―θΜ·«βΨΏ”–…±ΨζœϊΕΨΉς”ΟΘ§ ««ΩΥαΓΓΓΓ BΘ°Ιΐ―θΜ·«β «άκΉ”Μ·ΚœΈο
CΘ°Ιΐ―θΜ·«βΩ…“‘ΖΔ…ζΖ÷ΫβΖ¥”ΠΓΓΓΓΓΓ DΘ°Ιΐ―θΜ·«β «Υ°ΒΡΆ§Ζ÷“λΙΙΧε
[άΐ3](2003ΡξΫ≠Υ’Θ§1)Υ°Ή ‘¥Ζ«≥Θ÷Ί“ΣΘ§ΝΣΚœΙζ»ΖΕ®2003ΡξΈΣΙζΦ Β≠Υ°ΡξΓΘœ¬Ν–ΙΊ”ΎΥ°ΒΡΥΒΖ®÷–¥μΈσΒΡ «
AΘ°’τΝσΖ® «ΚΘΥ°Β≠Μ·ΒΡΖΫΖ®÷°“ΜΓΓΓΓΓΓ BΘ°Β≠Υ°ΒΡΟήΕ»–Γ”ΎΚΘΥ°ΒΡΟήΕ»
CΘ°»ΎΜ·ΒΡ―©Υ°÷–ΩσΈο÷ Κ§ΝΩ±»…νΨ°Υ°÷–ΒΡ…ΌΓΓ DΘ°0Γφ“‘…œΘ§Έ¬Ε»‘ΫΗΏΘ§Υ°ΒΡΟήΕ»‘Ϋ–Γ
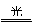 [άΐ4]1995Ρξ≈Β±¥ΕϊΜ·―ßΫ± Ύ”η÷¬ΝΠ―–ΨΩ≥τ―θ≤ψ±ΜΤΤΜΒΈ ΧβΒΡ»ΐΈΜΜ·―ßΦ“ΓΘ¥σΤχ÷–ΒΡ≥τ―θ≤ψΩ…¬Υ≥ΐ¥σΝΩΒΡΉœΆβœΏΘ§±ΘΜΛΒΊ«ρ…œΒΡ…ζΈοΓΘΖζάϊΑΚ(»γCCl2F2)Ω…‘ΎΙβΒΡΉς”Οœ¬Ζ÷ΫβΘ§≤ζ…ζCl‘≠Ή”Θ§Cl‘≠Ή”ΜαΕ‘≥τ―θ≤ψ≤ζ…ζ≥ΛΨΟΒΡΤΤΜΒΉς”ΟΓΘ”–ΙΊΖ¥”Π ΘΚΓΓΓΓ
[άΐ4]1995Ρξ≈Β±¥ΕϊΜ·―ßΫ± Ύ”η÷¬ΝΠ―–ΨΩ≥τ―θ≤ψ±ΜΤΤΜΒΈ ΧβΒΡ»ΐΈΜΜ·―ßΦ“ΓΘ¥σΤχ÷–ΒΡ≥τ―θ≤ψΩ…¬Υ≥ΐ¥σΝΩΒΡΉœΆβœΏΘ§±ΘΜΛΒΊ«ρ…œΒΡ…ζΈοΓΘΖζάϊΑΚ(»γCCl2F2)Ω…‘ΎΙβΒΡΉς”Οœ¬Ζ÷ΫβΘ§≤ζ…ζCl‘≠Ή”Θ§Cl‘≠Ή”ΜαΕ‘≥τ―θ≤ψ≤ζ…ζ≥ΛΨΟΒΡΤΤΜΒΉς”ΟΓΘ”–ΙΊΖ¥”Π ΘΚΓΓΓΓ
ΓΓ ΓΓO3ΓΓΓΓΓΓ O2+O Θ§Cl+O3ΓζClO+O2 Θ§ClO+OΓζCl+O2 Θ§ΉήΖ¥”ΠΘΚ2O3ΘΫ3O2
(1)‘Ύ…œ ω≥τ±δ≥…―θΤχΒΡΖ¥”ΠΙΐ≥Χ÷–Θ§Cl «
AΘ°Ζ¥”ΠΈοΓΓΓΓΓΓΓΓ B.…ζ≥…ΈοΓΓΓΓΓΓ C.÷–Φδ≤ζΈοΓΓΓΓΓΓΓΓΓΓ D.¥ΏΜ·ΦΝ
(2)O3ΚΆO2 «
ΓΓΓΓ AΘ°Ά§Ζ÷“λΙΙΧεΓΓΓΓ B.Ά§œΒΈοΓΓΓΓΓΓ C.―θΒΡΆ§ΥΊ“λ–ΈΧεΓΓ ΓΓD.―θΒΡΆ§ΈΜΥΊ
[Β±ΧΟΖ¥άΓ]
2ΓΔ―θΤχΚΆ≥τ―θ
(1)―θΤχ”κ≥τ―θ–‘÷ ΒΡ±»Ϋœ
|
Έο÷ |
―θΤχ |
≥τ―θ |
|
ΔΌΤχΧ§ ±ΒΡ―’…Ϊ |
ΓΓ |
ΓΓ |
|
ΔΎΤχΈΕ |
ΓΓ |
ΓΓ |
|
ΔέΖ–Βψ±»Ϋœ |
ΓΓ |
|
|
ΔήΆ§ΧθΦΰ ±ΒΡΟήΕ»±»Ϋœ |
ΓΓ |
|
|
ΔίΆ§ΧθΦΰ ±Υ°÷–»ήΫβ–‘±»Ϋœ |
ΓΓ |
|
|
ΔόœύΜΞΙΊœΒ |
ΓΓ |
(2)≥τ―θΒΡΜ·―ß–‘÷ ΚΆ”ΟΆΨ
ΔΌ≤ΜΈ»Ε®–‘[2O3(g)=3O2(g)ΘΜΓςH= -284 kJ/mol ]Θ§ΥΒΟς―θΤχΒΡΈ»Ε®–‘±»≥τ―θΓΓΓΓΓΓ ΓΘ
ΔΎΦΪ«ΩΒΡ―θΜ·–‘Θ§ΡήΫΪAgΓΔHgΒ»≤Μ“Ή±ΜΩ’Τχ―θΜ·ΒΡΫπ τΕχ―θΜ·Θ§ΡήΫΪ”–Μζ…Ϊ÷ ―θΜ·Θ§Ι Ω…”ΟΉςΆ―…Ϊ(Τ·ΑΉ)ΦΝΘ§“≤ΨΏ”–…±ΨζœϊΕΨΉς”ΟΘ§‘ρ”÷Ω…”ΟΉςœϊΕΨΦΝΓΘ‘Ύ“ΜΕ®ΧθΦΰœ¬≥τ―θΚΆ―θΤχΩ…œύΜΞΉΣΜ·Θ§Τδ”–ΙΊΜ·―ßΖΫ≥Χ ΫΈΣΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ Θ§ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
1ΓΔ―θΉε‘ΣΥΊΒΡ‘≠Ή”ΫαΙΙΦΑ–‘÷ ΒΡœύΥΤ–‘ΚΆΒί±δ–‘
(1)ΫαΙΙΘΚ
œύΥΤ–‘ΘΚΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
Βί±δ–‘ΘΚΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
(2)–‘÷ (OΓζTe)
ΓΓΓΓ œύΥΤ–‘ΘΚ÷ς“ΣΜ·ΚœΦέΈΣΓΓΓΓΓΓΓΓΓΓ ΦέΘ§«βΜ·ΈοΒΡΆ® ΫΈΣΓΓΓΓΓΓΓΓ Θ§ΉνΗΏΦέ―θΜ·ΈοΕ‘”ΠΒΡΥ°Μ·ΈοΒΡΆ® ΫΈΣΓΓΓΓΓΓΓΓΓΓΓΓ ΓΓΓΘ
ΓΓΓΓ Βί±δ–‘ΘΚ‘ΣΥΊΖ«Ϋπ τ–‘÷πΫΞΓΓΓΓΓΓ Θ§H2RΈ»Ε®–‘÷πΫΞΓΓΓΓΓΓ Θ§H2RO4Υα–‘÷πΫΞΓΓΓΓΓΓ ΓΘ
ΙζΦ ―ß–Θ”≈―Γ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com